Streochemický termín diastereotopický označuje vztah mezi dvěma skupinami v molekule, jejichž záměnou by vznikly sloučeniny, které jsou diastereomery. Diastereotopické skupiny jsou často, ale ne vždy, identické skupiny připojené ke stejnému atomu v molekule obsahující alespoň jedno chirální centrum.
Například dva atomy vodíku molekuly CH2 v (S)-2-bromobutanu jsou diastereotopické. Nahrazením jednoho atomu vodíku (zbarveného modře) atomem bromu vznikne (2S,3R)-2,3-dibromobutan. Nahrazením druhého atomu vodíku (červeně) atomem bromu vznikne diastereomer (2S,3S)-2,3-dibromobutan.
 |
 |
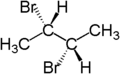 |
| (S)-2-bromobutan | (2S,3R)-2,3-dibromobutane | (2S,3S)-2,3-dibromobutan |
U chirálních molekul obsahujících diastereotopické skupiny, jako je tomu u 2-bromobutanu, není požadavek na enantiomerní nebo optickou čistotu; bez ohledu na svůj podíl bude každý enantiomer při substituci diastereomerních skupin vytvářet enantiomerní sady diastereomerů (ačkoli, jako v případě substituce bromem v 2-bromobutanu, mezoizomery nemají, přísně vzato, žádný enantiomer).
Diastereotopické skupiny nejsou navzájem zrcadlovými obrazy kolem žádné roviny. Vždy se liší, v jakémkoli prostředí, ale nemusí být rozlišitelné. Například oba páry vodíků CH2 v hydrochloridu ethylfenylalaninátu (PhCH2CH(NH3+)COOCH2CH3 Cl-) jsou diastereotopické a oba dávají páry odlišných signálů 1H-NMR v DMSO-d6 při 300 MHz, ale v podobném ethyl 2-nitrobutanoátu (CH3CH2CH(NO2)COOCH2CH3) dává pouze skupina CH2 vedle chirálního centra odlišné signály od svých dvou vodíků stejným přístrojem v CDCl3. Takové signály jsou často složité kvůli malým rozdílům v chemickém posunu, překrývání a další silné vazbě mezi geminálními hydrogeny. Na druhé straně dvě skupiny CH3 ipsenolu, které jsou od chirálního centra vzdáleny tři vazby, dávají samostatné 1H dublety při 300 MHz a samostatné 13C-NMR signály v CDCl3, ale diastereotopické hydrogeny v hydrochloridu ethylalaninátu (CH3CH(NH3+)COOCH2CH3 Cl-), rovněž tři vazby od chirálního centra, vykazují v DMSO-d6 sotva rozlišitelné 1H-NMR signály.

Diastereotopické skupiny vznikají také v achirálních molekulách. Například libovolný jeden pár vodíků CH2 v 3-pentanolu (obrázek 1) je diastereotopický, protože oba uhlíky CH2 jsou enantiotopické. Substituce kteréhokoli ze čtyř vodíků CH2 vytvoří dvě chirální centra najednou a dva možné produkty substituce vodíků na kterémkoli uhlíku CH2 budou diastereomery. Tento druh vztahu je často snadněji zjistitelný u cyklických molekul. Například jakákoli dvojice vodíků CH2 v cyklopentanolu (obrázek 2) je podobně diastereotopická, což lze snadno rozpoznat, protože jeden z vodíků v této dvojici bude cis ke skupině OH (na stejné straně čela kruhu), zatímco druhý k ní bude trans (na opačné straně).
Termín diastereotopický se také používá pro identické skupiny připojené ke stejnému konci alkenové části, které by při záměně vytvořily geometrické izomery (rovněž spadající do kategorie diastereomerů). Hydrogeny CH2 propenu jsou tedy diastereotopické, jeden je cis ke skupině CH3 a druhý k ní trans, a nahrazením jednoho nebo druhého CH3 by vznikl cis- nebo trans–2-buten.

Diastereotopičnost není omezena na organické molekuly, ani na skupiny vázané na uhlík, ani na molekuly s chirálními tetraedrickými (sp3-hybridizovanými) centry: například dvojice vodíků v libovolné skupině CH2 nebo NH2 v tris(ethylendiamin)chrom(III) iontu (Cr(en)33+), kde je kovové centrum chirální, jsou diastereotopické (obrázek 2).
Termíny enantiotopický a diastereotopický lze také použít pro plochy planárních skupin (zejména karbonylových skupin a alkenových motilit). Viz Cahn-Ingold-Prelogovo pravidlo priority.
