Trauma, Degeneration und Krankheiten machen oft eine chirurgische Reparatur oder einen Ersatz notwendig. Bei Gelenkschmerzen geht es in erster Linie darum, die Schmerzen zu lindern und zu einem gesunden und funktionellen Lebensstil zurückzukehren. Dies erfordert in der Regel den Ersatz von Skelettteilen wie Knien, Hüften, Fingergelenken, Ellbogen, Wirbeln, Zähnen und die Reparatur des Kiefers. Der weltweite Markt für Biomaterialien wird auf fast 24.000 Mio. $ geschätzt. Orthopädische und zahnmedizinische Anwendungen machen etwa 55 % des gesamten Biomaterialienmarktes aus. Im Jahr 2000 wurden mit orthopädischen Produkten weltweit mehr als 13 Mrd. $ umgesetzt, was einem Anstieg von 12 % gegenüber 1999 entspricht. Es wird erwartet, dass sich die Expansion in diesen Bereichen aufgrund einer Reihe von Faktoren fortsetzen wird, einschließlich der alternden Bevölkerung, einer zunehmenden Vorliebe jüngerer bis mittelalterlicher Kandidaten für chirurgische Eingriffe, Verbesserungen der Technologie und des Lebensstils, eines besseren Verständnisses der Körperfunktionalität, verbesserter Ästhetik und des Bedarfs an besserer Funktion.
Biomaterialien
Biomaterialien sind per Definition „eine nicht-medikamentöse Substanz, die sich für den Einsatz in Systemen eignet, die die Funktion von Körpergeweben oder -organen verbessern oder ersetzen“. Bereits vor einem Jahrhundert wurden künstliche Materialien und Geräte so weit entwickelt, dass sie verschiedene Bestandteile des menschlichen Körpers ersetzen können. Diese Materialien sind in der Lage, über längere Zeit mit Körperflüssigkeiten und -geweben in Kontakt zu kommen und dabei kaum oder gar keine unerwünschten Reaktionen hervorzurufen.
Geschichtliche Entwicklung der Biomaterialien
Einige der frühesten Anwendungen von Biomaterialien reichen bis ins alte Phönizien zurück, wo lockere Zähne mit Golddrähten zusammengebunden wurden, um künstliche Zähne mit benachbarten Zähnen zu verbinden. In den frühen 1900er Jahren wurden Knochenplatten erfolgreich eingesetzt, um Knochenbrüche zu stabilisieren und deren Heilung zu beschleunigen. In den 50er und 60er Jahren befanden sich Blutgefäßersatz in der klinischen Erprobung und künstliche Herzklappen und Hüftgelenke in der Entwicklung.
Konstruktionsfaktoren für Biomaterialien
Bereits in der Anfangsphase dieses Bereichs stellten Chirurgen und Ingenieure Material- und Konstruktionsprobleme fest, die zu einem vorzeitigen Verlust der Implantatfunktion durch mechanisches Versagen, Korrosion oder unzureichende Biokompatibilität der Komponente führten. Schlüsselfaktoren für die Verwendung eines Biomaterials sind seine Biokompatibilität, seine Biofunktionalität und – in geringerem Maße – seine Verfügbarkeit. Keramik ist ein idealer Kandidat für alle oben genannten Funktionen, mit Ausnahme ihres spröden Verhaltens.
Implantatmaterialien
Es ist allgemein anerkannt, dass kein Fremdmaterial, das in einen lebenden Körper eingebracht wird, vollständig kompatibel ist. Die einzigen Substanzen, die sich vollständig anpassen, sind die vom Körper selbst hergestellten (autogen), und jede andere Substanz, die als fremd erkannt wird, löst eine Art von Reaktion aus (Reaktion des Wirtsgewebes). Die vier Arten von Reaktionen, die unterschiedliche Möglichkeiten der Befestigung von Implantaten am muskulären Skelettsystem ermöglichen, sind in Abbildung 1 dargestellt.
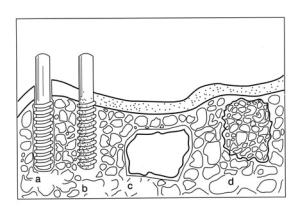
Abbildung 1. Klassifizierung von Biomaterialien nach ihrer Bioaktivität (a) bioinertes Aluminiumoxid-Zahnimplantat, (b) bioaktive Hydroxylapatit-Beschichtung auf einem metallischen Zahnimplantat, (c) oberflächenaktives Bioglas und (d) bioresorbierbares Tricalciumphosphat ( impant.
Klassifizierung von Biomaterialien
Wenn ein synthetisches Material in den menschlichen Körper eingebracht wird, reagiert das Gewebe je nach Materialtyp auf unterschiedliche Weise auf das Implantat. Der Mechanismus der Gewebereaktion (falls vorhanden) hängt von der Reaktion des Gewebes auf die Implantatoberfläche ab. Im Allgemeinen gibt es drei Begriffe, mit denen ein Biomaterial beschrieben oder klassifiziert werden kann und die die Reaktionen des Gewebes darstellen. Diese sind bioinert, bioresorbierbar und bioaktiv, die in einer Reihe von ausgezeichneten Übersichtsartikeln gut behandelt werden.
Bioinerte Biomaterialien
Der Begriff bioinert bezieht sich auf jedes Material, das nach dem Einsetzen in den menschlichen Körper nur eine minimale Wechselwirkung mit dem umgebenden Gewebe aufweist, z. B. Edelstahl, Titan, Aluminiumoxid, teilstabilisiertes Zirkoniumdioxid und ultrahochmolekulares Polyethylen. Im Allgemeinen kann sich um bioinerte Implantate eine faserige Kapsel bilden, so dass ihre Biofunktionalität von der Integration des Gewebes durch das Implantat abhängt (Abbildung 1a).
Bioaktive Biomaterialien
Bioaktiv bezieht sich auf ein Material, das nach dem Einsetzen in den menschlichen Körper mit dem umgebenden Knochen und in einigen Fällen sogar mit dem Weichgewebe interagiert. Dies geschieht durch eine zeitabhängige kinetische Veränderung der Oberfläche, die durch die Implantation in den lebenden Knochen ausgelöst wird. Eine Ionenaustauschreaktion zwischen dem bioaktiven Implantat und den umgebenden Körperflüssigkeiten führt zur Bildung einer biologisch aktiven Karbonat-Apatit-Schicht (CHAp) auf dem Implantat, die chemisch und kristallografisch der Mineralphase im Knochen entspricht. Beispiele für diese Materialien sind synthetisches Hydroxylapatit, Glaskeramik A-W und bioglass® (Abbildung 1b und c)).
Bioresorbierbare Biomaterialien
Bioresorbierbar ist ein Material, das sich nach dem Einsetzen in den menschlichen Körper aufzulösen beginnt (resorbiert wird) und langsam durch fortschreitendes Gewebe (wie Knochen) ersetzt wird. Gängige Beispiele für bioresorbierbare Materialien sind Tricalciumphosphat und Polymilchsäure-Polyglykolsäure-Copolymere. Kalziumoxid, Kalziumkarbonat und Gips sind weitere gängige Materialien, die in den letzten drei Jahrzehnten verwendet wurden (Abbildung 1d).
