


Mit der Anti-VEGF-Therapie erzielen Patienten mit neovaskulärer altersbedingter Makuladegeneration in der Regel deutliche Verbesserungen der Sehschärfe und der Lebensqualität. Während die kurzfristigen Ergebnisse geradezu spektakulär sind, bleiben einige wichtige Fragen zur langfristigen Behandlung dieser Patienten offen. Dazu gehören:
- Welches ist das beste Mittel?
- Wie oft sollte man behandeln?
- Verursacht die langfristige Einnahme dieser Mittel Sehkraftverlust und -schäden?
- Sind neue Plattformen für die langfristige Verabreichung dieser Wirkstoffe in Sicht?
- Dieser Artikel beantwortet diese Fragen auf der Grundlage der Ergebnisse von zulassungsrelevanten klinischen Studien.
Sind alle Anti-VEGF-Wirkstoffe gleich? Wie oft sollten wir behandeln?
Im Jahr 2006 belegten die wegweisenden Studien ANCHOR und MARINA die Wirksamkeit und Sicherheit von Ranibizumab (Lucentis, Roche/Genentech) bei monatlicher Verabreichung. Die Patienten verbesserten sich nach zwei Jahren um 10,7 bzw. 6,6 Buchstaben.1-2 In den parallel durchgeführten VIEW1- und VIEW2-Studien wurde eine mittlere Verbesserung der Sehkraft nach zwei Jahren mit Aflibercept (Eylea, Regeneron Pharmaceuticals) alle acht Wochen nach drei anfänglichen monatlichen Ladedosen nachgewiesen.3
Nachfolgende Studien ermöglichten es uns, die Wirksamkeit dieser Medikamente mit weniger häufigen Dosierungsintervallen zu untersuchen, einschließlich vierteljährlicher, pro re nata (PRN) und treat-and-extend-Schemata. Die PIER-Studie untersuchte die vierteljährliche Verabreichung von Ranibizumab nach einer dreimaligen monatlichen Ladedosis, und obwohl sie der Beobachtung überlegen war, verloren die PIER-Patienten nach einem Jahr 2,3 Buchstaben gegenüber dem Ausgangswert.4
Eine der frühesten Ausnahmen war PrONTO, eine Phase-I/II-Studie, in der 40 Patienten über einen Zeitraum von zwei Jahren mit monatlicher Überwachung und PRN-Retreatment auf der Grundlage von Sehschärfe, klinischer Untersuchung und optischen Kohärenztomographie-Parametern untersucht wurden.5 Die Ergebnisse der Sehschärfe kamen denen von ANCHOR und MARINA mit fast der Hälfte der Anzahl der Injektionen nahe, aber der Studie fehlte ein monatlicher Behandlungskontrollarm. Diese Ergebnisse konnten in nachfolgenden PRN-Studien nicht wiederholt werden.
In der HARBOR-Studie wurde die monatliche und die PRN-Dosierung von Ranibizumab verglichen. Die monatliche 0,5-mg-Gruppe gewann nach 24 Monaten 9,1 Buchstaben gegenüber 7,9 Buchstaben in der PRN-Gruppe. Dieser Unterschied war zwar statistisch nicht signifikant, aber die mediane Anzahl der Injektionen (nicht aber die Anzahl der Besuche) verringerte sich von 21,4 auf 13,3.6
CATT und IVAN waren ähnliche Studien, in denen die monatliche und die regelmäßige Gabe von Ranibizumab und Bevacizumab (Avastin, Roche/Genentech) verglichen wurden. Nach zwei Jahren erwies sich die PRN-Dosierung in beiden Studien (mit Ausnahme von PRN-Bevacizumab in der CATT-Studie) als nicht unterlegen gegenüber der monatlichen Behandlung, obwohl in den monatlichen Gruppen eine Tendenz zu besserem Sehvermögen bestand.7,8
TREX verglich eine monatliche Ranibizumab-Behandlung mit einem Behandlungs- und Verlängerungsschema (T&E).9 Auch hier war der Unterschied in der Sehschärfe statistisch nicht signifikant (10,5 in der monatlichen Gruppe und 8,7 in der T&E-Gruppe), tendierte aber zu einer besseren Sehkraft in der monatlichen Gruppe. Die durchschnittliche Anzahl der Injektionen betrug 25,5 gegenüber 18,6 über zwei Jahre. Außerdem verlor kein Patient der monatlichen Kohorte mehr als 2 Buchstaben, während fünf Patienten der T&E-Gruppe mindestens 3 Zeilen an Sehkraft verloren.
Während diese Studien kurzfristig statistisch ähnliche Ergebnisse bei monatlicher Verabreichung zeigten, waren die absoluten Ergebnisse bei monatlicher Verabreichung von Anti-VEGF-Mitteln fast einstimmig besser.
Wie geht es nach zwei Jahren weiter?
Die Daten aus diesen klinischen Studien sind nach zwei Jahren nicht so einfach zu interpretieren und anzuwenden wie die Daten aus den klinischen Studien, vor allem, weil in diesen Verlängerungsstudien hauptsächlich die langfristige Arzneimittelsicherheit untersucht wurde. Daher waren die Nachbeobachtungs- und Behandlungspläne nicht so streng.

HORIZON war die Erweiterungsstudie für die Patienten der Studien MARINA, ANCHOR und FOCUS. Diese Patienten folgten keinem Protokoll, sondern wurden nach dem Ermessen der Prüfärzte bei Evaluierungsbesuchen alle drei bis sechs Monate behandelt. Nach vier Jahren hatten die HORIZON-Patienten die anfänglichen Sehkraftgewinne im Wesentlichen wieder verloren und waren auf das Ausgangsniveau zurückgefallen (-0,1 Buchstaben).10 Eine weitere Datenanalyse ergab einen Zusammenhang zwischen besserer Sehkraft und mehr Injektionen.
In der CATT-Fünfjahresstudie wurden Patienten untersucht, die nach den ersten beiden Jahren der Studie nach dem Ermessen der Prüfärzte überwacht und behandelt wurden. Im Durchschnitt verloren die Patienten 3 Buchstaben im Vergleich zur Ausgangssituation. Die Patienten wurden im Durchschnitt achtmal pro Jahr untersucht und erhielten durchschnittlich fünf Behandlungen pro Jahr.11 Es wurde diskutiert, ob der Sehkraftverlust auf eine Unterbehandlung oder die Entwicklung einer Makulaatrophie zurückzuführen war, aber die Studie war nicht geeignet, um diesen Unterschied herauszufinden.12
Die VIEW-1-Erweiterungsstudie überwachte die Patienten strenger. Die Teilnehmer erhielten eine feste Dosierung im Abstand von >q8 Wochen, konnten aber auch häufigere Behandlungen erhalten, wenn sie vorgegebene Kriterien erfüllten. In dieser Erweiterungsstudie behielten die Patienten eine wesentlich bessere Sehkraft bei, mit einem durchschnittlichen Sehkraftgewinn von 7,1 Buchstaben gegenüber dem Ausgangswert (verglichen mit einem Gewinn von 10,4 Buchstaben beim primären Endpunkt nach einem Jahr).13
Was passiert langfristig und spielt die Häufigkeit der Behandlung eine Rolle?

Die besten Langzeitdaten, die wir haben, stammen aus Beobachtungsstudien. Die SEVEN-UP-Studie war eine Erweiterung der Ranibizumab-Studien. Obwohl es kein vorgegebenes Besuchsprogramm oder Injektionsprotokoll gab, liefern die Daten einige Informationen. Nach sieben Jahren hatten die Patienten im Durchschnitt 8,6 Buchstaben gegenüber dem Ausgangswert verloren. Patienten, die in den folgenden drei Jahren keine Injektionen erhielten, verloren 8,7 Buchstaben gegenüber dem Ausgangswert; diejenigen, die eine bis fünf Injektionen erhielten, verloren 10,8 Buchstaben; diejenigen, die sechs bis 10 Injektionen erhielten, verloren 6,9 Buchstaben; und diejenigen, die mehr als 11 Injektionen erhielten, gewannen 3,9 Buchstaben gegenüber dem Ausgangswert.14
Die Fight Retinal Blindness Study Group aus Australien beobachtete Patienten, die mit Anti-VEGF behandelt wurden, sieben Jahre lang. Diese Patienten verloren im Durchschnitt 2,6 Buchstaben gegenüber dem Ausgangswert, nachdem sie nach dem zweiten Jahr, in dem sie 4 Buchstaben gegenüber dem Ausgangswert hinzugewonnen hatten, durchschnittlich fünf Injektionen pro Jahr erhalten hatten.15
Die FIDO-Studie schließlich war eine Beobachtungsstudie an einem einzigen Zentrum, bei der in den ersten zwei Jahren eine feste Dosierung von 4 Wochen und danach von 8 Wochen verwendet wurde. Diese Patienten verbesserten sich gegenüber dem Ausgangswert um 12,1 Buchstaben (von einem Spitzenwert von 16,1 Buchstaben nach zwei Jahren) mit durchschnittlich 10,5 Injektionen pro Jahr.16
Die zentrale Botschaft dieser Langzeitbeobachtungsstudien ist, dass mehr Injektionen im Durchschnitt eindeutig zu einer besseren Sehkraft führen.

Wir haben jetzt 10-Jahres-Daten
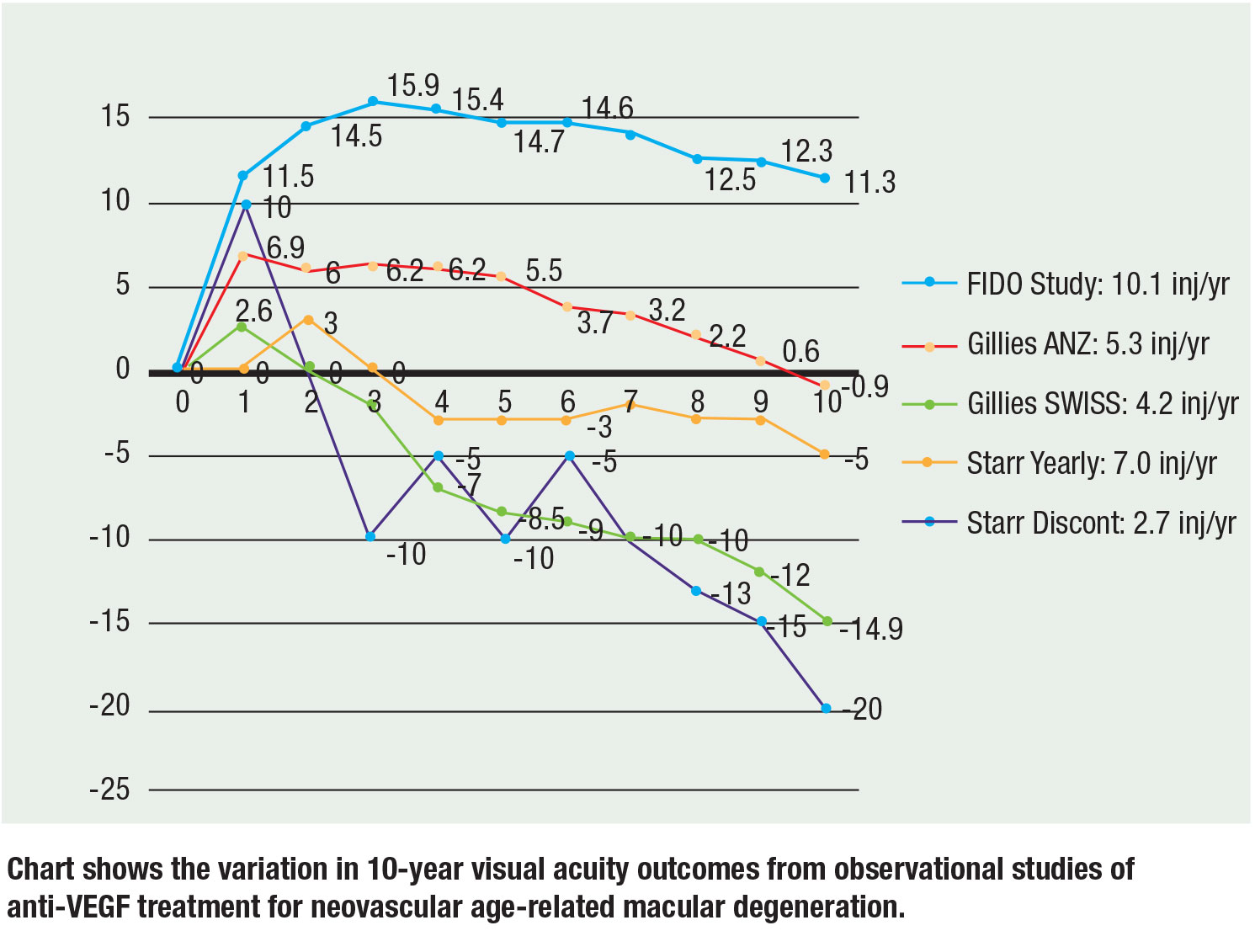
In jüngster Zeit haben drei große Beobachtungsstudien 10-Jahres-Daten vorgelegt, und die Ergebnisse bleiben gleich: Mehr Injektionen führen zu einer besseren Sehschärfe. Mark Gillies, MD, und Kollegen berichteten über Beobachtungsdaten aus Australien-Neuseeland und der Schweiz. Bei den ANZ-Patienten verringerte sich die durchschnittliche Sehkraft nach 10 Jahren um 0,9 Buchstaben gegenüber dem Ausgangswert, bei einem Median von 5,3 Injektionen/Jahr unter einem T&E-Schema, im Vergleich zu den Schweizer Patienten, deren Sehkraft sich um durchschnittlich 14,9 Buchstaben verringerte, bei einem Median von 4,2 Injektionen/Jahr unter PRN. Sie kamen zu dem Schluss, dass eine kontinuierliche Behandlung und mehr Injektionen zu einer besseren Sehkraft führen.17
Matthew Starr, MD, und Kollegen untersuchten eine Kohorte, die Patienten umfasste, die mindestens zwei Injektionen erhielten. Im Durchschnitt erhielten die Patienten fünf bis sieben Injektionen pro Jahr. Augen, die mindestens eine Injektion pro Jahr erhielten, verloren etwa 7 Buchstaben gegenüber dem Ausgangswert, während Augen, die nicht mindestens eine jährliche Injektion erhielten, 15 Buchstaben gegenüber dem Ausgangswert verloren.18
Unsere 10-jährige FIDO-Kohorte erreichte eine mittlere Zunahme der Sehkraft von 11,3 Buchstaben gegenüber einem Spitzenwert von 15,9 mit durchschnittlich 10,1 Injektionen pro Jahr während des Studienzeitraums.19
Es ist wichtig anzumerken, dass Vergleiche zwischen den Studien aufgrund der unterschiedlichen Ausgangssehschärfe und Patientenpopulationen mit Risiken behaftet sind, aber die Steigungen und Trends bestätigen die Korrelation zwischen mehr Injektionen und besserer Sehkraft. In der Abbildung (Seite 29) sind die 10-Jahres-Daten aus den drei Studien zusammengefasst.
Führt eine häufige Behandlung zu einem Fortschreiten der geografischen Atrophie?
Die Befürchtung eines Fortschreitens der geografischen Atrophie bei einer Anti-VEGF-Behandlung ist ein Grund zur Besorgnis und ein häufig angeführter Grund, nicht häufig zu behandeln. Einiges deutet darauf hin, dass das Risiko eines Sehkraftverlusts durch eine Unterbehandlung diese potenzielle Sorge bei weitem überwiegt. In der SEVEN-UP-Studie wurde eine höhere Inzidenz von GA in anderen Augen als in mit Anti-VEGF behandelten Augen festgestellt.14
Außerdem zeigten die 10-Jahres-Daten der FIDO-Studie eine etwas geringere Inzidenz von GA mit Sehkraftverlust nach 10 Jahren bei den behandelten Augen im Vergleich zu den unbehandelten Mitaugen (15 vs. 19 Prozent).19 Es ist wahrscheinlich, dass das Fortschreiten der echten GA unabhängig von der
Anti-VEGF-Behandlung ist und dass es sich um ein Austrocknen des neovaskulären Komplexes handelt, das wie GA aussieht, aber weniger schädliche Auswirkungen auf das Sehvermögen hat.
Fazit
Eine kontinuierliche, regelmäßige Behandlung mit Anti-VEGF-Mitteln liefert hervorragende Ergebnisse bei der Behandlung der feuchten AMD. Die Langzeitdaten zeigen, dass das Risiko eines Sehkraftverlusts bei einer Unterbehandlung größer ist als bei einer kontinuierlichen Behandlung in regelmäßigen Abständen, wie sie derzeit in Form von Dosierungen in festen Intervallen oder konservativen Treat-and-Extend-Schemata angewandt wird. Langfristige Verabreichungsplattformen wie das Port-Delivery-System und die Gentherapie scheinen vielversprechend zu sein, da sie die Hürden der Nichteinhaltung, die Belastung durch häufige Besuche und die Herausforderungen durch variable individuelle Dosierungsanforderungen verringern. RS
1. Brown DM, Kaiser PK, Michels M, et al. Ranibizumab versus Verteporfin bei neovaskulärer altersbedingter Makuladegeneration. N Engl J Med. 2006;355:1432-1444.
2. Rosenfeld PJ, Brown DM, Heier JS, et al. MARINA Study Group, Ranibizumab for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1419-1431.
3. Schmidt-Erfurth U, Kaiser PK, Korobelnik JF, et al. Intravitreale Aflibercept-Injektion bei neovaskulärer altersbedingter Makuladegeneration: Sechsundneunzig-Wochen-Ergebnisse der VIEW-Studien. Ophthalmology. 2014;121:193-201.
4. Regillo CD, Brown DM, Abraham P, et al. Randomized, double-masked, sham-controlled trial of ranibizumab for neovascular age-related macular degeneration: PIER-Studie Jahr 1. Am J Ophthalmol. 2008;145:239-248.
5. Lalwani GA, Rosenfeld PJ, Fung AE, et al. A variable-dosing regimen with intravitreal ranibizumab for neovascular age-related macular degeneration: year 2 of the PrONTO Study. Am J Ophthalmol. 2009;148:43-58.
6. Ho AC, Busbee BG, Regillo CD, et al, for the HARBOR Study Group. Vierundzwanzigmonatige Wirksamkeit und Sicherheit von 0,5 oder 2,0 mg Ranibizumab bei Patienten mit subfovealer neovaskulärer altersbedingter Makuladegeneration. Ophthalmology. 2014;121:2181-2192.
7. Martin DF, Maguire MG, Fine SL, et al, for the Comparison of Age-related Macular Degeneration Treatments Trials (CATT) Research Group. Ranibizumab und Bevacizumab zur Behandlung der neovaskulären altersbedingten Makuladegeneration: Zweijahresergebnisse. Ophthalmology. 2012;119:1388-1398.
8. Chakravarthy U, Harding SP, Rogers CA, et al. Alternative treatments to inhibit VEGF in age-related choroidal neovascularization: 2-year findings of the IVAN randomized control trial. Lancet. 2013;382:1258-1267.
9. Wykoff CC, Ou WC, Brown DM, et al. Randomisierte Studie zu Treat-and-Extend versus monatlicher Dosierung bei neovaskulärer altersbedingter Makuladegeneration: 2-Jahres-Ergebnisse der TREX-AMD-Studie. Ophthalmol Retina. 2017;1:314-321.
10. Singer MA, Awh CC, Sadda S, et al. HORIZON: An open-label extension trial of ranibizumab for choroidal neovascularization secondary to age-related macular degeneration. Ophthalmology. 2012;119:1175-1183.
11. Maguire MG, Martin DF, Ying GS, et al. Five-year outcomes with anti-vascular endothelial growth factor treatment of neovascular age-related macular degeneration: Der Vergleich von Studien zur Behandlung der altersbedingten Makuladegeneration. Ophthalmology. 2016;123:1751-1761.
12. Grunwald JE, Pistilli M, Ying GS, et al. Wachstum der geografischen Atrophie im Vergleich der Studien zur Behandlung der altersbedingten Makuladegeneration. Ophthalmology. 2015;122:809-816.
13. Kaiser PK, Singer M, Tolentino M, et al. Long-term safety and visual outcome of intravitreal aflibercept in neovascular age-related macular degeneration. Ophthalmol Retina. 2017;1:304-313.
14. Rofagha S, Bhisitkul RB, Boyer DS, Sadda SR, Zhang K, for the SEVEN-UP Study Group. et al. Seven-year outcomes in ranibizumab-treated patients in ANCHOR, MARINA, and HORIZON: A multicenter cohort study (SEVEN-UP). Ophthalmology. 2013;120:2292-2299.
15. Gillies MC, Campain A, Barthelmes D, et al, for the Fight Retinal Blindness Study Group. Long-term outcomes of treatment of neovascular age-related macular degeneration: Daten aus einer Beobachtungsstudie. Ophthalmology. 2015;122:1837-1845.
16. Peden MC, Suñer IJ, Hammer ME, Grizzard WS. Long-term outcomes in eyes receiving fixed-interval dosing of anti-vascular endothelial growth factor agents for wet age-related macular degeneration. Ophthalmology. 2015;122:803-808.
17. Gillies M, Arnold J, Bhandari S, et al. Ten-year outcomes of neovascular age-related macular degeneration from two regions. Am J Ophthalmol. 2020;210:116-124.
18. Starr MR, Kung FF, Bui YT, et al. Ten-year follow-up of patients with exudative age-related macular degeneration treated with intravitreal anti-vascular endothelial growth factor injections. Retina. Published online November 13, 2019.
19. Suñer IJ, Peden MC, Hammer ME, Grizzard WS. Ten-year outcomes in eyes receiving fixed-interval dosing of anti-vascular endothelial growth factor agents for wet age-related macular degeneration. Paper presented at Retina Society 2019; September 12, 2019; London, U.K.
20. Campochiaro PA, Marcus DM, Awh CC, et al. The port delivery system with ranibizumab for neovascular age-related macular degeneration: results from the randomized phase 2 LADDER clinical trial. Ophthalmology. 2019;126:1141-1154.
21. Ho AC; the Janssen/ORBIT Study Group. Precision delivery programs for cell and gene therapy. Paper presented at: Vail Vitrectomy Meeting; February 10, 2019; Vail, CO.
22. ADVM-022 Gentherapie für feuchte AMD (OPTIC). Sponsor: Adverum Biotechnologies. ClinicalTrials.gov Identifier: NCT03748784. Verfügbar unter: https://clinicaltrials.gov/ct2/show/NCT03748784. Accessed April 18, 2020.
23. RegenxBio meldet Finanz- und Betriebsergebnisse für das erste Quartal 2019 sowie ein weiteres positives Zwischen-Update der Phase I/IIa-Studie für RGX-314 zur Behandlung der feuchten AMD . Rockville, MD; May 7, 2019. https://www.prnewswire.com/news-releases/regenxbio-reports-first-quarter-2019-financial-and-operating-results-and-additional-positive-interim-phase-iiia-trial-update-for-rgx-314-for-the-treatment-of-wet-amd-300845423.html Zugriff am 9. Juli 2020.
