


Con la terapia anti-VEGF los pacientes con degeneración macular neovascular asociada a la edad suelen tener mejoras significativas en la agudeza visual y la calidad de vida. Aunque los resultados a corto plazo son espectaculares, persisten varias cuestiones importantes sobre el tratamiento a largo plazo de estos pacientes. Entre ellas se encuentran:
- ¿Cuál es el mejor agente?
- ¿Con qué frecuencia se debe tratar?
- ¿La dosificación a largo plazo de estos agentes provoca pérdida y daños en la visión?
- ¿Se vislumbran nuevas plataformas para la administración a largo plazo de estos agentes?
- Este artículo responde a estas preguntas basándose en los resultados de ensayos clínicos fundamentales.
¿Son todos los agentes anti-VEGF iguales? ¿Con qué frecuencia debemos tratarlos?
En 2006, los históricos estudios ANCHOR y MARINA demostraron la eficacia y seguridad de ranibizumab (Lucentis, Roche/Genentech) con dosis mensuales. Los pacientes ganaron 10,7 y 6,6 letras, respectivamente, a los dos años.1-2 Posteriormente, los estudios paralelos VIEW1 y VIEW2 mostraron una mejora media de la visión a los dos años con aflibercept (Eylea, Regeneron Pharmaceuticals) cada 8 semanas después de tres dosis iniciales de carga mensuales.3
Los ensayos posteriores permitieron evaluar la eficacia de estos fármacos empleando intervalos de dosificación menos frecuentes, incluyendo regímenes trimestrales, pro re nata (PRN) y de tratamiento y extensión. El estudio PIER examinó la dosificación trimestral con ranibizumab después de tres dosis de carga mensuales y, aunque fue superior a la observación, los pacientes del PIER perdieron 2,3 letras con respecto al valor inicial al año.4
Una de las primeras excepciones fue PrONTO, un ensayo de fase I/II que evaluó a 40 pacientes durante dos años con un seguimiento mensual y un retratamiento PRN basado en la agudeza visual, el examen clínico y los parámetros de la tomografía de coherencia óptica.5 Los resultados de agudeza visual se aproximaron a los de ANCHOR y MARINA con casi la mitad del número de inyecciones, pero el estudio carecía de un brazo de control de tratamiento mensual. Estos resultados no se han duplicado en ensayos PRN posteriores.
El ensayo HARBOR comparó la dosificación mensual y PRN de ranibizumab. El grupo de 0,5 mg mensuales ganó 9,1 letras a los 24 meses frente a las 7,9 letras del grupo PRN. Aunque esta diferencia no fue estadísticamente significativa, la mediana del número de inyecciones (pero no del número de visitas) se redujo de 21,4 a 13,3.6
CATT e IVAN fueron estudios similares que compararon la dosificación mensual y PRN de ranibizumab y bevacizumab fuera de etiqueta (Avastin, Roche/Genentech). A los dos años, se comprobó que la dosis PRN no era inferior al tratamiento mensual en ambos estudios (excepto en el caso del bevacizumab PRN en el CATT), aunque hubo una tendencia hacia una mejor visión en los grupos mensuales.7,8
TREX comparó el ranibizumab mensual con un régimen de tratamiento y extensión (T&E).9 Una vez más, la diferencia de agudeza visual no fue estadísticamente significativa (10,5 en el grupo mensual y 8,7 en el grupo T&E), pero hubo una tendencia hacia una mejor visión en el grupo mensual. El número medio de inyecciones fue de 25,5 frente a 18,6 en dos años. Además, ningún paciente de la cohorte mensual perdió más de 2 letras, mientras que cinco pacientes de T&E perdieron al menos 3 líneas de visión.
Aunque estos estudios han mostrado resultados estadísticamente similares con la dosificación mensual a corto plazo, los resultados de los datos absolutos han sido casi unánimemente superiores con la dosificación mensual de los agentes anti-VEGF.
¿Qué ocurre después de dos años?
Los datos más allá de dos años de estos ensayos clínicos no son tan fáciles de interpretar y aplicar como los datos de los ensayos clínicos, principalmente porque estos estudios de extensión evaluaron principalmente la seguridad del fármaco a largo plazo. Por lo tanto, el seguimiento y los programas de tratamiento no fueron tan rigurosos.

HORIZON fue el estudio de extensión para los pacientes de los ensayos MARINA, ANCHOR y FOCUS. Estos pacientes no siguieron un protocolo; recibieron el tratamiento a discreción de los investigadores durante las visitas de evaluación cada tres o seis meses. A los cuatro años, los pacientes de HORIZON perdieron esencialmente las ganancias de AV iniciales y retrocedieron a la visión de referencia (-0,1 letras).10 El análisis posterior de los datos descubrió una asociación entre la mejora de la visión y un mayor número de inyecciones.
El estudio CATT, de cinco años de duración, evaluó a los pacientes monitorizados y tratados a discreción de los investigadores tras los dos primeros años del ensayo. En promedio, los pacientes perdieron 3 letras en comparación con la visión inicial. Los pacientes fueron visitados una media de ocho veces al año y recibieron una media de cinco tratamientos al año.11 Se discutió si la pérdida de visión se debía a un tratamiento insuficiente o al desarrollo de atrofia macular, pero el ensayo no tenía la potencia necesaria para determinar esta diferencia.12
El estudio de extensión VIEW 1 realizó un seguimiento más riguroso de los pacientes. Los participantes recibieron dosis de intervalo fijo >q8 semanas, pero podían recibir tratamientos más frecuentes si cumplían los criterios preespecificados. En esta extensión, los pacientes conservaron una visión mucho mejor, con una ganancia media de visión de 7,1 letras desde el inicio (en comparación con una ganancia de 10,4 letras en el punto final primario de un año).13
¿Qué ocurre a largo plazo y qué importancia tiene la frecuencia de las dosis?

Los mejores datos a largo plazo que tenemos proceden de estudios observacionales. El estudio SEVEN-UP fue una extensión de los ensayos con ranibizumab. Aunque no había un programa de visitas preestablecido ni un protocolo de inyecciones, los datos proporcionan cierta información. A los siete años, los pacientes perdieron una media de 8,6 letras respecto a la situación inicial. Los pacientes que no recibieron inyecciones durante los tres años siguientes perdieron 8,7 letras con respecto al valor inicial; los que recibieron entre una y cinco inyecciones perdieron 10,8 letras; los que recibieron entre seis y diez inyecciones perdieron 6,9 letras; y los que recibieron más de 11 inyecciones ganaron 3,9 letras con respecto al valor inicial.14
El Fight Retinal Blindness Study Group de Australia observó a pacientes tratados con anti-VEGF durante siete años. Estos pacientes perdieron una media de 2,6 letras respecto a la línea de base, habiendo recibido una media de cinco inyecciones al año después del segundo año, cuando habían ganado 4 letras respecto a la línea de base.15
Por último, el estudio FIDO fue un estudio observacional de un solo centro en el que se utilizó una dosis fija de 4 semanas durante los dos primeros años y >8 semanas después. Estos pacientes ganaron 12,1 letras desde el inicio (desde un pico de 16,1 letras a los dos años) con una media de 10,5 inyecciones al año.16
El mensaje central de estos estudios observacionales a largo plazo es que claramente, en promedio, más inyecciones se traducen en una mejor visión.

Ahora tenemos datos a 10 años
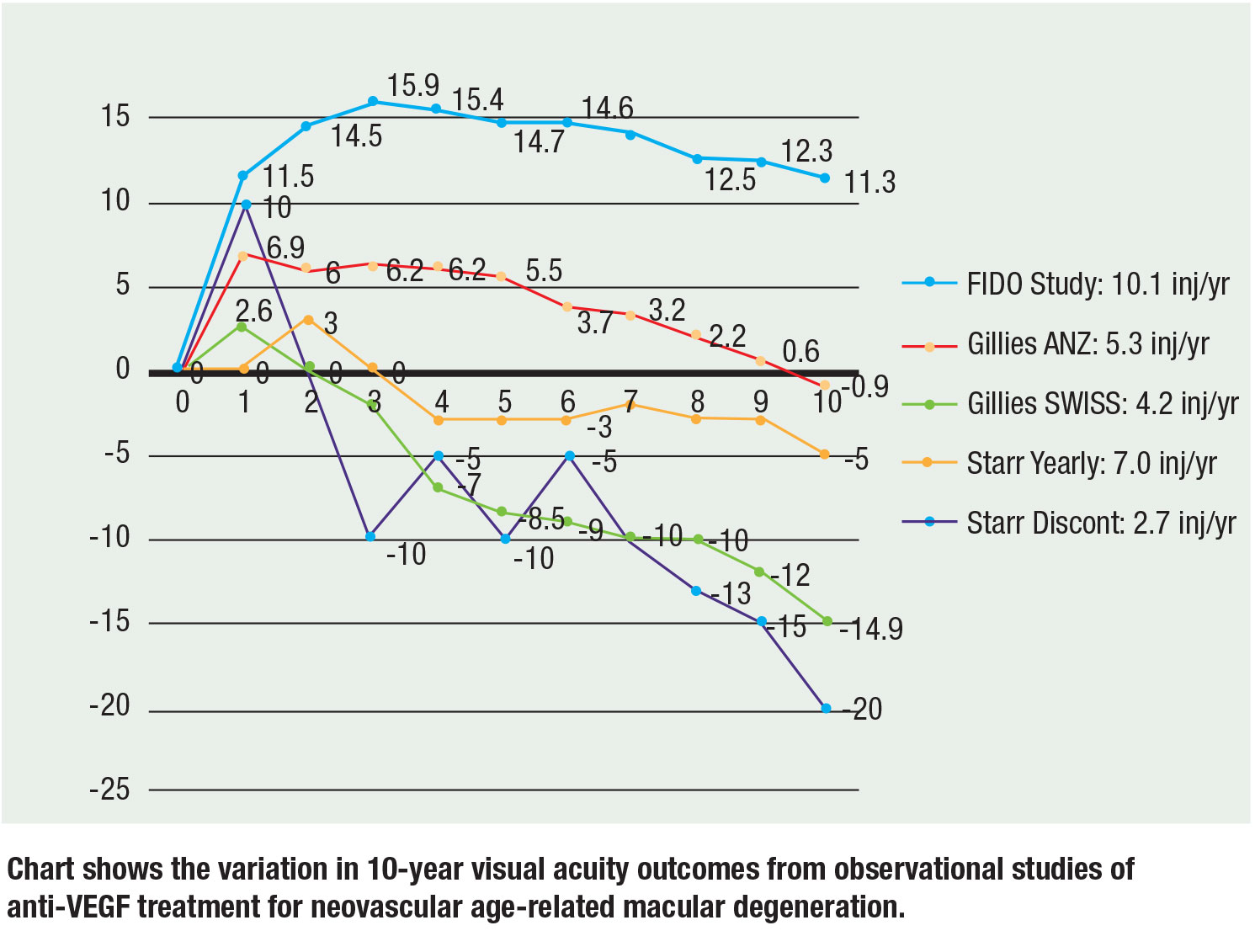
Recientemente, tres grandes estudios observacionales han reportado datos a 10 años y los resultados siguen siendo consistentes: Más inyecciones se traducen en una mejor agudeza visual. El Dr. Mark Gillies y sus colegas presentaron datos de observación de Australia-Nueva Zelanda y Suiza. En los pacientes de Australia-Nueva Zelanda, la visión media disminuyó en 0,9 letras con respecto a la línea de base a los 10 años, con una mediana de 5,3 inyecciones al año en un régimen de T&E, en comparación con los pacientes suizos, cuya visión disminuyó en una media de 14,9 letras con una mediana de 4,2 inyecciones al año en PRN. Su conclusión fue que el tratamiento continuo y un mayor número de inyecciones lograban una mejor visión.17
Matthew Starr, MD, y sus colegas evaluaron una cohorte que incluía a pacientes que recibieron al menos dos inyecciones. En promedio, los pacientes recibieron entre cinco y siete inyecciones al año. Los ojos que recibían al menos una inyección al año perdían aproximadamente 7 letras con respecto a la línea de base, mientras que los ojos que no recibían al menos una inyección anual perdían 15 letras con respecto a la línea de base.18
Nuestra cohorte de FIDO de 10 años logró un aumento medio de la visión de 11,3 letras desde un pico de 15,9 con una media de 10,1 inyecciones al año durante el período de estudio.19
Es importante señalar que existen riesgos inherentes a las comparaciones entre ensayos, dada la diferente agudeza visual inicial y las poblaciones de pacientes, pero las pendientes y las tendencias mantienen la correlación de más inyecciones con una mejor visión. La figura (página 29) resume los datos a 10 años de los tres ensayos.
¿El tratamiento frecuente da lugar a la progresión de la atrofia geográfica?
La preocupación por la progresión de la atrofia geográfica con el tratamiento anti-VEGF ha sido una preocupación y una razón frecuentemente invocada para no tratar con frecuencia. Algunas pruebas sugieren que el riesgo de pérdida de visión por el subtratamiento supera con creces esta posible preocupación. El ensayo SEVEN-UP mostró una mayor incidencia de AG en los ojos del compañero que en los ojos tratados con anti-VEGF.14
Además, los datos de FIDO a 10 años demostraron una incidencia ligeramente menor de AG con pérdida de visión a 10 años en los ojos tratados en comparación con los ojos contrarios no tratados (15 frente a 19%).19 Es probable que la progresión de la verdadera AG sea independiente del tratamiento con anti-VEGF, y que lo que se observe sea la desecación del complejo neovascular que se parece a la AG pero con un impacto menos perjudicial para la visión.
Línea de fondo
El tratamiento continuo y regular con agentes anti-VEGF proporciona resultados extraordinarios en el tratamiento de la DMAE húmeda. Los datos a largo plazo demuestran que el riesgo de pérdida de visión es mayor por el subtratamiento que por el tratamiento continuo a intervalos regulares, como se aplica actualmente en la dosificación a intervalos fijos o en los regímenes conservadores de tratar y prolongar. Las plataformas de administración a largo plazo, como el sistema de administración por puerto y la terapia génica, parecen prometedoras para disminuir las barreras del incumplimiento, la carga de las visitas frecuentes y los desafíos de los requisitos variables de dosificación individual. RS
1. Brown DM, Kaiser PK, Michels M, et al. Ranibizumab versus verteporfina para la degeneración macular neovascular relacionada con la edad. N Engl J Med. 2006;355:1432-1444.
2. Rosenfeld PJ, Brown DM, Heier JS, et al. MARINA Study Group, Ranibizumab for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1419-1431.
3. Schmidt-Erfurth U, Kaiser PK, Korobelnik JF, et al. Inyección intravítrea de aflibercept para la degeneración macular neovascular asociada a la edad: resultados de noventa y seis semanas de los estudios VIEW. Ophthalmology. 2014;121:193-201.
4. Regillo CD, Brown DM, Abraham P, et al. Ensayo aleatorio, doblemente enmascarado y controlado con simulacro de ranibizumab para la degeneración macular neovascular asociada a la edad: PIER Study year 1. Am J Ophthalmol. 2008;145:239-248.
5. Lalwani GA, Rosenfeld PJ, Fung AE, et al. Un régimen de dosis variable con ranibizumab intravítreo para la degeneración macular neovascular relacionada con la edad: año 2 del estudio PrONTO. Am J Ophthalmol. 2009;148:43-58.
6. Ho AC, Busbee BG, Regillo CD, et al, para el grupo de estudio HARBOR. Eficacia y seguridad a 24 meses de 0,5 o 2,0 mg de ranibizumab en pacientes con degeneración macular subfoveal neovascular relacionada con la edad. Ophthalmology. 2014;121:2181-2192.
7. Martin DF, Maguire MG, Fine SL, et al, para el grupo de investigación Comparison of Age-related Macular Degeneration Treatments Trials (CATT). Ranibizumab y bevacizumab para el tratamiento de la degeneración macular neovascular relacionada con la edad: resultados de dos años. Ophthalmology. 2012;119:1388-1398.
8. Chakravarthy U, Harding SP, Rogers CA, et al. Tratamientos alternativos para inhibir el VEGF en la neovascularización coroidea relacionada con la edad: hallazgos de 2 años del ensayo de control aleatorio IVAN. Lancet. 2013;382:1258-1267.
9. Wykoff CC, Ou WC, Brown DM, et al. Ensayo aleatorio de tratamiento y extensión frente a dosis mensuales para la degeneración macular neovascular relacionada con la edad: resultados de 2 años del estudio TREX-AMD. Ophthalmol Retina. 2017;1:314-321.
10. Singer MA, Awh CC, Sadda S, et al. HORIZON: Un ensayo de extensión abierto de ranibizumab para la neovascularización coroidea secundaria a la degeneración macular relacionada con la edad. Ophthalmology. 2012;119:1175-1183.
11. Maguire MG, Martin DF, Ying GS, et al. Resultados a cinco años con el tratamiento del factor de crecimiento endotelial antivascular de la degeneración macular relacionada con la edad neovascular: The comparison of age-related macular degeneration treatments trials. Ophthalmology. 2016;123:1751-1761.
12. Grunwald JE, Pistilli M, Ying GS, et al. Crecimiento de la atrofia geográfica en la comparación de los ensayos de tratamientos de degeneración macular relacionada con la edad. Ophthalmology. 2015;122:809-816.
13. Kaiser PK, Singer M, Tolentino M, et al. Seguridad a largo plazo y resultado visual de aflibercept intravítreo en la degeneración macular neovascular relacionada con la edad. Ophthalmol Retina. 2017;1:304-313.
14. Rofagha S, Bhisitkul RB, Boyer DS, Sadda SR, Zhang K, para el Grupo de Estudio SEVEN-UP. et al. Resultados a siete años en pacientes tratados con ranibizumab en ANCHOR, MARINA y HORIZON: Un estudio de cohortes multicéntrico (SEVEN-UP). Ophthalmology. 2013;120:2292-2299.
15. Gillies MC, Campain A, Barthelmes D, et al, para el grupo de estudio Fight Retinal Blindness. Resultados a largo plazo del tratamiento de la degeneración macular neovascular relacionada con la edad: Datos de un estudio observacional. Ophthalmology. 2015;122:1837-1845.
16. Peden MC, Suñer IJ, Hammer ME, Grizzard WS. Resultados a largo plazo en los ojos que reciben dosis de intervalo fijo de agentes del factor de crecimiento endotelial vascular para la degeneración macular húmeda relacionada con la edad. Ophthalmology. 2015;122:803-808.
17. Gillies M, Arnold J, Bhandari S, et al. Resultados a diez años de la degeneración macular neovascular relacionada con la edad de dos regiones. Am J Ophthalmol. 2020;210:116-124.
18. Starr MR, Kung FF, Bui YT, et al. Seguimiento a diez años de pacientes con degeneración macular exudativa asociada a la edad tratados con inyecciones intravítreas del factor de crecimiento endotelial vascular. Retina. Publicado en línea el 13 de noviembre de 2019.
19. Suñer IJ, Peden MC, Hammer ME, Grizzard WS. Resultados a diez años en ojos que reciben dosis de intervalo fijo de agentes del factor de crecimiento endotelial vascular para la degeneración macular húmeda relacionada con la edad. Documento presentado en la Retina Society 2019; 12 de septiembre de 2019; Londres, Reino Unido.
20. Campochiaro PA, Marcus DM, Awh CC, et al. El sistema de entrega de puerto con ranibizumab para la degeneración macular neovascular relacionada con la edad: resultados del ensayo clínico aleatorizado de fase 2 LADDER. Ophthalmology. 2019;126:1141-1154.
21. Ho AC; el grupo de estudio Janssen/ORBIT. Programas de entrega de precisión para la terapia celular y génica. Documento presentado en: Vail Vitrectomy Meeting; 10 de febrero de 2019; Vail, CO.
22. Terapia génica ADVM-022 para la DMAE húmeda (OPTIC). Patrocinador: Adverum Biotechnologies. Identificador de ClinicalTrials.gov: NCT03748784. Disponible en: https://clinicaltrials.gov/ct2/show/NCT03748784. Consultado el 18 de abril de 2020.
23. RegenxBio informa de los resultados financieros y operativos del primer trimestre de 2019 y de una actualización positiva adicional del ensayo provisional de fase I/IIa de RGX-314 para el tratamiento de la DMAE húmeda . Rockville, MD; 7 de mayo de 2019. https://www.prnewswire.com/news-releases/regenxbio-reports-first-quarter-2019-financial-and-operating-results-and-additional-positive-interim-phase-iiia-trial-update-for-rgx-314-for-the-treatment-of-wet-amd-300845423.html Consultado el 9 de julio de 2020.
