- ¿Qué es la entropía?
- ¿Qué es la tercera ley de la termodinámica?
- Importancia de la tercera ley de la termodinámica
La tercera ley de la termodinámica establece que a medida que la temperatura de un sistema se aproxima al cero absoluto, su entropía se hace constante, o el cambio de entropía es cero. La tercera ley de la termodinámica predice las propiedades de un sistema y el comportamiento de la entropía en un entorno único conocido como temperatura absoluta.
La entropía de un sistema acotado o aislado se hace constante a medida que su temperatura se acerca a la temperatura absoluta (cero absoluto).
La termodinámica es una de las ramas más importantes y ampliamente estudiadas de la ciencia física. Además de atormentar a los estudiantes de ingeniería mecánica durante la mayor parte de su vida académica, su ubicuidad se ve desde la fría brisa de mi aire acondicionado hasta una de las cimas de la era industrial: la máquina de vapor. Su aplicación se rige por tres leyes, que se conocen como las Leyes de la Termodinámica. Estas leyes definen cómo el trabajo, el calor y la energía afectan a un sistema. Un sistema es cualquier región del Universo que tiene un límite finito a través del cual se transfiere la energía. Todo lo que está fuera de este límite es su entorno.
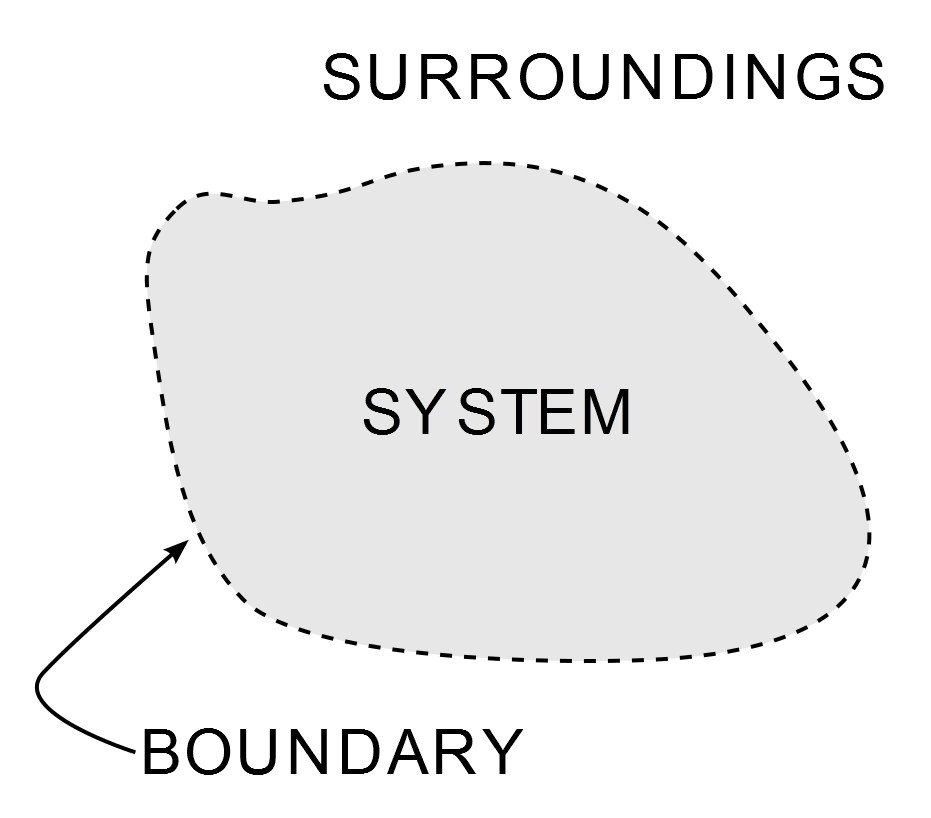
Ilustración de un sistema en termodinámica. (Photo Credit : Wavesmikey / Wikipedia Commons)
¿Qué es la entropía?
Mientras que la primera ley de la termodinámica implica que el Universo comenzó con una energía utilizable finita, en la que un sistema que extrae energía la gastará en parte haciendo trabajo y en parte mediante el aumento de su temperatura interna, la segunda ley explora sus implicaciones. Esto incluye la conversión de esta energía utilizable finita en energía no utilizable; por ejemplo, la formación de la materia que se produjo hace miles de millones de años debido a la condensación de la energía con la que comenzó el Universo. En este proceso, la energía finita utilizable se convierte ahora en energía inutilizable.
Esta energía no utilizable se mide con algo llamado «Entropía», un barómetro para medir la aleatoriedad o el desorden en un sistema.
Ilustración de la entropía como un aumento del desorden.
El Universo es como una habitación llena de ropa que está tirada de forma desordenada. La entropía de este sistema aumenta a medida que se usa y se desecha más y más ropa, complementando el desorden, a menos que el habitante se esfuerce por recogerla y organizarla, lo que reduce este desorden.
Considerando el Universo como un sistema, no hay nada en su entorno de donde derivar energía, así que con toda su energía convertida en energía inutilizable, todo lo que queda es un lugar frío y oscuro. Esto se llama muerte por calor y es una de las formas en que el Universo podría terminar. Un sistema acotado como nuestro Universo posee fuentes de energía finitas, como sus brillantes estrellas, que arderán durante eones antes de rendirse a las crueles leyes de la naturaleza.

¿Qué es la tercera ley de la termodinámica?
La tercera ley de la termodinámica predice las propiedades de un sistema y el comportamiento de la entropía en un entorno único conocido como temperatura absoluta. La temperatura absoluta es la temperatura más baja conocida y establece un límite inferior al rango de temperaturas del Universo.
¡Cómo mola! No, en serio, ¿qué tan frío es? La temperatura absoluta es 0 Kelvin, la unidad estándar de temperatura o -273,15 grados Celsius. La temperatura absoluta también se conoce como cero absoluto en algunos círculos y países. Esta escala te dará una idea.
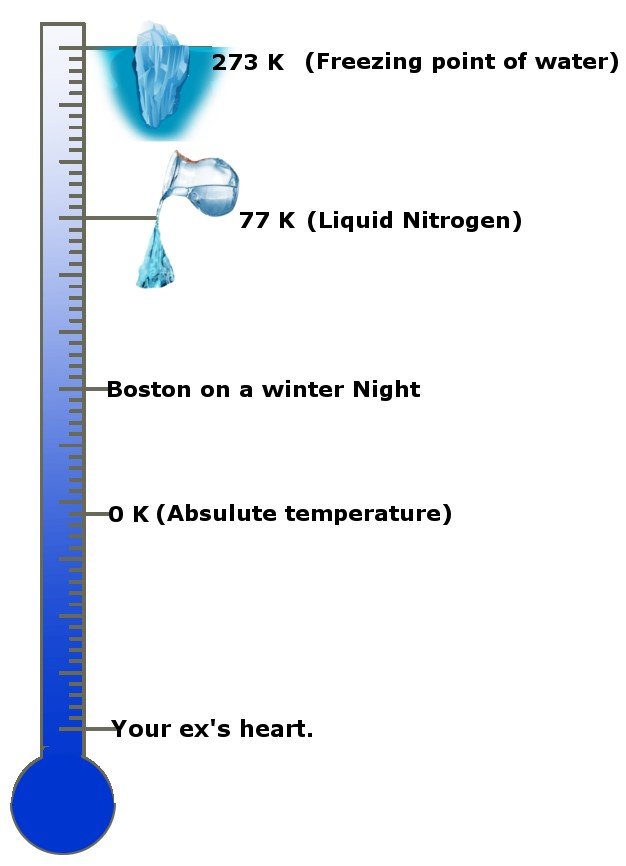
La tercera ley establece que a medida que la temperatura de un sistema se aproxima al cero absoluto, su entropía se hace constante, o el cambio de entropía es cero.

La afirmación se representa mediante esta ecuación, donde T se asemeja a la temperatura y delta S es el cambio en la entropía del sistema. La denotación «tiende a cero», representada por una flecha que apunta hacia cero, implica que a medida que la temperatura disminuye hasta un valor infinitesimal, el sistema alcanza una entropía constante extrayendo energía de su entorno, pero como dicta la primera ley, parte de esta energía se sumará a la energía interna del sistema, negando así un estado de entropía constante.
Importancia de la tercera ley de la termodinámica
La tercera ley es raramente aplicable a nuestro día a día y gobierna la dinámica de los objetos a las temperaturas más bajas conocidas. Define lo que se llama un «cristal perfecto», cuyos átomos están pegados en sus posiciones. El cristal perfecto, por tanto, no posee absolutamente ninguna entropía, lo que sólo se consigue a la temperatura absoluta.
El concepto de entropía también ha sido popular en algunas teorías que definen objetivamente el flujo continuo del tiempo, como el aumento lineal de la entropía del Universo.
En realidad, a 0 Kelvin, los cambios de entropía para las reacciones relativas a la formación de la materia serán nulos, aunque prácticamente toda la materia manifiesta alguna cantidad de entropía, debido a la presencia de la más mínima cantidad de calor. Lo más frío que hemos medido es 3 K, en las lejanas profundidades del Universo, más allá de las estrellas y las galaxias.
En otras palabras, ¡disfruta del verano mientras dure!
¿Qué es la Primera Ley de la Termodinámica?
¿Qué es la Segunda Ley de la Termodinámica?
