El término estereoquímico diastereotópico se refiere a la relación entre dos grupos de una molécula que, si se sustituyen, generarían compuestos que son diastereómeros. Los grupos diastereotópicos son a menudo, pero no siempre, grupos idénticos unidos al mismo átomo en una molécula que contiene al menos un centro quiral.
Por ejemplo, los dos átomos de hidrógeno de la fracción CH2 del (S)-2-bromobutano son diastereotópicos. La sustitución de un átomo de hidrógeno (coloreado en azul) por un átomo de bromo producirá (2S,3R)-2,3-dibromobutano. La sustitución del otro átomo de hidrógeno (coloreado en rojo) por un átomo de bromo producirá el diastereómero (2S,3S)-2,3-dibromobutano.
 |
 |
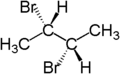 |
| (S)-2-bromobutano | (2S,3R)-2,3-dibromobutane | (2S,3S)-2,3-dibromobutano |
En las moléculas quirales que contienen grupos diastereotópicos, como en el caso del 2-bromobutano, no es necesaria la pureza enantiomérica u óptica; sin importar su proporción, cada enantiómero generará conjuntos enantioméricos de diastereómeros al sustituir los grupos diastereotópicos (aunque, como en el caso de la sustitución por bromo en el 2-bromobutano, los meso isómeros no tienen, estrictamente hablando, ningún enantiómero).
Los grupos diastereotópicos no son imágenes especulares entre sí sobre cualquier plano. Son siempre diferentes, en cualquier entorno, pero pueden no ser distinguibles. Por ejemplo, ambos pares de hidrógenos CH2 en el hidrocloruro de fenilalaninato de etilo (PhCH2CH(NH3+)COOCH2CH3 Cl-) son diastereotópicos y ambos dan pares de señales distintas de 1H-NMR en DMSO-d6 a 300 MHz, pero en el similar 2-nitrobutanoato de etilo (CH3CH2CH(NO2)COOCH2CH3), sólo el grupo CH2 junto al centro quiral da señales distintas de sus dos hidrógenos con el mismo instrumento en CDCl3. Estas señales suelen ser complejas debido a las pequeñas diferencias en el desplazamiento químico, el solapamiento y un fuerte acoplamiento adicional entre los hidrógenos gemínicos. Por otra parte, los dos grupos CH3 del ipsenol, que están a tres enlaces del centro quiral, dan dobletes 1H separados a 300 MHz y señales 13C-NMR separadas en CDCl3, pero los hidrógenos diastereotópicos del hidrocloruro de alaninato de etilo (CH3CH(NH3+)COOCH2CH3 Cl-), también a tres enlaces del centro quiral, muestran señales 1H-NMR apenas distinguibles en DMSO-d6.

Los grupos diastereotópicos también surgen en las moléculas quirales. Por ejemplo, cualquier par de hidrógenos CH2 en el 3-pentanol (Figura 1) son diastereotópicos, ya que los dos carbonos CH2 son enantiotópicos. La sustitución de cualquiera de los cuatro hidrógenos CH2 crea dos centros quirales a la vez, y los dos posibles productos de sustitución del hidrógeno en cualquier carbono CH2 serán diastereómeros. Este tipo de relación suele ser más fácil de detectar en las moléculas cíclicas. Por ejemplo, cualquier par de hidrógenos CH2 en el ciclopentanol (Figura 2) son igualmente diastereotópicos, y esto se discierne fácilmente ya que uno de los hidrógenos del par será cis respecto al grupo OH (en el mismo lado de la cara del anillo) mientras que el otro será trans respecto a él (en el lado opuesto).
El término diastereotópico también se aplica a grupos idénticos unidos al mismo extremo de una fracción de alqueno que, si se sustituyen, generarían isómeros geométricos (que también entran en la categoría de diastereómeros). Así, los hidrógenos CH2 del propeno son diastereotópicos, siendo uno de ellos cis al grupo CH3, y el otro trans al mismo, y la sustitución de uno u otro por CH3 generaría cis- o trans–2-buteno.

La diastereotopicidad no se limita a las moléculas orgánicas, ni a los grupos unidos al carbono, ni a las moléculas con centros tetraédricos quirales (hibridados sp3): por ejemplo, el par de hidrógenos en cualquier grupo CH2 o NH2 en el ion tris(etilendiamina)cromo(III) (Cr(en)33+), donde el centro metálico es quiral, son diastereotópicos (Figura 2).
Los términos enantiotópico y diastereotópico también pueden aplicarse a las caras de los grupos planares (especialmente a los grupos carbonilos y a las mocidades de los alquenos). Ver la regla de prioridad de Cahn-Ingold-Prelog.
