- What is Entropy?
- What’s the Third Law of Thermodynamics?
- Ważność trzeciego prawa termodynamiki
Trzecie prawo termodynamiki stwierdza, że w miarę jak temperatura układu zbliża się do zera bezwzględnego, jego entropia staje się stała lub zmiana entropii wynosi zero. Trzecie prawo termodynamiki przewiduje właściwości systemu i zachowanie entropii w unikalnym środowisku znanym jako temperatura bezwzględna.
Trzeciorzędowa entropia systemu ograniczonego lub izolowanego staje się stała, gdy jego temperatura zbliża się do temperatury bezwzględnej (zera bezwzględnego).
Termodynamika jest jedną z najważniejszych i najszerzej badanych gałęzi nauk fizycznych. Poza dręczeniem studentów inżynierii mechanicznej przez większość ich życia akademickiego, jej wszechobecność jest widoczna od zimnego powiewu mojego klimatyzatora do jednego z szczytowych osiągnięć ery przemysłowej – silnika parowego. Jej realizacją rządzą trzy prawa, które znane są jako Prawa Termodynamiki. Prawa te określają, w jaki sposób praca, ciepło i energia wpływają na system. System to dowolny obszar we Wszechświecie, który jest ograniczony w sposób skończony i przez który przekazywana jest energia. Wszystko poza tą granicą jest jego otoczeniem.
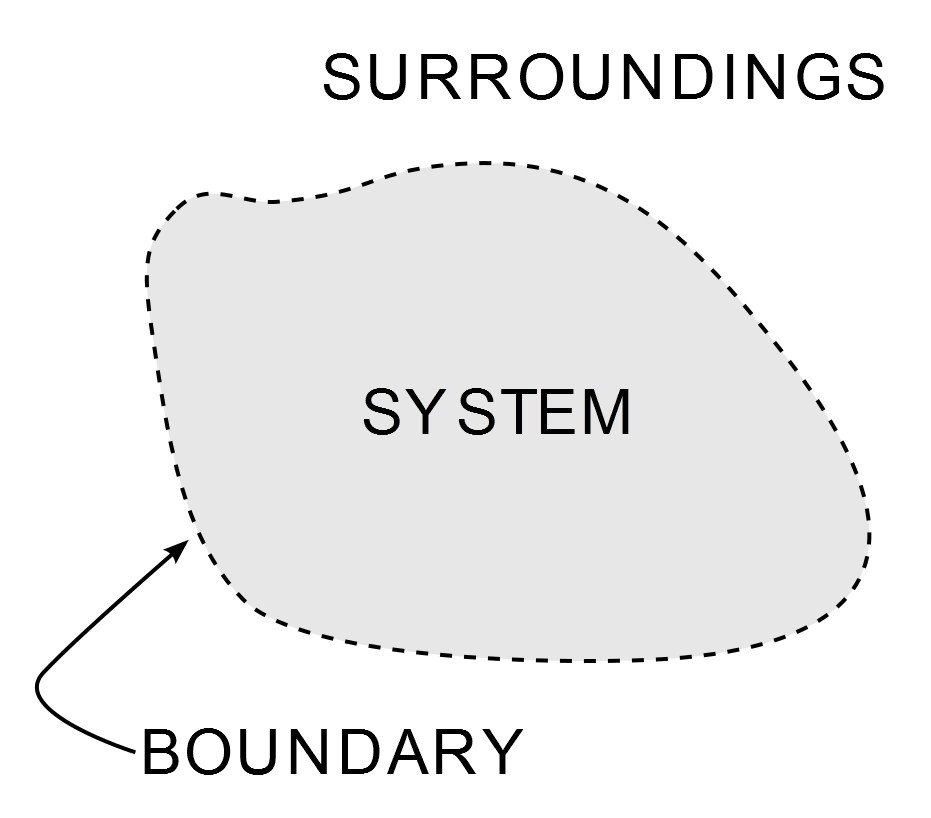
Ilustracja systemu w termodynamice. (Photo Credit : Wavesmikey / Wikipedia Commons)
What is Entropy?
While pierwsze prawo termodynamiki implikuje, że Wszechświat rozpoczął się ze skończoną energią użytkową, gdzie system pobierający energię częściowo wyda ją na wykonanie pracy, a częściowo wyda ją poprzez zwiększenie swojej temperatury wewnętrznej, drugie prawo bada jego implikacje. Obejmuje to przekształcenie tej skończonej energii użytkowej w energię nieużyteczną; na przykład formowanie się materii, które miało miejsce miliardy lat temu w wyniku kondensacji energii, z którą rozpoczął się Wszechświat. W tym procesie, skończona energia użytkowa jest teraz przekształcana w energię nieużyteczną.
Ta nieużyteczna energia jest mierzona przez coś zwanego „Entropią”, barometr do pomiaru przypadkowości lub nieuporządkowania w systemie.
Ilustracja entropii jako wzrostu nieuporządkowania.
Wszechświat jest jak pokój wypełniony ubraniami, które leżą wokół w niezorganizowany sposób. Entropia tego systemu wzrasta, ponieważ coraz więcej ubrań jest używanych i wyrzucanych, uzupełniając bałagan, chyba że mieszkaniec podejmuje wysiłek, aby je pozbierać i uporządkować, co zmniejsza ten nieporządek.
Patrząc na Wszechświat jako jeden system, nie ma nic w jego otoczeniu, z czego mógłby czerpać energię, więc z całą jego energią zamienioną na energię bezużyteczną, wszystko, co pozostaje, to zimne, ciemne miejsce. Nazywa się to śmiercią cieplną i jest jednym ze sposobów, w jaki Wszechświat może się skończyć. System ograniczony, taki jak nasz Wszechświat, posiada skończone źródła energii, takie jak jego jasne gwiazdy, które będą płonąć przez eony, zanim poddadzą się okrutnym prawom natury.

Co to jest trzecie prawo termodynamiki?
Trzecie prawo termodynamiki przewiduje właściwości systemu i zachowanie entropii w unikalnym środowisku znanym jako temperatura absolutna. Temperatura absolutna jest najniższą znaną temperaturą i wyznacza dolną granicę zakresu temperatur Wszechświata.
Jakie to fajne! Nie, poważnie, jak zimne to jest? Temperatura absolutna to 0 Kelwinów, standardowa jednostka temperatury lub -273,15 stopni Celsjusza! Temperatura absolutna jest również znana jako zero absolutne w niektórych kręgach i krajach. Ta skala da Ci wyobrażenie.
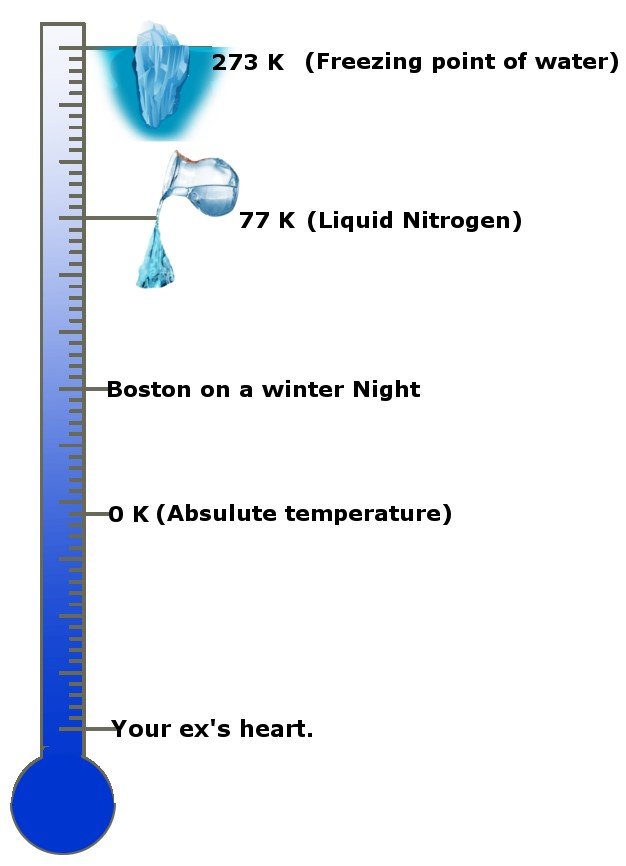
Trzecie prawo mówi, że gdy temperatura układu zbliża się do zera bezwzględnego, jego entropia staje się stała lub zmiana entropii wynosi zero.

Stwierdzenie to jest reprezentowane przez to równanie, gdzie T przypomina temperaturę, a delta S jest zmianą entropii układu. Określenie „dąży do zera” reprezentowane przez strzałkę skierowaną w stronę zera oznacza, że w miarę obniżania się temperatury do nieskończenie małej wartości, układ osiąga stałą entropię pobierając energię z otoczenia, ale jak nakazuje pierwsze prawo, część tej energii doda się do energii wewnętrznej układu, zaprzeczając w ten sposób stałemu stanowi entropii.
Importance of the third law of thermodynamics
Trzecie prawo rzadko ma zastosowanie w naszym codziennym życiu i rządzi dynamiką obiektów w najniższych znanych temperaturach. Definiuje ono tak zwany „kryształ doskonały”, którego atomy są przyklejone do swoich pozycji. Idealny kryształ posiada zatem absolutnie zerową entropię, która jest osiągalna tylko w temperaturze absolutnej.
Koncepcja entropii była również popularna w niektórych teoriach definiujących ciągły przepływ czasu w sposób obiektywny, takich jak liniowy wzrost entropii Wszechświata.
Idealnie, w temperaturze 0 Kelwinów, zmiany entropii dla reakcji dotyczących powstawania materii będą równe zeru, chociaż praktycznie cała materia przejawia pewną ilość entropii, dzięki obecności najmniejszej ilości ciepła. Najzimniejsza zmierzona temperatura wynosi 3 K, w odległej głębi Wszechświata, poza gwiazdami i galaktykami.
Innymi słowy, ciesz się latem, póki trwa!
Co to jest Pierwsze Prawo Termodynamiki?
Co to jest Drugie Prawo Termodynamiki?
.
