Introducere
Boala pulmonară obstructivă cronică (BPOC) este o cauză semnificativă de mortalitate și morbiditate în întreaga lume modernă. Rata de mortalitate a acestei boli este în creștere și se preconizează că va deveni a treia cauză de deces la nivel mondial până în 2020.1 Nu este posibil să se definească BPOC doar pe baza volumului expirator forțat în 1s (FEV1), astfel încât Inițiativa globală pentru boala pulmonară obstructivă cronică (GOLD) a elaborat o definiție multidimensională pentru evaluarea BPOC.2 Noua definiție include prevalența simptomelor și istoricul anterior al exacerbărilor, pe lângă valoarea FEV1 și, de asemenea, pune accentul pe evaluarea comorbidităților. Pentru a evalua simptomele, se recomandă fie testul modificat al Consiliului de Cercetare Medicală (mMRC), fie testul de evaluare a BPOC (CAT). În plus, pentru a evalua impactul bolii asupra vieții de zi cu zi a fost utilizată o scală de calitate a vieții specifică bolii (SGRQ, SF-36, CCQ). Unele studii au demonstrat o relație puternică între CAT și chestionarul St. George’s Respiratory Questionnaire (SGRQ).3,4 Ladeira et al.5 au arătat că CAT a fost corelat cu indicele BODE.
BPOC este o boală complexă și include componente genetice, celulare și moleculare. Există multe celule și molecule diferite implicate în căile inflamatorii. Mai mulți indicatori au fost utilizați pentru a demonstra o potențială inflamație sistemică legată de boală.6-9 Inflamația căilor respiratorii și a parenchimului pulmonar este un mecanism patogenic major al BPOC. În plus, inflamația sistemică persistentă poate fi asociată cu o serie de comorbidități extrapulmonare și efecte pulmonare.10 Cercetările recente au furnizat dovezi ale existenței unui „nou fenotip inflamator sistemic distinct al BPOC”. 7 Într-un studiu recent, s-a demonstrat că comorbiditatea cardiovasculară și diabetul au fost asociate cu niveluri mai ridicate pentru unii markeri ai inflamației sistemice.11 Prin urmare, încărcătura genetică, inflamația sistemică și bolile comorbide sunt asociate cu diverse fenotipuri în BPOC. Este esențial ca noi perspective să fie dezvoltate în gestionarea acestei boli.
În prezent, CAT a fost utilizată din ce în ce mai mult pentru evaluarea și monitorizarea BPOC. Deși au fost definiți mai mulți biomarkeri serici în BPOC, nu există un singur biomarker unic suficient și eficient care să poată fi utilizat pentru a evalua starea pacienților cu BPOC. S-a demonstrat că biomarkerii sunt asociați cu mai mulți parametri, cum ar fi inflamația, spitalizarea și mortalitatea.7-13 Cu toate acestea, relația dintre CAT și biomarkeri nu a fost demonstrată în mod clar. Prin urmare, studiul de față își propune să investigheze nivelurile de inflamație sistemică în BPOC și să determine relația dintre CAT și markerii de inflamație și calitatea vieții.
Materiale și metodeDesignul studiului
Acesta a fost un studiu observațional transversal cu o singură vizită. O sută zece pacienți cu BPOC diagnosticați conform criteriilor GOLD14 și șaizeci și cinci de subiecți de control au fost recrutați între februarie 2013 și august 2013. Subiecții de control au fost aleși dintre cei trimiși la o clinică de pneumologie și medicină internă de la Spitalul Universitar Balikesir, supuși unor investigații de rutină. A fost obținut consimțământul în cunoștință de cauză în scris de la toți participanții, iar studiul a fost aprobat de Comitetul de etică instituțională al Facultății de Medicină din cadrul Universității Balikesir.
Toți pacienții au fost supuși unui examen fizic, radiografiei toracice, testului funcției respiratorii și testelor de analiză sanguină de rutină. Au fost înregistrate numărul de exacerbări din anul anterior și istoricul fumatului. Scorul de dispnee CAT, mMRC a fost realizat prin interviuri față în față de către specialistul în pneumologie. Scorurile SGRQ au fost raportate de către pacienți. Pentru grupul de control sănătos au fost efectuate doar un test al funcției respiratorii și teste de analiză sanguină de rutină.
Populația studiului
Criterii de includere: Pacienții au fost incluși dacă: (1) aveau peste 40 de ani; (2) erau fumători actuali sau foști fumători cu un istoric de fumat ≥10 pachete-ani; (3) prezentau un FEV1 post-bronhodilatator
80% și un FEV1/FVC0,7. Subiecții de control au fost incluși dacă: (1) aveau peste 40 de ani; (2) nu sufereau de boli pulmonare, după cum a stabilit un medic; (3) prezentau o spirometrie normală (FEV1>85% și FEV1/FVC>0,7); și (4) aveau un istoric de fumat de
Criterii de excludere: Au fost excluși pacienții care; (1) au avut o exacerbare a BPOC în ultimele 6 săptămâni; (2) au avut o afecțiune respiratorie, alta decât BPOC sau o afecțiune malignă; (3) au avut o boală inflamatorie cronică (vasculită, boală inflamatorie intestinală, poliartrită reumatoidă etc.) (4) avea o boală concomitentă necontrolată sau severă (infarct miocardic, aritmie etc.).
Măsuri
Caracteristicile demografice, vârsta, sexul, obiceiul de a fuma, admiterea la un serviciu de urgență sau spitalizarea în ultimul an, bolile însoțitoare și tratamentele existente au fost toate înregistrate în mod corespunzător. Am definit o exacerbare ca fiind o agravare a simptomelor care a necesitat corticosteroizi orali și/sau antibiotice și/sau spitalizare. Bolile comorbide au fost stabilite pe baza istoricului clinic și a constatărilor examenului fizic din timpul vizitei și au fost susținute de o revizuire a dosarelor medicale disponibile. Au fost documentate medicamentele curente, inclusiv inhalatoarele, antihipertensivele sau alte medicamente. Au fost măsurate înălțimea, greutatea și indicii IMC și s-a efectuat, de asemenea, o spirometrie în conformitate cu orientările internaționale (ATS/ERS).15 Boala a fost clasificată în conformitate cu vechea și noua versiune a stadializării GOLD.14 În primul rând, stadializarea spirometrică GOLD (stadializarea bazată pe FEV1 (1-4)) și, în al doilea rând, stadializarea GOLD (clasa A-D). Dispneea a fost evaluată prin scara de dispnee mMRC.16 Pacienții cu BPOC au fost clasificați în categoriile A, B, C și D, combinând evaluarea simptomelor prin scorurile de dispnee mMRC și riscul de exacerbare.
CAT: Valabilitatea și fiabilitatea versiunii turcești a acestei scale a fost verificată anterior.17 CAT include 8 itemi și produce scoruri totale cuprinse între 0 și 40; scorurile mai mari indică o afectare mai severă a stării de sănătate sau un control mai puțin reușit al BPOC.3
Chestionarul de calitate a vieții: Calitatea vieții a fost evaluată prin utilizarea traducerii turcești a chestionarului St. George’s Respiratory Diseases Questionnaire (SGRQ).18
Biomarkeri
Am ales biomarkerii pe baza studiilor anterioare.7,9-13 Probele de sânge prelevate de la toți subiecții au fost centrifugate și păstrate la -80°C. Toate probele au fost analizate la finalizarea studiului. Serul a fost studiat într-un dispozitiv de diagnosticare (BioTek, ELx 800, SUA) cu utilizarea unor kituri comerciale (eBioscience, Human TNF-α și Human IL-6 Platinum ELISA, Austria) și cu metodele de testare a necrozei tumorale alfa (TNF-α) și a unui nivel de interleukină-6 (IL-6) prin testul imunoenzimatic (ELISA). Nivelurile de proteină C-reactivă (CRP) au fost evaluate cu un analizor de chimie clinică (Cobes Integra 800, Roche diagnostics) folosind un kit comercial. Valoarea de referință a CRP este de 0-0,5mg/L, în timp ce cea mai mică valoare analizată a IL-6 este de 0,92pg/ml. Cea mai mică valoare analizată a TNFα este de 2,3pg/ml. Concentrațiile de TNF-α și IL-6 din unele probe au fost sub limita inferioară de cuantificare (LLQ). În analiza indivizilor cu valori sub LLQ, a fost utilizat un nivel nominal de jumătate din valoarea LLQ pentru a evita o denaturare în jos a datelor din populație.19
Analiză statistică
Valorile medii ale CRP din grupurile BPOC și de control (3,2 (1,5,7,1), 1,3 (0,6,2,7)) au fost identificate din studii similare.7 După aceea, în fiecare grup, dimensiunea eșantionului a fost calculată prin utilizarea formulei de calcul a mediei cu o precizie de 80% și o eroare de 5%. În consecință, s-a constatat că dimensiunea eșantionului trebuie să fie de cel puțin 55 de subiecți în fiecare grup. Rezultatele sunt prezentate ca medie±SD, mediană sau procent, după caz. Testul t al lui Student și ANOVA au fost utilizate pentru testele parametrice; testul U al lui Mann-Whitney, Kruskal-Wallis și statisticile chi pătrat au fost utilizate pentru testele neparametrice pentru comparațiile între grupuri. Testul exact al lui Fisher a evaluat diferențele dintre procentele de comorbidități și diferențele dintre sexe. Testul chi-pătrat a evaluat diferențele dintre procentele de comorbidități. Corelația perechilor de variabile continue la pacienții cu BPOC a fost examinată prin corelația Pearson. O valoare de p
0,05 a fost considerată semnificativă din punct de vedere statistic. Toate analizele statistice au fost efectuate cu softul SPSS (versiunea 20.0).RezultateCaracterizarea clinică a subiecților
Studiul a inclus 110 pacienți (vârsta medie de 64±8,9 ani; 100 de sex masculin (90,9%)), și 65 de subiecți de control (vârsta medie de 61,5±9,2 ani, 55 de sex masculin (84,6%)). Caracteristicile demografice și clinice ale grupurilor de pacienți și de control sunt prezentate în tabelul 1. Patruzeci și cinci (40,9%) de pacienți cu BPOC aveau o boală însoțitoare (cardiopatie ischemică (n=21), hipertensiune arterială (n=13), diabet zaharat (n=8), altele (n=3)). Media FEV1 a fost de 48,8% din valoarea prognozată, iar media FEV1/FVC: 55,4% în grupul BPOC. Scorul mediu CAT a fost de 22,6 (±9,2), mMRC: 1,9 (±0,9) și SGRQ total: 58,4 (±22,2). Dintre cei 110 pacienți, 9,1% au fost în stadiul 1, 37,3% în stadiul 2, 42,7% în stadiul 3, 10,9% în stadiul 4, în conformitate cu stadializarea spirometrică GOLD. Când pacienții au fost clasificați în funcție de stadializarea GOLD, 27,3% au fost grupa A, 30,9% au fost grupa B, 7,3% au fost grupa C și 34,5% au fost grupa D.
Caracteristici demografice, funcționale, clinice ale grupurilor de pacienți și de control.
| Pacient (n=110) | Control (n=65) | p-valoare | ||
|---|---|---|---|---|
| Vârsta | 64.0±8.9 | 61.5±9.2 | 0,080 | |
| Bărbați n, (%) | 100 (90,9) | 55 (84.6) | 0,224 | |
| BMI, kg/m2 | 26,5±5,6 | 25±2,6 | 0.064 | |
| Pack-years | 38,9±23 | 0,1±1,2 | ||
| Co-morbidități, n (%) | ||||
| Orice | 65 (59.1) | 42 (64,6) | 0,95 | |
| Cardiopatie ischemică | 21(19,1) | 11 (16,9) | ||
| HT | 13 (11.8) | 6 (9.2) | ||
| DM | 8 (7.3) | 4 (6.2) | ||
| Altele | 3 (2.7) | 2 (3,1) | ||
| mMRC | 1,94±0,9 | 0,04±0,2 | ||
| FEV1, % prezis | 48,8±17.8 | 89.4±5.6 | ||
| FVC, % prezis | 68.7±17.8 | 92.1±5.8 | ||
| FEV1/FVC, % | 55.4±12,9 | 89,6±4,7 | ||
| Stadiul spirometric GLOR, n (%) | ||||
| 1 | 10 (9.1) | |||
| 2 | 41 (37.3) | |||
| 3 | 47 (42.7) | |||
| 4 | 12 (10.9) | |||
| Stadiul GOLD, n (%) | ||||
| A | 30 (27.3) | |||
| B | 34 (30.9) | |||
| C | 8 (7,3) | |||
| D | 38 (34.5) | |||
| SGRQ-scoring total | 58,4±22,2 | |||
| Scoring CAT | 22.6±9,2 | |||
| TNFα (pg/ml) | 109,5±58 | 14,6±18 | ||
| IL-6 (pg/ml) | 10.3±18 | 2,14±1,9 | ||
| CRP (mg/L) | 1,6±1,7 | 0,4±0,3 | ||
Abbreviații: IMC, indicele de masă corporală, HT: hipertensiune arterială, DM: diabet, FEV1: volum expirator forțat în 1 secundă, FVC: capacitate vitală forțată, CAT: COPD assessment test.
COPD/controlează
Nu a existat nicio diferență semnificativă între vârstele (p=0,080, testul t Student) și sexele celor două grupuri (p=0,453, testul exact al lui Fisher) (tabelul 1). Grupurile au prezentat incidențe similare ale comorbidităților (p=0,095, testul χ2). Așa cum era de așteptat, pacienții cu BPOC au avut parametrii funcției pulmonare (VEMS, CVF, VEMS1/CVF) semnificativ mai mici comparativ cu controalele (p
0,001, testul t Student). În general, pacienții cu BPOC au prezentat niveluri serice mai mari de CRP (1,6±1,7mg/L) și TNF-α (109,5±58pg/ml) și IL-6 (10,3±18pg/ml) decât controalele sănătoase (CRP: 0,4±0,3mg/L, p0,001; TNF-α: 14,6±18pg/ml, p0,001; IL-6: 2,14±1,9pg/ml, p0,001, Student’s t-test) (Tabelul 1).Asocierea între chestionarele CAT și caracteristicile pacienților
A existat o corelație între scorul CAT și stadiul spirometric GOLD (Pearson’s r=0,43; p
0,001). Scorul CAT a crescut în paralel cu severitatea bolii. A existat o relație semnificativă din punct de vedere statistic între scorul CAT și numărul de exacerbări în anul precedent (Pearson’s r=0,35, p0,001), durata bolii (Pearson’s r=0,29, p0,001), fumatul (pachet-an) (Pearson’s r=0,27, p=0,014) și mMRC (Pearson’s r=0,59, p0,001). S-a constatat că scorul CAT a fost corelat în mod semnificativ cu FEV1 (Pearson’s r=-0,39, p0,001) și FVC (Pearson’s r=-42, p=0,003). În același timp, a fost observată o corelație puternică între scorul CAT și scorurile SGRQ privind simptomele, activitatea, impactul și scorul total (Pearson’s r=0,72; p0,001).Asocierea dintre biomarkeri și caracteristicile pacienților
Asociația dintre markerii inflamatori și parametrii funcției pulmonare a fost comparată. Pe măsură ce FEV1 a scăzut, nivelurile de biomarker au crescut semnificativ. Nivelurile CRP au fost corelate cu FEV1 (Pearson’s r=-0,39, p
0,001), FVC (Pearson’s r=-0,33, p0,001) și FEV1/FVC (Pearson’s r=-0,38, p0,001). Nivelurile de TNF-α au fost, de asemenea, corelate cu FEV1 (Pearson’s r=-0,57, p0,001), FVC (Pearson’s r=-0,37, p0,001) și FEV1/FVC (Pearson’s r=-0,66, p0,001). Nivelurile de IL-6 au fost, de asemenea, corelate cu FEV1 (Pearson’s r=-0,31, p0,001), FVC (Pearson’s r=-0,32, p0,001) și FEV1/FVC (Pearson’s r=-0,34, p0,001). S-a observat o corelație semnificativă între CRP, TNF-α, IL-6 și fumat (pachet-an) (Pearson’s r=0,35, r=0,44, r=0,27, p0,001, respectiv). Pacienții cu BPOC cu boli cardiovasculare au avut un nivel crescut de CRP (2,98±2.4mg/L) în comparație cu pacienții fără comorbidități (1,56±1,5mg/L, p=0,008 test ANOVA urmat de testul post hoc LSD). Nu a existat nicio asociere semnificativă cu alți biomarkeri și comorbidități. Pe măsură ce IL-6 a crescut, scorul mMRC a crescut, dar această relație nu a fost semnificativă din punct de vedere statistic (p=0,06). Atunci când markerii inflamatori au fost comparați cu scorul CAT, s-a demonstrat că nivelurile CRP au avut o corelație semnificativă (r=0,43, p0,001) (Fig. 1), în timp ce nu s-a observat nicio corelație cu TNF-α și IL-6. A existat o corelație între nivelurile CRP și TNFα (r=0,48, p0,001). Nu a fost observată nicio asociere directă între biomarkeri și clasa A-D sau stadiile spirometrice.
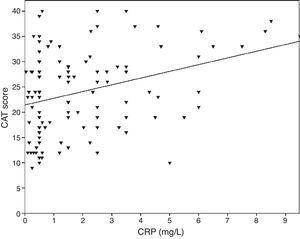
Relația dintre scorurile CAT și CRP (r=0,43, p0,001).
Discuție
Pentru evaluarea BPOC sunt utilizate unele instrumente de evaluare, cum ar fi testele clinice (CAT, BODE), markerii de inflamație și chestionarele de calitate a vieții. Este general acceptat faptul că este necesară o evaluare multidimensională pentru a înțelege și gestiona boala. BPOC este o afecțiune complexă, cu o componentă sistemică, iar unii pacienți par să aibă un fenotip inflamator. În acest studiu, CAT a fost efectuată ca un nou test clinic și a fost investigată relația dintre CAT și alte componente ale BPOC.
Una dintre aceste componente este inflamația sistemică. Biomarkerii cel mai des studiați în BPOC pentru a indica inflamația sistemică, care sunt utilizați în mod obișnuit, sunt CRP, IL-6, TNF-α, IL-8 și fibrinogenul. Mai multe studii au raportat anterior niveluri circulante ridicate ale acestor markeri la pacienții cu BPOC stabilă.6-9,20-23 Într-un studiu recent, Agustí et al. au arătat că 30% dintre pacienții cu BPOC nu prezentau dovezi de inflamație sistemică, iar 16% dintre pacienți prezentau o inflamație sistemică persistentă.7 Interesant este faptul că, în acest studiu, nivelurile serice ale TNF-α și IL-8 s-au dovedit a fi mai ridicate la fumătorii cu spirometrie normală în comparație cu pacienții cu BPOC. Ceilalți markeri precum globulele albe, IL-6, CRP și fibrinogenul s-au dovedit a fi mai mari la pacienții cu BPOC decât la fumătorii cu spirometrie normală și la nefumători. În studiul nostru, nivelurile de CRP, TNF-α, IL-6 au fost semnificativ mai mari la toți pacienții cu BPOC în comparație cu grupul de control. S-a constatat că toți biomarkerii au fost corelați cu expunerea cumulativă la fumat și cu reducerea parametrilor testelor funcționale pulmonare (FEV1, FVC și FEV1/FVC). Nivelul biomarkerilor se raportează la gradul de obstrucție a fluxului de aer. Aceste rezultate sunt în concordanță cu cele raportate în studii transversale anterioare.13 Într-un alt studiu care a examinat rezultatele ECLIPSE, comorbiditățile cardiovasculare și diabetul au fost corelate cu unii markeri ai inflamației sistemice.9 În studiul nostru, pacienții cu BPOC cu afecțiuni cardiovasculare au avut un nivel crescut al CRP în comparație cu pacienții fără comorbidități. Inflamația sistemică crescută la BPOC cu boli cardiovasculare susține un mecanism fiziopatologic între BPOC și aceste comorbidități.
Relația dintre CAT și inflamația sistemică nu a fost clarificată de studiile efectuate până în prezent. Într-un studiu, s-a demonstrat că există o corelație semnificativă între LCN1, LCN2 și CAT.8 În studiul nostru, s-a demonstrat o relație semnificativă între CAT și CRP. Cu toate acestea, o corelație similară nu a putut fi demonstrată cu TNF-α și IL-6.
În studiul de față, pacienții cu BPOC au fost clasificați în patru grupe (A-D) și stadii (1-4) în conformitate cu vechea și noua versiune a clasificării GOLD. Se poate observa că stadiul 1 și stadiul 4 constituie cea mai mică proporție din populație, cu 10% fiecare, în conformitate cu vechea clasificare. În noua versiune, populația a fost distribuită aproape în mod egal între grupele A, B și D; cea mai mică distribuție a fost cea a grupei C. În alte studii, s-a demonstrat, de asemenea, că grupa C constituie cea mai mică proporție din distribuție.24,25 Noua clasificare indică faptul că pot exista unii pacienți cu simptome multiple, dar cu obstrucții ușoare ale căilor respiratorii, precum și unii pacienți cu puține simptome, dar cu obstrucții severe ale căilor respiratorii. Comorbiditățile și inflamația sistemică pot duce la creșterea exacerbării și a simptomelor la pacienții cu obstrucție ușoară/moderată și, în acest fel, face ca acești pacienți să fie plasați în grupele cu risc ridicat (clasa C sau D). Într-un studiu, s-a demonstrat că subtipul C include pacienții cu o stare de comorbiditate mai mare, iar subtipul D include pacienții cu cea mai severă exacerbare, o rată ridicată de exacerbare legată de spitalizare și cele mai slabe rezultate.26 Într-un studiu recent, Agustí et al. au comparat două grupuri cu și fără inflamație sistemică persistentă și au arătat că pacienții care prezintă inflamație persistentă în timpul urmăririi au avut rate de exacerbare mai mari pe an în comparație cu celălalt grup, deși anomaliile pulmonare au fost similare în aceste două grupuri.7
GOLD recomandă utilizarea scalei CAT sau mMRC pentru evaluarea simptomelor. Am folosit scala mMRC pentru atribuirea grupurilor, deoarece atunci când am luat în considerare simptomele pe baza CAT, numărul pacienților cu mai puțin de 10 puncte de ruptură a fost foarte mic (8 pacienți). Scorurile CAT mai mari pot fi asociate cu percepțiile mai mari ale simptomelor pacienților. S-a demonstrat, de asemenea, că CAT și mMRC nu sunt echivalente, iar acest lucru poate cauza unele diferențe în clasificare.24,25,27 În noua clasificare, celelalte puncte de tăiere sunt compuse din numărul de exacerbări pe an. Relația dintre scorul CAT bazal și frecvența exacerbărilor a fost demonstrată la pacienții cu BPOC.28 Pothirat et al. au arătat că modificarea scorului CAT în timpul vizitelor de monitorizare este un instrument util pentru detectarea deteriorării acute a stării de sănătate a pacienților cu BPOC.29 În studiul nostru, s-a observat o relație puternică între CAT, mMRC și ratele exacerbărilor. S-a constatat, de asemenea, că CAT a fost corelat cu durata bolii și cu fumatul (pachet-an). S-a constatat că FEV1 mediu al pacienților a fost de 48,8% din valoarea prognozată, iar scorul mediu CAT a fost de 22,6. A fost evidențiată o asociere puternică între CAT și FEV1, FVC și stadiul spirometric GOLD. Pe măsură ce FEV1 și FVC au scăzut, scorul CAT a crescut. De asemenea, scorul CAT s-a corelat pozitiv cu un stadiu GOLD mai greu. Aceste rezultate arată că CAT reflectă foarte bine severitatea bolii.
O altă componentă importantă a managementului BPOC este calitatea vieții. O varietate de chestionare de viață au fost utilizate pentru a evalua efectele bolii asupra vieții de zi cu zi. Fiabilitatea și validitatea versiunii turcești a SGRQ au fost dovedite.30 Câteva studii au arătat că a fost observată o corelație semnificativă între CAT și SGRQ.3,4 Într-un studiu, s-a raportat că CAT este sensibilă la modificarea stării de sănătate asociată cu exacerbările BPOC.31 În studiul nostru, a fost demonstrată o relație puternică între CAT și SGRQ. Deoarece CAT, în comparație cu SGRQ, este un test mai scurt și mai ușor de înțeles, utilizarea CAT este mai practică.
Studiul de față are mai multe limitări, cum ar fi designul transversal, un studiu cu un singur centru și dimensiunea mică a eșantionului. În plus, markerii de inflamație nu au putut fi comparați la fumătorii care au o funcție pulmonară normală, deoarece aceștia nu au fost incluși în prezentul studiu. Medicamentele pentru pacienți pot exercita o influență asupra răspunsului inflamator sistemic și a stării de sănătate și, de asemenea, pot afecta rezultatele.
În concluzie, CAT este un test care poate fi utilizat în evaluarea BPOC, deoarece fiabilitatea și validitatea sa au fost clar demonstrate. Rezultatele studiului nostru indică relația dintre CAT și CRP, precum și alte componente ale BPOC (parametrii clinici, funcționali). Cu toate acestea, sunt necesare studii multicentrice longitudinale pentru a evalua relația dintre CAT și biomarkeri.
Dezvăluiri eticeProtecția subiecților umani și a animalelor
Autorii declară că nu au fost efectuate experimente pe oameni sau animale pentru acest studiu.
Confidențialitatea datelor
Autorii declară că au respectat protocoalele centrului lor de lucru privind publicarea datelor pacienților și că toți pacienții incluși în studiu au primit informații suficiente și și-au dat consimțământul informat în scris pentru a participa la studiu.
Dreptul la intimitate și consimțământul informat
Autorii au obținut consimțământul informat în scris al pacienților sau subiecților menționați în articol. Autorul corespondent este în posesia acestui document.
Autoritate
Designul studiului: NS, FE și AAH; Colectarea datelor: NS, CB; Analiza și interpretarea datelor: NS, AAH și CB; Revizuirea critică a manuscrisului: NS, FE, CB și AAH.
Conflicte de interese
Autorii declară că nu au conflicte de interese în pregătirea acestui manuscris.
.
