Redaktørens note: Platinum Highlight-artikler er bemærkelsesværdige publikationer, der med jævne mellemrum udvælges af Dr. Craig Reynolds, associeret direktør, National Cancer Institute, blandt de senest udgivne Platinum-publikationer.![]()
Når Alison Rattray og kolleger i Gene Regulation and Chromosome Biology Laboratory (GRCBL) undersøgte en mutant gærcelle, som de havde isoleret i en screening, bemærkede de noget mærkeligt.
DNA’et udviste en “meget specifik, men underlig omlægning”, forklarede hun. Arrangementet viste sig at være et DNA-palindrom, “hvilket åbnede døren til at studere disse flygtige DNA-motiver”, sagde hun.
Rattray, der er videnskabelig medarbejder i GRCBL, NCI Center for Cancer Research, sagde, at selv om deres opdagelse fandt sted for en række år siden, fortsætter deres gruppe med at studere DNA-reparation og omarrangementer, der resulterer i unormal reparation “på grund af forbindelsen med visse kræftformer”. Gruppens mål er at forstå oprindelsen af disse omlægninger bedre, tilføjede hun.
Rattray er en vigtig bidragyder til forskning rapporteret i BMC Genomics, der beskriver gruppens nyudviklede metode til genom-dækkende sekventering af DNA-palindromer i en kræftcellelinje.
Hvad er et DNA-palindrom?
En palindromisk sekvens af nukleotider (som er mærket med A, T, C eller G) opstår, når komplementære DNA-strenge læser det samme i begge retninger, enten fra 5-prime-enden eller 3-prime-enden. For eksempel betragtes sekvensen GGATCC på den ene DNA-streng som et palindrom, fordi sekvensen på den komplementære streng er CCTAGG.
På grund af sekvensens komplementaritet kan palindromiske sekvenser også folde sig tilbage på sig selv og danne hårnålesløjfer eller korsformede sekvenser, der er udskudt fra den normale dobbelthelix, sagde Rattray. “Små hårnåle er ikke problematiske, men når palindromer er lange (mere end 100 basepar), forstyrrer de normale cellulære processer såsom transkription og replikation,” forklarede hun.
Nogle kræftceller udviser massive genomomlægninger, som omfatter genamplifikationer, translokationer og deletioner, og disse omlægninger er ofte forbundet med tilstedeværelsen af et palindrom, hvilket tyder på en mulig korrelation mellem palindromet og genomlægningerne. Hvordan disse hændelser opstår, er ikke velforstået. Det, man ved, er imidlertid, at sådanne omlægninger er forbundet med kræftens udvikling og prognose, sagde Rattray.
Ny hypotese om genomisk omlægning
Ifølge Rattray tyder den foretrukne model, der oprindeligt blev foreslået for mere end 60 år siden af Barbara McClintock, Ph.D., på, at søsterkromatider efter et kromosombrud replikerer og smelter sammen og skaber et kromosom med to centromer, der er forbundet af et DNA-palindrom. I McClintocks model fører det at have to centromerer til yderligere genomiske omlægninger.
Rattray sagde imidlertid, at hendes gruppe og andre har vist, at “DNA-palindromer er ustabile og kan føre til genomiske omlægninger i sig selv, hvilket yderligere tyder på, at palindromer ikke kun kan opstå ved søsterkromatidfusion, men også ved andre mekanismer, såsom replikationsfejl.”
Gruppen opstillede den hypotese, at “i kræftformer, der gennemgår massive omlægninger, er cellerne modtagelige for palindromdannelse, og når de er dannet, fører palindromets ustabilitet til yderligere omlægninger, herunder genamplifikation, translokationer og deletioner,” sagde Rattray. “Enhver genomlægning er mutagen, og omlægninger, der fremmer cellevækst, som i kræft, vil naturligvis blive begunstiget af selektion.”
Ny teknologi identificerer og karakteriserer palindromer
Forskerne har udviklet en teknologi, som vil gøre det muligt for dem at undersøge tumorer med det formål at forstå sandsynligheden for palindromdannelse i disse tumorer, sagde Rattray. De håber at lære, hvilke begivenheder der initierer sådanne ustabile dannelser, og denne nye forståelse kan føre til nye behandlinger. For eksempel, sagde hun, har gruppen allerede fastslået, at visse gærceller, der er modtagelige for palindromdannelse, er langt mere følsomme end normale celler over for stråling samt over for forbindelser, der ofte anvendes i behandlingen af kræft, såsom cisplatin.
“I øjeblikket forsøger jeg at etablere metoder til selektivt at berige palindromer fra resten af det cellulære DNA, hvilket vil give større følsomhed i analysen af palindromindholdet i kræftceller,” sagde hun. Med den tidligere metode mistede forskerne de forbindelsessekvenser, der kunne give ledetråde til palindromernes oprindelse, og måtte analysere dem en efter en, forklarede hun. “Vi har nu vist, at PacBio-platformen let kan sekventere gennem et DNA-palindrom”, sagde hun.
Rattray fik sin doktorgrad ved University of Washington i Seattle, hvor hun studerede retroviral replikation. Efter et postdoc-stipendium på Columbia University, hvor hun studerede DNA-rekombination og rearrangementer induceret af DNA-dobbeltstrengsbrud i gær, kom hun til NCI i Frederick, hvor hun arbejdede i laboratoriet under Jeffrey Strathern, ph.d., chef for GRCBL.
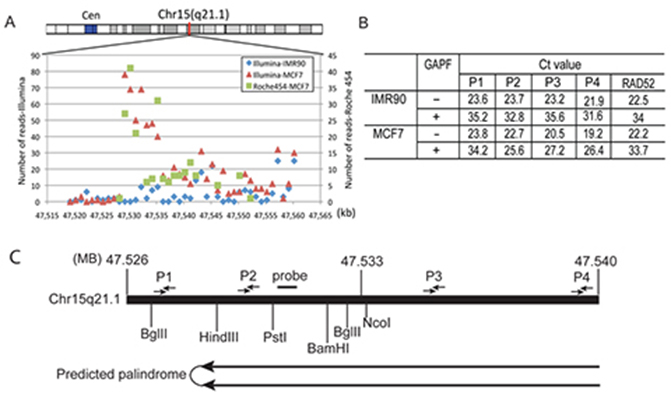
Palindrom kortlægningsstrategi. (A) Fordeling af læsetætheden i Chr15q21.1: 47.529.204-47.550.373-regionen vist som 1-kb-bins. (B) qPCR-analyse til overvågning af palindromberigelse og bestemmelse af Chr15q21.1-palindromets retningsbestemthed. Forskerne beregnede omfanget af udtynding af en specifik TaqMan-primersætregion baseret på Ct-værdien før og efter GAPF-protokollen i både IMR-90- og MCF-7-prøver. Foldberigelsen er baseret på sammenligning af folddepletion blandt forskellige primersæt (P1, P2, P3 og P4) i forhold til en enkeltkopi-sekvens i genomet (RAD52). Placeringen af TaqMan-præmersættene P1, P2, P3 og P4 er angivet i (C), kort over genomisk område Chr15: 47,520,000-47,550,000 med restriktionssteder og primerplaceringer. Figur fra Yang et al., GAP-Seq: a method for identification of DNA palindromes, BMC Genomics 2014, 15:394; doi:10.1186/1471-2164-15-394.
