Geneerinen nimi: indosyaniinivihreä
Asennusmuoto: injektio, jauhe, lyofilisoitu, liuosta varten
Lääketieteellisesti tarkistettu Drugs.com. Viimeksi päivitetty 1. lokakuuta 2020.
- Haittavaikutukset
- Dosointi
- Valmisteet
- Vuorovaikutukset
- Raskaus
- Lisätiedot
Itsevihreän lääkkeen käyttöaiheet ja käyttöaiheet
Itsevihreän lääkkeen käyttöaiheet:
Sydäntehon, maksan toiminnan ja maksan verenkierron määrittämiseen
IC-Greenin annostus ja antotapa
Väriaineen laimennustutkimukset
Väriaineen laimennuskäyrien tekemisessä tiedossa oleva määrä väriainetta ruiskutetaan yksittäisenä boluksena mahdollisimman nopeasti sydänkatetrin kautta valittuihin kohtiin verenkiertoelimistössä. Rekisteröintilaite (oksimetri tai densitometri) kiinnitetään neulaan tai katetriin väriaine-veriseoksen näytteenottoa varten systeemisestä valtimon näytteenottokohdasta.
Steriileissä olosuhteissa IC-Green® -jauhe on liuotettava tätä tuotetta varten varattuun steriiliin injektionesteisiin käytettävään veteen (Sterile Water for Injection, USP) ja liuos on käytettävä kuuden tunnin kuluessa sen valmistamisesta. Jos saostumaa esiintyy, liuos on hävitettävä.
Yleiset IC-Green®-annokset laimennuskäyriä varten ovat seuraavat:
Aikuiset – 5,0 mg
Lapset – 2,5 mg
Vauvaikäiset – 1,25 mg
Nämä väriaineannokset ruiskutetaan tavallisesti 1 ml:n tilavuuteen. Diagnostisen sydänkatetroinnin suorittamisessa suositellaan keskimäärin viittä laimennuskäyrää. Injektoidun väriaineen kokonaisannos on pidettävä alle 2 mg/kg.
Vaikka ruiskun huuhteluun voidaan käyttää steriiliä injektionesteisiin käytettävää vettä, isotonista keittosuolaliuosta on käytettävä huuhtelemaan väriainejäämät sydänkatetrista verenkiertoon hemolyysin välttämiseksi. Väriaineen injektioruiskun huuhtelua lukuun ottamatta kaikissa muissa katetrointitoimenpiteen osissa tulisi käyttää suolaliuosta.
Kalibrointiväriainekäyrien kalibrointi: Laimennuskäyrien kvantifioimiseksi IC-Green® -väriaineen standardilaimennokset kokoveressä tehdään seuraavasti. On erittäin suositeltavaa, että näiden standardilaimennosten valmistuksessa käytetään samaa väriainetta, jota käytettiin injektioissa. Väkevin väriaineliuos valmistetaan laimentamalla tarkasti 1 ml 5 mg/ml väriainetta 7 ml:lla tislattua vettä. Tämä konsentraatio puolitetaan sitten peräkkäin laimentamalla 4 ml edellistä konsentraatiota 4 ml:lla tislattua vettä.
Jos laimennuskäyrissä käytettiin 2,5 mg/ml:n konsentraatiota, 1 ml 2,5 mg/ml:n väriainetta lisätään 1 ml:aan 3 ml:aa tislattua vettä, jotta saadaan kaikkein väkevin ”standardiliuos”. Tämä konsentraatio puolitetaan sitten peräkkäin laimentamalla 2 ml edellistä konsentraatiota 2 ml:lla tislattua vettä.
Sitten 0,2 ml:n annokset (kalibroidusta ruiskusta tarkasti mitattuna) näistä väriaineliuoksista lisätään 5 ml:n liuosnäytteisiin tutkittavan verestä, jolloin saadaan väriaineen lopulliset konsentraatiot veressä, jotka alkavat arviolta arviolta arvosta 24,0 mg/litraa (todellinen konsentraatio riippuu tarkasta lisätyn väriaineen määrästä). Tämä pitoisuus puolitetaan luonnollisesti peräkkäin seuraavissa koehenkilön verinäytteissä. Nämä tunnettuja määriä väriainetta sisältävät verinäytteet sekä nollanäyte, johon on lisätty 0,2 ml suolaliuosta, joka ei sisällä väriainetta, ohjataan detektorilaitteen läpi ja kirjatuista poikkeamista muodostetaan kalibrointikäyrä.
Maksafunktiotutkimukset
Johtuen sen absorptiospektristä IC-Green®:n (injektionesteisiin käytettävän indosyaniini-vihreän) vaihtelevia konsentraatioita veressä voidaan tarkkailla korvan densitometrialla tai ottamalla verinäytteitä ajoitetuin väliajoin. Molempien menetelmien tekniikka on seuraava.
Potilas on tutkittava paastossa, perustilassa. Potilas on punnittava ja annos on laskettava 0,5 mg/kg ruumiinpainon perusteella.
Steriileissä olosuhteissa IC-Green®-jauhe on liuotettava mukana toimitettuun Sterile Water for Injection, USP:hen. 25 mg:n injektiopulloon on lisättävä tarkalleen 5 ml Sterile Water for Injection, USP:tä, jolloin saadaan 5 mg väriainetta millilitraa liuosta kohti.
Pistetään laskettu määrä väriainetta (0,5 mg/kg ruumiinpainoa) käsivarren laskimon luumeniin mahdollisimman nopeasti ilman, että väriaine pääsee karkaamaan laskimon ulkopuolelle. (Jos käytetään fotometristä menetelmää, ennen IC-Green®:n ruiskuttamista otetaan potilaan käsivarresta 6 ml laskimoverta seerumin nollakokeen ja standardikäyrän muodostamista varten ja ruiskutetaan saman neulan kautta oikea määrä väriainetta.)
Korvan tiheysmittaus: Korvaoksimetriaa on myös käytetty, ja sen avulla voidaan seurata IC-Green®:n ilmaantumista ja häviämistä ilman, että kalibrointiin tarvitaan verinäytteiden ottoa ja spektrofotometristä analyysia. Olisi käytettävä korvan tiheysmittaria, jossa on kompensoiva valosähköinen kenno, joka korjaa veren tilavuuden ja hematokriitin muutokset, ja havaitsemisvalokenno, joka rekisteröi tasot. Tällä laitteella voidaan mitata samanaikaisesti sydämen ulostuloa, veren tilavuutta ja IC-Green®*:n maksapuhdistumaa. Tätä tekniikkaa on käytetty vastasyntyneillä, terveillä aikuisilla sekä maksasairauksia sairastavilla lapsilla ja aikuisilla. Normaalin koehenkilön poistumisnopeus on 18-24 % minuutissa. Koska maksan ulkopuolista poistumista ei tapahdu, IC-Green®:n todettiin soveltuvan vakavien kroonisten maksasairauksien sarjatutkimukseen ja vakaan maksan verenkierron mittaamiseen. Suurempina annoksina IC-Green® -valmistetta voidaan käyttää lääkkeiden aiheuttamien maksan toiminnan muutosten havaitsemiseen ja lievien maksavaurioiden havaitsemiseen.
Korvapainemittarin avulla 0,5 mg/kg:n annos normaaleilla koehenkilöillä antaa seuraavan puhdistumismallin.
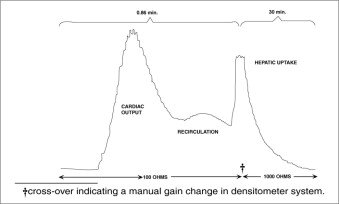
*The Waters Company, Rochester, Minnesota, toimittama dikromaattinen korvakappaleen densitometri.
Fotometrinen menetelmä –
Määritys väriaineen prosentuaalisen retentioasteen avulla:
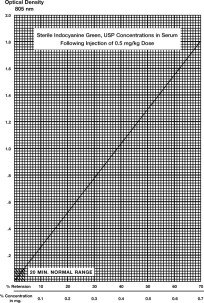
Tyypillinen käyrä, joka on saatu piirtämällä väriainekonsentraatio optisen tiheyden funktiona. Prosentuaalinen retentio voidaan lukea tästä kuvaajasta. Jos halutaan tarkempia tuloksia, käyrä, jossa käytetään potilaan verta ja määrityksessä käytettävää IC-Green®-pulloa, voidaan muodostaa seuraavasti:
- Otetaan 6 ml väriainetta sisältämätöntä laskimoverta potilaan käsivarresta. Laita koeputkeen ja anna veren hyytyä. Seerumi on erotettava sentrifugoimalla.
- Pipetoi 1 ml seerumia mikrokyvettiin.
- Lisää seerumiin 1 lambda (λ) 5 mg/ml IC-Green® (steriili indosyaniinivihreä)-vesiliuosta (steriili indosyaniinivihreä), jolloin laimennokseksi saadaan 5 mg/litra, joka on 50 %:n retentioasteen standardi. (Lisäämällä 2 lambda (λ) 5 mg/ml IC-Green® -liuosta saadaan 100 %:n retentio; tätä pitoisuutta ei kuitenkaan voida lukea spektrofotometrillä.)
- Tämän liuoksen optinen tiheys luetaan 805 nm:ssä käyttäen nollakokeena normaalia seerumia.
- Käyttämällä samanlaista kuvaajapaperia kuin kuvassa on käytetty, piirretään vaiheessa 4 saatu 50 %:n luku ja piirretään viiva, joka yhdistää tämän pisteen nollakoordinaatteihin.
Prosenttinen retentio: Yksittäinen 20 minuutin näyte (joka otetaan vastakkaisen käsivarren laskimosta kuin ruiskutettu näyte) kerätään ja annetaan hyytyä, sentrifugoidaan ja sen optinen tiheys määritetään 805 nm:ssä käyttäen potilaan normaalia seerumia nollanäytteenä. Väriainekonsentraatio voidaan lukea yllä olevasta käyrästä. Yhden 20 minuutin seeruminäytteen tulisi terveillä henkilöillä sisältää enintään 4 % väriaineen alkuperäisestä pitoisuudesta. Prosentuaalisen retentioasteen käyttö on epätarkempaa kuin prosentuaalisen häviämisasteen käyttö. Hemolyysin ei odoteta häiritsevän lukemaa.
Määritys väriaineen katoamisnopeuden avulla: Prosentuaalisen katoamisnopeuden laskemiseksi otetaan näytteet 5, 10, 15 ja 20 minuutin kuluttua väriaineen ruiskuttamisesta. Valmistele näyte edellisen kohdan mukaisesti ja mittaa optiset tiheydet 805 nm:ssä käyttäen potilaan normaalia seerumia nollanäytteenä. IC-Green® -pitoisuus kussakin ajoitetussa näytteessä on määritettävä kuvassa esitetyn pitoisuuskäyrän avulla. Arvot on piirrettävä semilogaritmiselle paperille.
IC-Green®:ää sisältävät näytteet on luettava samassa lämpötilassa, koska sen optiseen tiheyteen vaikuttavat lämpötilan vaihtelut.
Normaaliarvot: Prosentuaalinen katoamisnopeus terveillä koehenkilöillä on 18-24 % minuutissa. Normaali biologinen puoliintumisaika on 2,5-3,0 minuuttia.
Silmän angiografiatutkimukset
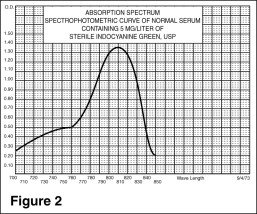
IC-Green®:n heräte- ja emissiospektri (kuva 1) ja absorptiospektri (kuva 2) tekevät siitä käyttökelpoisen silmän angiografiassa.
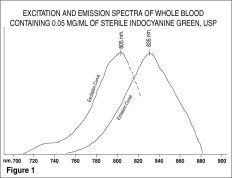
Käytettävistä kuvantamislaitteista ja -tekniikasta riippuen on käytettävä jopa 40 mg IC-Green® -väriainetta 2 ml:ssa Steriiliä injektionesteisiin käytettävää vettä, USP. Antecubitaalilaskimoon voidaan pistää IC-Green® -väriaineen bolus, ja välittömästi sen jälkeen on annettava 5 ml:n bolus normaalia suolaliuosta.
ANNOSMUODOT JA VAHVUUDET
IC-Green® on steriili, lyofilisoitu vihreä jauhe, joka sisältää 25 mg indosyaniinivihreää, jonka mukana on enintään 5 %:n natriumjodidi.
Vasta-aiheet
IC-Green® sisältää natriumjodidia, ja sitä on käytettävä varoen potilailla, joilla on aiemmin esiintynyt jodidiallergiaa anafylaksiariskin vuoksi.
Varoitukset ja varotoimet
Anaphylaxia
Anafylaksiasta johtuvia kuolemantapauksia on raportoitu IC-Green® -valmisteen antamisen jälkeen sydämen katetroinnin yhteydessä.
Lääkkeen epävakaus
IC-Green® -valmiste on epästabiili vesiliuoksessa, ja se on käytettävä 6 tunnin kuluessa. Väriaine on kuitenkin stabiili plasmassa ja kokoveressä, joten epäjatkuvalla näytteenottotekniikalla saadut näytteet voidaan lukea tunteja myöhemmin. Sekä väriaineliuoksen käsittelyssä että laimennuskäyrien tekemisessä on käytettävä steriilejä tekniikoita. Jos saostumaa esiintyy, liuos on hävitettävä.
Lääkkeiden ja laboratoriotestien yhteisvaikutukset
Radioaktiivisen jodin imeytymistutkimuksia ei saa tehdä vähintään viikkoon IC-Green® -valmisteen käytön jälkeen.
Haittavaikutukset
Potilailla, joilla on tai ei ole aiemmin ollut allergiaa jodideille, on raportoitu napafylaktisia tai nokkosihottumareaktioita. Jos tällaisia reaktioita esiintyy, hoida asianmukaisilla aineilla, esim, adrenaliinilla, antihistamiineilla ja kortikosteroideilla.
Lääkeinteraktiot
Natriumbisulfiittia sisältävät valmisteet, mukaan lukien jotkin hepariinivalmisteet, pienentävät IC-Green®:n imeytymishuippua veressä, eikä niitä siksi pidä käyttää antikoagulanttina näytteiden ottamisessa analyysiä varten.
KÄYTTÖ ERITYISRYHMISSÄ
Raskaus
Eläinten lisääntymistutkimuksia ei ole tehty IC-Green®:llä. Ei myöskään tiedetä, voiko IC-Green® aiheuttaa sikiövaurioita, kun sitä annetaan raskaana olevalle naiselle, tai voiko se vaikuttaa lisääntymiskykyyn. IC-Green® -valmistetta tulee antaa raskaana olevalle naiselle vain, jos se on selvästi indikoitu.
Imettävät äidit
Ei tiedetä, erittyykö tämä lääke ihmismaitoon. Koska monet lääkkeet erittyvät ihmismaitoon, on noudatettava varovaisuutta, kun IC-Green®-valmistetta annetaan imettävälle naiselle.
Pediatrinen käyttö
Turvallisuus ja teho lapsipotilailla on osoitettu. Katso erityiset annostelutiedot lapsipotilaille kohdasta ANNOSTUS JA ANNOSTUS (2).
Geriatrinen käyttö
Iäkkäiden ja nuorempien potilaiden välillä ei ole havaittu yleisiä eroja turvallisuudessa tai tehossa.
Yliannostus
Yliannostukseen liittyviä merkkejä, oireita tai laboratoriolöydöksiä kuvaavia tietoja ei ole saatavilla. LD50 laskimonsisäisen annostelun jälkeen vaihtelee hiirillä 60 ja 80 mg/kg, rotilla 50 ja 70 mg/kg ja kaneilla 50 ja 80 mg/kg välillä. Kehon pinta-alaan perustuen nämä annokset ovat 2,4-13-kertaiset ihmiselle suositeltuun enimmäisannokseen (MRHD) 2 mg/kg verrattuna indikaattorilaimennustutkimuksissa, 10-52-kertaiset MRHD-arvoon 0,5 mg/kg verrattuna maksan toimintaa koskevissa tutkimuksissa ja 7-39-kertaiset MRHD-arvoon 0,5 mg/kg verrattuna.67 mg/kg silmän angiografiatutkimuksissa.
IC-Green Kuvaus
IC-Green® on steriili, lyofilisoitu vihreä jauhe, joka sisältää 25 mg indosyaniinivihreää, jossa on enintään 5 % natriumjodidia. Se on pakattu injektionesteisiin käytettävän steriilin injektionesteisiin tarkoitetun veden, USP, kanssa, jota käytetään indosyaniinivihreän liuottamiseen. IC-Green® on tarkoitettu annettavaksi laskimoon.
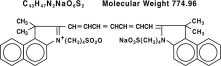
Indosyaniinivihreä on vesiliukoinen trikarbosyaniiniväriaine, jonka spektriabsorptiohuippu on 800 nm:ssä. Indosyaniinivihreän kemiallinen nimi on 1 H-Benzindolium, 2-indoli-2-ylideeni]-1,3,5-heptatrienyyli]-1,1-dimetyyli-3-(4-sulfobutyyli)-,hydroksidi, sisäsuola, natriumsuola. IC-Green®:n pH on noin 6,5, kun se on rekonstruoitu. Jokainen IC-Green®-injektiopullo sisältää 25 mg indosyaniinivihreää steriilinä lyofilisoituna jauheena.
IC-Green – Kliininen farmakologia
IC-Green® mahdollistaa indikaattorin laimennuskäyrien tallentamisen sekä diagnostiikka- että tutkimustarkoituksiin happisaturaation vaihteluista riippumatta. Laskimonsisäisen injektion jälkeen IC-Green® sitoutuu nopeasti plasman proteiiniin, jonka pääasiallinen kantaja on albumiini (95 %). IC-Green® ei kulje merkittävästi ekstrahepaattisessa tai enterohepaattisessa verenkierrossa; samanaikaiset valtimo- ja laskimoveriarviot ovat osoittaneet, että väriaineen imeytyminen munuaisiin, perifeerisiin verisuoniin, keuhkoihin tai aivo-selkäydinkanavaan on vähäistä. IC-Green® imeytyy plasmasta lähes yksinomaan maksan parenkyymisoluihin ja erittyy kokonaan sappeen. Sappitietukoksen jälkeen väriaine näkyy maksan imusolmukkeessa sapesta riippumatta, mikä viittaa siihen, että sappiteiden limakalvo on riittävän ehjä estämään väriaineen diffuusion, mutta sallimaan bilirubiinin diffuusion. Nämä ominaisuudet tekevät IC-Green® -väriaineesta hyödyllisen maksan toiminnan indeksin.
IC-Green® -väriaineen absorptiohuippu ja emissiohuippu sijaitsevat alueella (800-850 nm), jossa pigmenttiepiteelin energian läpäisy on tehokkaampaa kuin näkyvän valoenergian alueella. IC-Green®:llä on myös se ominaisuus, että se on lähes 98-prosenttisesti sitoutunut veren proteiineihin, minkä vuoksi liiallista väriaineen ekstravasaatiota ei tapahdu voimakkaasti fenestroituneessa suonikalvon verisuonistossa. Siksi se on käyttökelpoinen sekä absorptio- että fluoresenssi-infrapuna-angiografiassa suonikalvon verisuonistossa, kun käytetään sopivia suodattimia ja filmiä silmänpohjakamerassa.
Plasman fraktionaalisen katoamisnopeuden suositellulla 0,5 mg/kg annoksella on raportoitu olevan naisilla merkitsevästi suurempi kuin miehillä, vaikka puhdistuman laskennallisessa arvossa ei ollut merkittävää eroa.
Nonkliininen toksikologia
Karsinogeenisuus, mutageenisuus, hedelmällisyyden heikentyminen
Tutkimuksia karsinogeenisuuden, mutageenisuuden tai hedelmällisyyden heikentymisen arvioimiseksi ei ole tehty.
Valmistustapa/varastointi ja käsittely
IC-Green® toimitetaan pakkauksessa (NDC 17478-701-02), joka sisältää kuusi 25 mg:n IC-Green®-injektiopulloa ja kuusi 10 ml:n steriiliä injektionesteisiin käytettävää injektionesteisiin käytettävää vettä (Sterile Water for Injection, USP) sisältävää ampullia:
NDC 17478-701-25 IC-Green®-injektiopullo. 25 mg:n täyte 20 ml:n injektiopullossa.
NDC 17478-701-10 Sterile Water for Injection, USP -ampulli. 10 ml:n täyttö 10 ml:n ampullissa.
VARASTOINTI: Säilytä 20°-25°C:ssa (68°-77°F).
AKORN
Valmistaja: Akorn, Inc.
Lake Forest, IL 60045
IG00N rev. 06/16
Pakkausetiketin pääasiallinen näyttöteksti:
NDC 17478-701-25
IC-Green®
(indosyaniinivihreä
injektioon, USP)
25 mg Sterile Rx only

Kartongin pääasiallinen näyttöteksti:
Akorn-logo NDC 17478-701-02
IC-Green®
(indosyaniinivihreä
injektionesteisiin, USP)
25 mg:n pakkaus
vain steriili Rx

Principal-näyttöpaneelissa teksti pakkauksen etikettiin:
NDC 17478-701-10
Steriili vesi
injektionesteisiin, USP
IC-Green®:lle (indosyaniini
vihreä injektionesteisiin, USP)
10 ml steriiliä Rx-pakkausta varten

Perusnäyttöpaneelin teksti pakkauksen etikettiin:
NDC 17478-701-10
Akornin logo
Steriili injektionesteisiin käytettävä vesi
, USP
IC-Green®
(indosyaniinivihreä
injektioon, USP)
Steriili
6 ampullia
(10 ml kukin) Rx only

| IC-17478-701 |
| Pakkaus | |||
| # | Erätekoodi | Pakkauskuvaus | |
| 1 | NDC:17478-701-02 | 1 KIT in 1 CARTON | |
| Osamäärä | ||||
| Tuotenumero | Pakkausmäärä | Tuotteen kokonaismäärä | ||
| Tuotenumero 1 | 6 VIAL, SINGLE-DOSE | 6 | ||
| Part 2 | 6 AMPULI | 60 ml | ||
Part 1 of 2
IC-Vihreä
indosyaniinin vihreä injektio, jauhe, lyofilisoitu, liuosta varten
| Tuotetiedot | |||
| Käyttötapa | INTRAVENOUS | DEA Schedule | |
| Vaikuttava aine/vaikuttava osa | |||
| Ainesosan nimi | Vahvuuden perusta | Vahvuus | Vahvuus |
| indosyaniinivihreää (indosyaniinivihreä hapon muoto) | indosyaniinivihreä | 25 mg | |
| Vaikuttavat ainesosat | |
| Ainesosan nimi | Vahvuus |
| Vesi | . |
| Pakkaus | |||
| # | Koodi | Pakkauksen kuvaus | |
| 1 | 1 INJECTION, JAUHE, LYOPHILOITU, LIUOTTAMISEEN 1 VIILOSSA, SINGLE-ANNOS | ||
| Myyntitiedot | ||||
| Myyntikategoria | Hakemusnumero tai monografian viittaus | Myynnin aloitus Päiväys | Markkinoinnin päättymispäivä | |
| NDA | NDA011525 | 09/01/2007 | ||
Part 2 of 2
AQUEOUS SOLVENT
water injektio
| Tuotetiedot | |||
| Annostustapa | INTRAVENOOSI | DEA-luettelo | |
| VAIKUTTAVAT AINEET | |
| Ainesosan nimi | Vahvuus |
| Vesi | |
| Pakkaus | |||
| # | Tuotekoodi | Pakkauksen kuvaus | |
| 1 | 10 ml 1 AMPULE | ||
| Markkinointitiedot | |||
| Markkinointiluokka | Hakemusnumero tai monografian viittaus | Markkinoinnin alkamispäivämäärä | Markkinoinnin päättymispäivämäärä |
| NDA | NDA011525 | 09/01/2007 | |
| Markkinointiin liittyvät tiedot | |||
| Markkinointikategoria | Markkinointiin liittyvät tiedot | ||
| Markkinointiin liittyvät tiedot tai Monografian viittaus | Markkinoinnin alkamispäivä | Markkinoinnin päättymispäivä | |
| NDA | NDA011525 | 09/01/2007 | |
Labeler – Akorn, Inc. (117696770)
Rekisteröijä – Akorn, Inc. Akorn Operating Company LLC (117693100)
| Toimipaikka | |||
| Nimi | Asoite | ID/FEI | Toimipaikka |
| Akorn, Inc. | 117696790 | LABEL(17478-701), PACK(17478-701) | |
| Toimipaikka | |||
| Nimi | Asoite | ID/FEI | Toiminta |
| Akorn, Inc. | 117696832 | VALMISTUS(17478-701), ANALYYSI(17478-701), STERILOINTI(17478-701) | |
