



VEGF-vasta-ainetta sisältävällä hoidolla neovaskulaarista ikääntymiseen liittyvää makuladegeneraatiota sairastavilla potilailla on tyypillisesti tapahtunut huomattavia parannuksia näöntarkkuuteen ja elämänlaatuun. Vaikka lyhyen aikavälin tulokset ovat suorastaan huikeita, näiden potilaiden pitkän aikavälin hoitoon liittyy edelleen useita tärkeitä kysymyksiä. Niitä ovat mm:
- Mikä on paras aine?
- Miten usein pitäisi hoitaa?
- Aiheuttaako näiden aineiden pitkäaikainen annostelu näön heikkenemistä ja vaurioita?
- Onko näköpiirissä uusia alustoja näiden aineiden pitkäaikaiseen annosteluun?
- Tässä artikkelissa vastataan näihin kysymyksiin keskeisten kliinisten tutkimusten tulosten perusteella.
Ovatko kaikki anti-VEGF-aineet samanarvoisia? Kuinka usein pitäisi hoitaa?
Vuonna 2006 maamerkkitutkimukset ANCHOR ja MARINA osoittivat kuukausittain annosteltavan ranibitsumabin (Lucentis, Roche/Genentech) tehon ja turvallisuuden. Potilaat paranivat 10,7 ja 6,6 kirjainta kahdessa vuodessa.1-2 Myöhemmin rinnakkaiset VIEW1- ja VIEW2-tutkimukset osoittivat näön keskimääräisen paranemisen kahdessa vuodessa aflibertseptillä (Eylea, Regeneron Pharmaceuticals), jota annosteltiin kahdeksan viikon välein kolmen alkuperäisen kuukausittaisen latausannoksen jälkeen.3
Seuraavissa tutkimuksissa saatiin arvioitua näiden lääkeaineiden teho harvemmalla annosteluväliajalla, mukaan luettuina neljännesvuosittaiset, pro re nata (PRN) -annosteluväliä koskevat annosteluväliä koskevat annosteluväliä koskevat annosteluväliä koskevat annosteluväliajat sekä hoito- ja pidennysohjelmat. PIER-tutkimuksessa tutkittiin ranibitsumabin neljännesvuosittaista annostelua kolmen kuukausittaisen latausannoksen jälkeen, ja vaikka PIER-potilaat olivat tarkkailua parempia, he menettivät yhden vuoden kuluttua 2,3 kirjainta lähtötasosta.4
Yksi varhaisimmista poikkeuksista oli PrONTO, vaiheen I/II tutkimus, jossa arvioitiin 40 potilasta kahden vuoden ajan kuukausittaisella seurannalla ja PRN-uudelleenhoitohoidolla, joka perustui näöntarkkuuteen, kliiniseen tutkimukseen ja optiseen koherenssitomografiaan perustuviin parametreihin.5 Näöntarkkuustulokset lähentelivät ANCHOR- ja MARINA-tutkimusten tuloksia melkein puolet pienemmällä injektiomäärällä kuin tutkimusten ANCHOR- ja MARINA-tutkimukset, mutta tutkimuksesta puuttui kuukausittaisen hoidon kontrolliryhmä. Näitä tuloksia ei ole toistettu myöhemmissä PRN-tutkimuksissa.
HARBOR-tutkimuksessa verrattiin ranibitsumabin kuukausittaista ja PRN-annostelua. Kuukausittainen 0,5 mg:n ryhmä sai 9,1 kirjainta 24 kuukaudessa verrattuna 7,9 kirjaimeen PRN-ryhmässä. Vaikka tämä ero ei ollut tilastollisesti merkitsevä, injektioiden mediaanimäärä (mutta ei käyntien määrä) väheni 21,4:stä 13,3:een.6
CATT ja IVAN olivat samankaltaisia tutkimuksia, joissa verrattiin ranibitsumabin kuukausittaista ja PRN-annostelua ja off-label-valmisteista bevasitsumabia (Avastin, Roche/Genentech). Kahden vuoden kuluttua PRN-annostelun ei todettu olevan huonompi kuin kuukausittaisen hoidon molemmissa tutkimuksissa (lukuun ottamatta PRN-kevytbevasitsumabia CATT-tutkimuksessa), vaikka kuukausittain annostelluissa ryhmissä oli havaittavissa suuntaus parempaan näkökykyyn7,8.
TREX-tutkimuksessa verrattiin kuukausittain annosteltavaa ranibitsumabia hoitoon ja jatkamiseen (T&E) perustuvaan hoitoon.9 Jälleen kerran näöntarkkuuden ero ei ollut tilastollisesti merkitsevä (10,5 kuukausiryhmässä ja 8,7 T&E-ryhmässä), mutta suuntaus oli parempaan näköön kuukausiryhmässä. Keskimääräinen pistosten määrä oli 25,5 verrattuna 18,6 pistokseen kahden vuoden aikana. Yksikään kuukausittaisen kohortin potilaista ei myöskään menettänyt yli kahta kirjainta, kun taas viisi T&E-potilasta menetti vähintään kolme näköviivaa.
Vaikka nämä tutkimukset ovat osoittaneet tilastollisesti samankaltaisia tuloksia kuukausittaisella annostelulla lyhyellä aikavälillä, absoluuttisten tietojen tulokset ovat olleet lähes yksimielisesti parempia anti-VEGF-lääkkeiden kuukausittaisella annostelulla.
Mitä tapahtuu kahden vuoden kuluttua?
Kahden vuoden jälkeisiä tietoja näistä kliinisistä tutkimuksista ei ole yhtä helppo tulkita ja soveltaa kuin kliinisten tutkimusten tietoja, pääasiassa siksi, että näissä jatkotutkimuksissa arvioitiin pääasiassa lääkkeiden pitkäaikaista turvallisuutta. Seuranta- ja hoitosuunnitelmat eivät siis olleet yhtä tiukkoja.

HORIZON oli MARINA-, ANCHOR- ja FOCUS-tutkimusten potilaiden jatkotutkimus. Nämä potilaat eivät noudattaneet protokollaa; he saivat hoitoa tutkijoiden harkinnan mukaan arviointikäyntien aikana kolmen tai kuuden kuukauden välein. Neljän vuoden kuluttua HORIZON-potilaat menettivät olennaisesti alkuvaiheen näköhavainnon paranemisen ja taantuivat lähtötason näön tasolle (-0,1 kirjainta).10 Tietojen jatkoanalyysissä havaittiin yhteys paremman näön ja useampien injektioiden välillä.
Viisivuotisessa CATT-tutkimuksessa arvioitiin potilaita, joita seurattiin ja hoidettiin tutkijoiden harkinnan mukaan tutkimuksen kahden ensimmäisen vuoden jälkeen. Potilaat menettivät keskimäärin 3 kirjainta verrattuna lähtötilanteen näkökykyyn. Potilaita katsottiin keskimäärin kahdeksan kertaa vuodessa, ja he saivat keskimäärin viisi hoitoa vuodessa.11 Joitakin keskusteluja käytiin siitä, johtuiko näön heikkeneminen alihoidosta vai makulan atrofian kehittymisestä, mutta tutkimuksen teho ei riittänyt tämän eron selvittämiseen.12
VIEW 1 -laajennustutkimuksessa potilaita seurattiin tarkemmin. Osallistujat saivat kiinteän >q8-viikkoisen annostelun, mutta he saattoivat saada tiheämpiä hoitoja, jos he täyttivät ennalta määritellyt kriteerit. SEVEN-UP-tutkimus oli ranibitsumabitutkimusten jatkotutkimus. Vaikka tutkimuksessa ei ollut ennalta määriteltyä käyntiaikataulua tai injektioprotokollaa, tiedot antavat jonkin verran tietoa. Seitsemän vuoden kuluttua potilaat menettivät keskimäärin 8,6 kirjainta lähtötilanteesta. Potilaat, jotka eivät saaneet yhtään injektiota seuraavien kolmen vuoden aikana, menettivät 8,7 kirjainta lähtötilanteesta; potilaat, jotka saivat yhdestä viiteen injektiota, menettivät 10,8 kirjainta; potilaat, jotka saivat kuudesta kymmeneen injektiota, menettivät 6,9 kirjainta; ja potilaat, jotka saivat yli 11 injektiota, menettivät 3,9 kirjainta lähtötilanteesta.14
Australialaisessa Fight Retinal Blindness Study Group -tutkimusryhmässä (Fight Retinal Blindness Study Group) tarkkailtiin potilaita, joita oli hoidettu antiepiteelillä (anti-VEGF:llä), seitsemänä vuonna. Nämä potilaat menettivät keskimäärin 2,6 kirjainta lähtötilanteesta, kun he olivat saaneet keskimäärin viisi injektiota vuodessa toisen vuoden jälkeen, jolloin he olivat saaneet 4 kirjainta lähtötilanteesta.15
Loppujen lopuksi FIDO-tutkimus oli yksikeskuksinen havainnointitutkimus, jossa käytettiin q4-viikkoisia kiinteitä annosteluja ensimmäisten kahden vuoden ajan ja >q8 viikkoa sen jälkeen. Nämä potilaat saivat lähtötilanteesta 12,1 kirjainta lisää (huippuarvo oli 16,1 kirjainta kahden vuoden kohdalla), kun pistoksia annettiin keskimäärin 10,5 vuodessa.16
Keskeinen viesti näissä pitkäaikaisissa havainnointitutkimuksissa on se, että keskimäärin useammat pistokset merkitsivät selvästi parempaa näkökykyä.

Meillä on nyt 10 vuoden tiedot
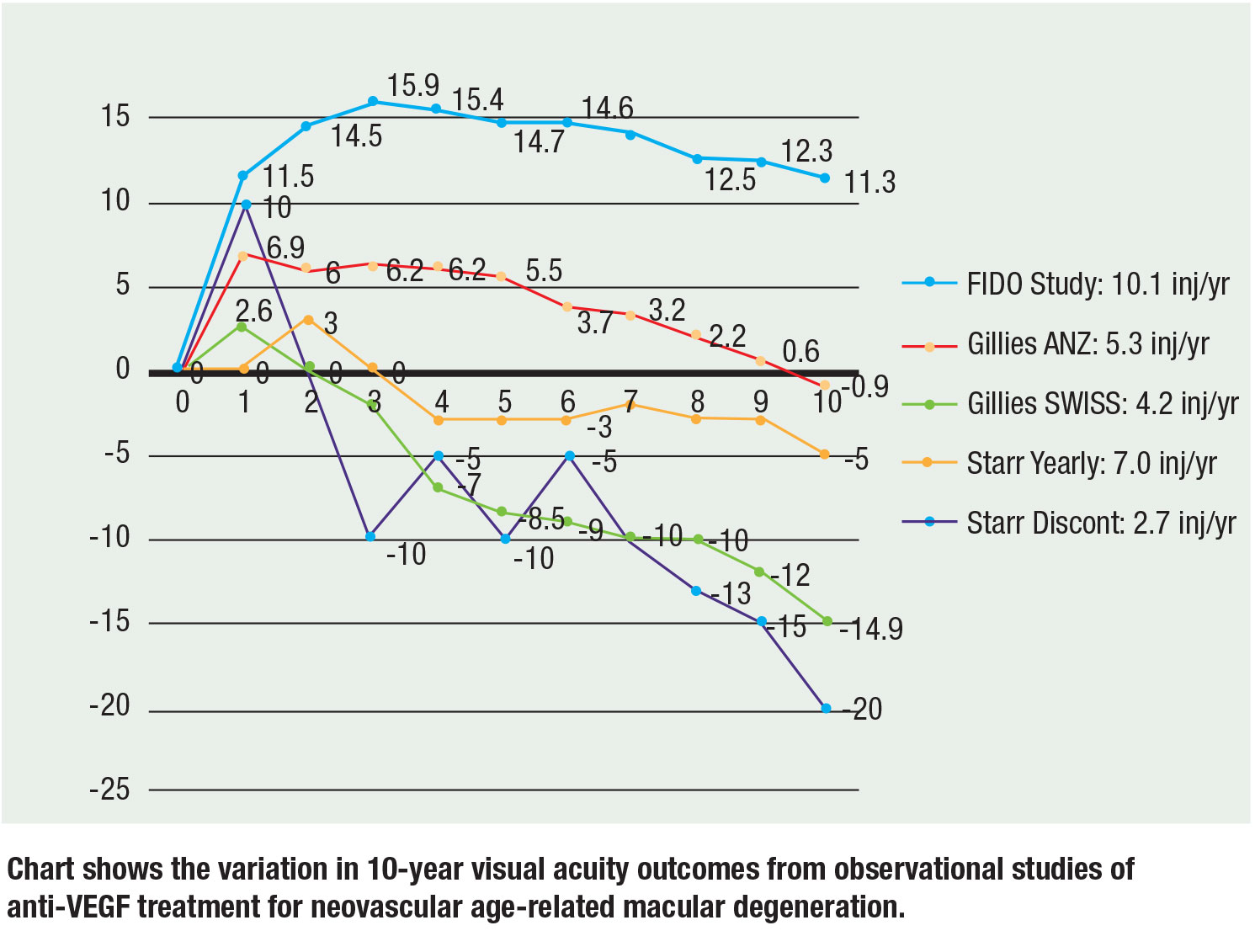
Viime aikoina kolmessa laajassa havainnointitutkimuksessa on raportoitu 10 vuoden tiedot, ja tulokset ovat edelleen johdonmukaisia: Useammat injektiot johtavat parempaan näöntarkkuuteen. Lääketieteen tohtori Mark Gillies ja kollegat raportoivat Australiasta, Uudesta-Seelannista ja Sveitsistä saadut havainnointitiedot. ANZ-potilaiden keskimääräinen näkökyky heikkeni 10 vuoden kuluttua 0,9 kirjainta lähtötilanteesta, kun T&E-valmisteella annettujen injektioiden mediaani oli 5,3 injektiota vuodessa, verrattuna sveitsiläispotilaisiin, joiden näkö heikkeni keskimäärin 14,9 kirjainta, kun PRN-valmisteella annettujen injektioiden mediaani oli 4,2 injektiota vuodessa. Heidän johtopäätöksensä oli, että jatkuvalla hoidolla ja useammalla injektiolla saavutettiin parempi näkö.17
Matthew Starr, MD, ja kollegat arvioivat kohorttia, johon kuului potilaita, jotka olivat saaneet vähintään kaksi injektiota. Keskimäärin potilaat saivat viidestä seitsemään injektiota vuodessa. Silmät, jotka saivat vähintään yhden injektion vuodessa, menettivät noin 7 kirjainta lähtötilanteesta, kun taas silmät, jotka eivät saaneet vähintään yhtä injektiota vuodessa, menettivät 15 kirjainta lähtötilanteesta.18
Meidän 10-vuotinen FIDO-kohorttimme saavutti keskimääräisen 11,3 kirjaimen näönlisäyksen huippulukemasta 15,9 kirjaimella, kun injektioita annettiin keskimäärin 10,1 vuodessa tutkimusjakson aikana.19 19
On tärkeää huomata, että ristikkäistutkimusten vertailuun liittyy luonnostaan riskejä, kun otetaan huomioon erilaiset alkuperäiset näöntarkkuudet ja potilaspopulaatiot, mutta kaltevuudet ja kehityssuunnat pitävät paikkansa korrelaatiossa, jonka mukaan useammat injektiot johtavat parempaan näkökykyyn. Kuviossa (sivu 29) on yhteenveto kolmen tutkimuksen 10 vuoden tiedoista.
Johtaako tiheä hoito geografisen atrofian etenemiseen?
Huoli geografisen atrofian etenemisestä anti-VEGF-hoidon yhteydessä on ollut huolenaihe, ja siihen on usein vedottu perusteluna sille, miksi hoitoa ei anneta usein. Jotkin todisteet viittaavat siihen, että alihoidosta aiheutuva näön heikkenemisen riski on paljon suurempi kuin tämä mahdollinen huolenaihe. SEVEN-UP-tutkimus osoitti, että GA:n esiintyvyys oli suurempi muissa silmissä kuin anti-VEGF:llä hoidetuissa silmissä14 .
Lisäksi FIDO:n 10-vuotistutkimus osoitti, että GA:n ja näön menetyksen esiintyvyys 10 vuoden kuluttua oli hieman pienempi hoidetuissa silmissä kuin hoitamattomissa muissa silmissä (15 prosenttia vs. 19 prosenttia).19 On todennäköistä, että todellisen GA:n eteneminen on riippumaton
anti-VEGF-hoidosta, ja se, mitä havaitaan, on neovaskulaarisen kompleksin kuivumista, joka näyttää GA:lta, mutta jolla on vähemmän haitallinen vaikutus näkökykyyn.
Bottom Line
Jatkuva, säännöllinen anti-VEGF-lääkehoito antaa erinomaisia tuloksia kostean AMD:n hoidossa. Pitkän aikavälin tiedot osoittavat, että näön heikkenemisen riski on suurempi alihoidosta kuin jatkuvasta, säännöllisin väliajoin tapahtuvasta hoidosta, jota nykyisin sovelletaan kiinteän väliajan annostelussa tai konservatiivisissa treat-and-extend-ohjelmissa. Pitkäkestoiset annostelumenetelmät, kuten porttiannostelujärjestelmä ja geeniterapia, vaikuttavat lupaavilta, sillä ne vähentävät hoitomyöntyvyyden puuttumisen esteitä, tiheistä käynneistä aiheutuvaa taakkaa ja vaihtelevista yksilöllisistä annosteluvaatimuksista aiheutuvia haasteita. RS
1. Brown DM, Kaiser PK, Michels M, et al. Ranibitsumabi versus verteporfiini neovaskulaarisen ikään liittyvän makuladegeneraation hoidossa. N Engl J Med. 2006;355:1432-1444.
2. Rosenfeld PJ, Brown DM, Heier JS, et al. MARINA Study Group, Ranibizumab for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1419-1431.
3. Schmidt-Erfurth U, Kaiser PK, Korobelnik JF, et al. Intravitreaalinen aflibersepti-injektio neovaskulaariseen ikään liittyvään makuladegeneraatioon: VIEW-tutkimusten 96 viikon tulokset. Ophthalmology. 2014;121:193-201.
4. Regillo CD, Brown DM, Abraham P, et al. Randomized, double-masked, sham-controlled trial of ranibizumab for neovascular age-related macular degeneration: PIER-tutkimuksen vuosi 1. Am J Ophthalmol. 2008;145:239-248.
5. Lalwani GA, Rosenfeld PJ, Fung AE, et al. A variable-dosing regimen with intravitreal ranibizumab for neovascular age-related macular degeneration: year 2 of the PrONTO Study. Am J Ophthalmol. 2009;148:43-58.
6. Ho AC, Busbee BG, Regillo CD, et al, for the HARBOR Study Group. 0,5 tai 2,0 mg ranibitsumabin 24 kuukauden teho ja turvallisuus potilailla, joilla on subfoveaalinen neovaskulaarinen ikään liittyvä makuladegeneraatio. Ophthalmology. 2014;121:2181-2192.
7. Martin DF, Maguire MG, Fine SL, et al, Comparison of Age-related Macular Degeneration Treatments Trials (CATT) Research Groupin puolesta. Ranibitsumabi ja bevasitsumabi neovaskulaarisen ikään liittyvän makuladegeneraation hoidossa: kahden vuoden tulokset. Ophthalmology. 2012;119:1388-1398.
8. Chakravarthy U, Harding SP, Rogers CA, et al. Alternative treatments to inhibit VEGF in age-related choroidal neovascularization: 2-year findings of the IVAN randomized control trial. Lancet. 2013;382:1258-1267.
9. Wykoff CC, Ou WC, Brown DM, et al. Randomized trial of treat-and-extend versus monthly dosing for neovascular age-related macular degeneration: 2-year results of the TREX-AMD study. Ophthalmol Retina. 2017;1:314-321.
10. Singer MA, Awh CC, Sadda S, et al. HORIZON: An open-label extension trial of ranibizumab for choroidal neovascularization secondary to age-related macular degeneration. Ophthalmology. 2012;119:1175-1183.
11. Maguire MG, Martin DF, Ying GS, et al. Five-year outcomes with anti-vascular endothelial growth factor treatment of neovascular age-related macular degeneration: The comparison of age-related macular degeneration treatments trials. Ophthalmology. 2016;123:1751-1761.
12. Grunwald JE, Pistilli M, Ying GS, et al. Growth of geographic atrophy in the comparison of age-related macular degeneration treatments trials. Ophthalmology. 2015;122:809-816.
13. Kaiser PK, Singer M, Tolentino M, et al. Intravitaalisen aflibertseptin pitkäaikainen turvallisuus ja näkötulokset neovaskulaarisessa ikään liittyvässä makuladegeneraatiossa. Ophthalmol Retina. 2017;1:304-313.
14. Rofagha S, Bhisitkul RB, Boyer DS, Sadda SR, Zhang K, SEVEN-UP-tutkimusryhmän puolesta. et al. Seitsemän vuoden hoitotulokset ranibitsumabilla hoidetuilla potilailla ANCHOR-, MARINA- ja HORIZON-tutkimusryhmissä: Monikeskuksinen kohorttitutkimus (SEVEN-UP). Ophthalmology. 2013;120:2292-2299.
15. Gillies MC, Campain A, Barthelmes D, et al, Fight Retinal Blindness Study Groupin puolesta. Neovaskulaarisen ikään liittyvän makuladegeneraation hoidon pitkäaikaistulokset: Data from an observational study. Ophthalmology. 2015;122:1837-1845.
16. Peden MC, Suñer IJ, Hammer ME, Grizzard WS. Pitkän aikavälin hoitotulokset silmissä, jotka saavat kiinteän intervallin välein annosteltuja verisuonten endoteelin kasvutekijää estäviä aineita märkään ikään liittyvään makuladegeneraatioon. Ophthalmology. 2015;122:803-808.
17. Gillies M, Arnold J, Bhandari S, et al. Neovaskulaarisen ikään liittyvän makuladegeneraation kymmenvuotistulokset kahdelta alueelta. Am J Ophthalmol. 2020;210:116-124.
18. Starr MR, Kung FF, Bui YT, et al. Kymmenen vuoden seuranta potilailla, joilla on eksudatiivinen ikään liittyvä makuladegeneraatio ja joita on hoidettu intravitreaalisilla anti-vaskulaarisen endoteelin kasvutekijän injektioilla. Retina. Julkaistu verkossa 13. marraskuuta 2019.
19. Suñer IJ, Peden MC, Hammer ME, Grizzard WS. Kymmenen vuoden hoitotulokset silmissä, jotka saivat kiinteän intervallin välein annosteltuja verisuonten endoteelin kasvutekijää estäviä aineita märkään ikään liittyvään makuladegeneraatioon. Paper presented at Retina Society 2019; September 12, 2019; London, U.K.
20. Campochiaro PA, Marcus DM, Awh CC, et al. Porttiannostelujärjestelmä ranibitsumabin kanssa neovaskulaarisen ikään liittyvän makuladegeneraation hoitoon: satunnaistetun vaiheen 2 LADDER-kliinisen tutkimuksen tulokset. Ophthalmology. 2019;126:1141-1154.
21. Ho AC; Janssen/ORBIT-tutkimusryhmä. Solu- ja geeniterapian täsmälähetysohjelmat. Paper presented at: Vail Vitrectomy Meeting; 10. helmikuuta 2019; Vail, CO.
22. ADVM-022 geeniterapia märkään AMD:hen (OPTIC). Sponsori: Adverum Biotechnologies. ClinicalTrials.gov-tunniste: NCT03748784. Saatavilla osoitteessa: https://clinicaltrials.gov/ct2/show/NCT03748784. Viitattu 18. huhtikuuta 2020.
23. RegenxBio raportoi vuoden 2019 ensimmäisen vuosineljänneksen taloudellisista ja operatiivisista tuloksista sekä positiivisesta välivaiheen I/IIa-tutkimuksen päivityksestä RGX-314:n osalta kostean AMD:n hoidossa. Rockville, MD; 7. toukokuuta 2019. https://www.prnewswire.com/news-releases/regenxbio-reports-first-quarter-2019-financial-and-operating-results-and-additional-positive-interim-phase-iiia-trial-update-for-rgx-314-for-the-treatment-of-wet-amd-300845423.html Luettu 9. heinäkuuta 2020.
