Le syndrome du délire excité est une présentation fréquente mais mal caractérisée aux urgences, avec un large diagnostic différentiel. Les patients sont souvent identifiés initialement par les forces de l’ordre, mais les tentatives de contrôle des personnes souffrant du SDE par des moyens de contention physiques, chimiques ou électriques sont associées à un taux de morbidité et de mortalité excessivement élevé.
Cas
Un homme de 25 ans se présente aux urgences amené par le SAMU pour un état mental altéré (EMA). Avant l’arrivée, les ambulanciers fournissent un rapport radio indiquant que le patient a été trouvé agité, se comportant de manière agressive, puis a grimpé sur le capot de l’ambulance. Il a été noté qu’il était extrêmement fort et difficile à maîtriser. Les ambulanciers lui ont administré 5 mg de midazolam par voie intramusculaire et ont réussi à le maîtriser physiquement, mais à l’arrivée, il reste extrêmement agité, hurle et se cogne contre les barres latérales du brancard. Il ne répond à aucune question et son discours est absurde. À l’examen, le patient est nettement tremblant, chaud au toucher, avec des secousses myocloniques et un bruxisme. Des abrasions superficielles étendues sont notées sur son abdomen, son thorax et ses extrémités. Il est trop agité pour obtenir les premiers signes vitaux. Quelles sont vos prochaines étapes ?
Contexte
Le syndrome de délire excité (SDE) est une présentation commune mais mal caractérisée aux urgences avec un large diagnostic différentiel. Décrit dans la littérature depuis plus de 100 ans,1 il est supposé impliquer un excès catécholaminergique impliquant des catécholamines endogènes liées au stress, des médicaments catécholaminergiques exogènes,2 et/ou une surstimulation des récepteurs de la dopamine et du glutamate NMDA dans le cadre d’une maladie psychiatrique ou médicale organique. Les causes peuvent être regroupées de manière générale en étiologies métaboliques/endocriniennes, neurologiques, infectieuses, toxicologiques et psychiatriques (tableau 1).
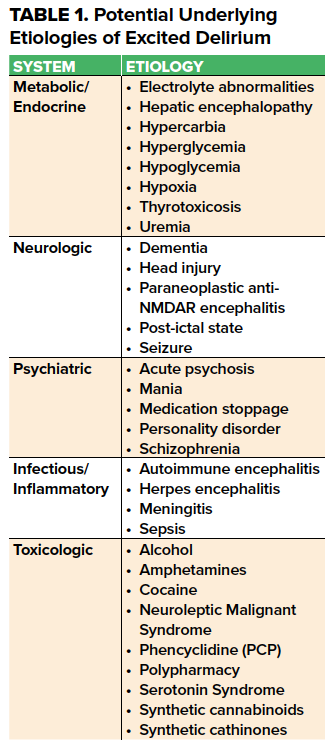
La présence concomitante d’une intoxication médicamenteuse aiguë, en particulier de sympathomimétiques, et d’antécédents de maladie mentale avec des caractéristiques psychotiques est la plus fréquente parmi celles-ci. L’incidence de l’ExDS est très variable, avec une augmentation de l’incidence dans les années 19803 liée à l’augmentation de la consommation de cocaïne4, d’amphétamines et de phencyclidine. Récemment, les cathinones synthétiques et les cannabinoïdes ont été mis en cause.5,6
Les patients sont souvent identifiés initialement par les forces de l’ordre. Les interventions des forces de l’ordre visant à contrôler les personnes souffrant de SDE par des moyens de contention physiques, chimiques ou électriques sont associées à un taux de morbidité et de mortalité extrêmement élevé ; le SDE est impliqué dans plus de 3 % des interventions policières impliquant un recours à la force, est associé à plus de 10 % des décès en garde à vue, et entre 38 % et 86 % des décès liés au SDE sont survenus en garde à vue, en particulier associés aux méthodes de coercition policières et/ou à l’asphyxie positionnelle2.
En soi, l’ExDS comporte un risque de mortalité extrêmement élevé, avec environ 2/3 des patients ExDS qui meurent dans le cadre préhospitalier7 en l’absence de tout traumatisme majeur, de contrainte physique ou d’intervention de la police. La mortalité est plus fortement associée à la dépression respiratoire, à l’hyperthermie sévère, à l’acidémie ou à une combinaison de ces facteurs.8 Parmi ces facteurs, l’hyperthermie profonde présente la plus forte association avec la mortalité:9 Les températures centrales extrêmes peuvent altérer la perméabilité de la barrière hémato-encéphalique, contribuer au dysfonctionnement ou à la dégradation des protéines et potentialiser la neurotoxicité induite par le glutamate.10
Diagnostic différentiel
À ce jour, il n’existe pas de définition universellement reconnue du SDE. La description initiale s’est développée à partir de l’identification post-mortem basée sur l’histoire et était un terme englobant utilisé dans de nombreux contextes médicaux et juridiques. Dans un livre blanc publié en 2009, l’American College of Emergency Physicians a décrit l’ExDS comme un sous-ensemble de l’AMS et a recommandé que, malgré l’imprécision de l’entité clinique, les caractéristiques saillantes de l’histoire soient combinées au diagnostic différentiel des causes courantes de l’AMS pour décrire la présentation. L’ExDS a été décrit comme » un syndrome d’étiologie incertaine caractérisé par le délire, l’agitation et un dysfonctionnement autonome hyperadrénergique « , avec » des symptômes caractéristiques de comportement bizarre et agressif, de cris, de paranoïa, de panique, de violence envers les autres, de force physique inattendue et d’hyperthermie « .1 Les patients atteints d’ExDS présentent généralement une combinaison d’agitation, de tolérance accrue à la douleur, de tachypnée et de diaphorèse ; ces patients ont tendance à développer une acidémie sévère qui évolue vers un arrêt cardiaque soudain.11 Les caractéristiques de présentation communes du syndrome et le large chevauchement avec d’autres conditions nécessitent la recherche d’autres étiologies sous-jacentes, comme indiqué dans le tableau 1.
Gestion
La gestion est adaptée à la présentation du patient et doit être centrée sur 4 piliers de soins fondés sur des preuves : contrôle de l’agitation, correction de l’hyperthermie, évitement de l’acidose et recherche de l’étiologie sous-jacente (tableau 1).
Parce que l’asphyxie positionnelle, la dépression respiratoire, l’hyperthermie sévère, l’acidose, et/ou les arythmies fatales induites par les catécholamines12 peuvent précipiter le collapsus cardiovasculaire, ceux-ci doivent être prévenus et pris en charge de manière agressive. Ces principes sont valables aussi bien dans le cadre préhospitalier qu’aux urgences, car une reconnaissance rapide et un traitement délibéré et approprié par les prestataires de services préhospitaliers peuvent réduire les dommages et prévenir les mauvais résultats. De nombreux services d’urgence disposent de protocoles spécifiques pour traiter le SDE, qui mettent souvent l’accent sur la primauté d’un positionnement sûr et d’une sédation rapide à l’aide de benzodiazépines et/ou de kétamine. S’ils ne sont pas explicitement définis dans le protocole, les prestataires de services préhospitaliers doivent donner la priorité à ces approches dans la pratique, en reconnaissant que les patients ExDS sont, ou ont le potentiel de devenir très rapidement gravement malades. L’identification précoce par le personnel du SAMU peut atténuer le risque de mort subite, alerter le personnel des urgences d’accueil et aider les médecins légistes à mieux comprendre la présentation et à identifier la probabilité que le patient ait été victime d’un ExDS.13
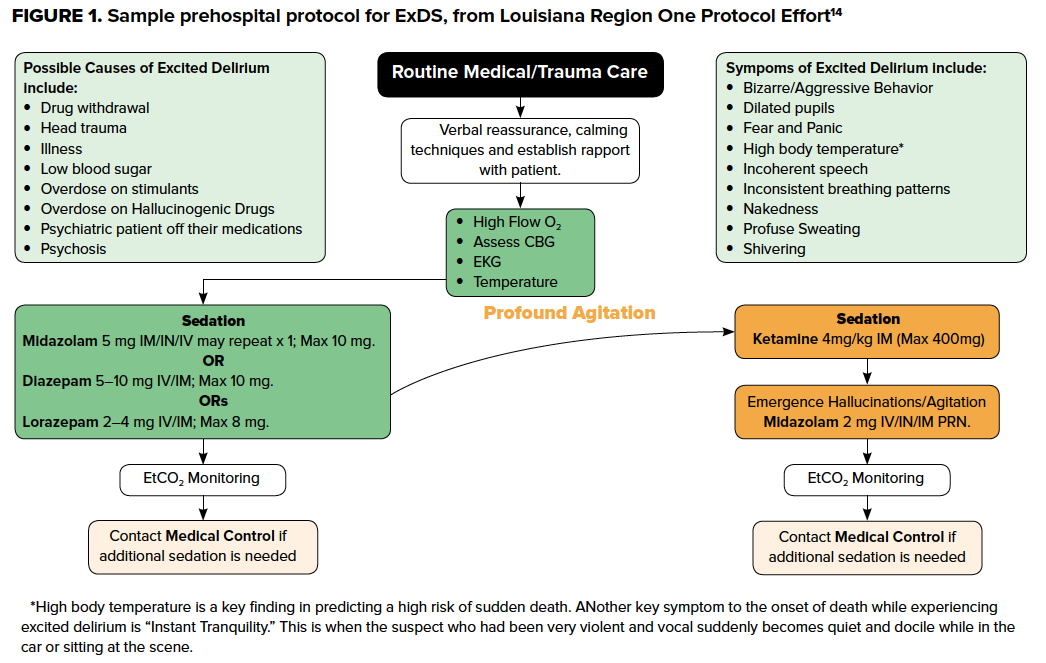
Contrôle de l’agitation
Les recommandations consensuelles pour la gestion pharmacologique du SMA consistent à traiter d’abord l’étiologie sous-jacente et ensuite les symptômes comportementaux. Cependant, le SDE est caractérisé par un état d’agitation dangereuse qui nécessite presque universellement une sédation.2 L’agitation sévère peut empêcher l’accès IV ou les analyses au début de la rencontre avec le patient. L’agitation grave peut empêcher l’accès IV ou les analyses dès le début de la rencontre avec le patient. Ainsi, les objectifs initiaux chez le patient indifférencié souffrant de SDE doivent être de fournir rapidement et efficacement une sédation tout en immobilisant le patient dans une position sûre. Suite à de nombreux décès de patients placés sous contention à l’hôpital, la Joint Commission et de nombreuses politiques hospitalières ont élaboré des exigences spécifiques pour des contentions physiques sûres. Il s’agit notamment de réévaluer fréquemment, en face à face avec le soignant, la nécessité de la contention afin de minimiser la durée de la contention mécanique. Les principes importants à respecter lors de la contention d’un patient sont d’éviter toute pression sur le visage, le cou et la poitrine, ce qui entraînerait une asphyxie, une acidose respiratoire ou métabolique et la mort. De même, l’ExDS peut être secondaire à l’hypoxie, et il est préférable de placer un masque sans réinspiration avec de l’oxygène à 100 %, car il fait office de masque à crachat. De plus, il est souvent nécessaire d’utiliser des contentions à 4 ou 5 points, en plaçant le patient en position couchée avec la tête du lit élevée à 30° tout en retenant un des bras du patient au-dessus de la tête et l’autre sous la taille.
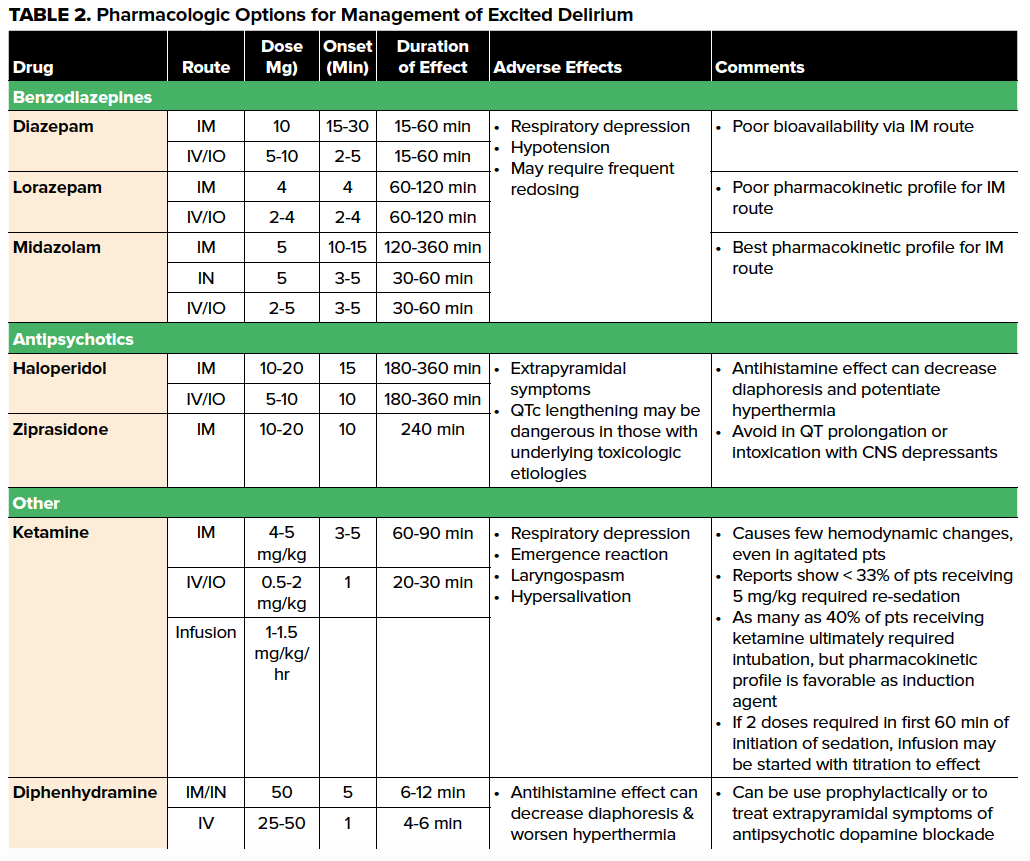
Bien que les piliers traditionnels de la gestion pharmacologique de l’agitation comprennent les benzodiazépines (en particulier le lorazépam et le midazolam), les antihistaminiques comme la diphénhydramine et les antipsychotiques, ces médicaments présentent de nombreux inconvénients chez le patient ExDS (tableau 2). Étant donné que la progression vers le collapsus cardiovasculaire est le plus souvent associée à l’hyperthermie, à la dépression respiratoire et à l’acidémie, les choix pharmacologiques en matière de sédation des patients atteints de SDE doivent compléter les efforts visant à contrer ces altérations physiologiques, et non les aggraver. Ces dernières années, les pénuries nationales de diazépam et de lorazépam intraveineux15, ainsi que la prépondérance des preuves et la préférence des prestataires de soins ont encouragé l’utilisation de la kétamine pour la gestion de la sédation du SDE, avec des gammes de dosage typiques fournies dans le tableau 2. La latitude relative dans le calcul et la voie d’administration, le début rapide de l’action et la facilité de progression de la sédation à l’induction et à l’intubation en séquence retardée ou rapide font de la kétamine un bon choix primaire pour les patients souffrant de SDE avec ou sans accès IV.16 Un autre avantage de la kétamine est le fait qu’elle préserve les réflexes des voies aériennes du patient, lui permettant de continuer à respirer spontanément. Bien que la plupart des patients sédatés à la kétamine ne nécessitent pas une gestion agressive des voies respiratoires, l’attention portée aux voies respiratoires du patient, ainsi que la surveillance de la sédation procédurale, doivent être utilisées chez tous les patients ExDS traités à la kétamine.
Correction de l’hyperthermie
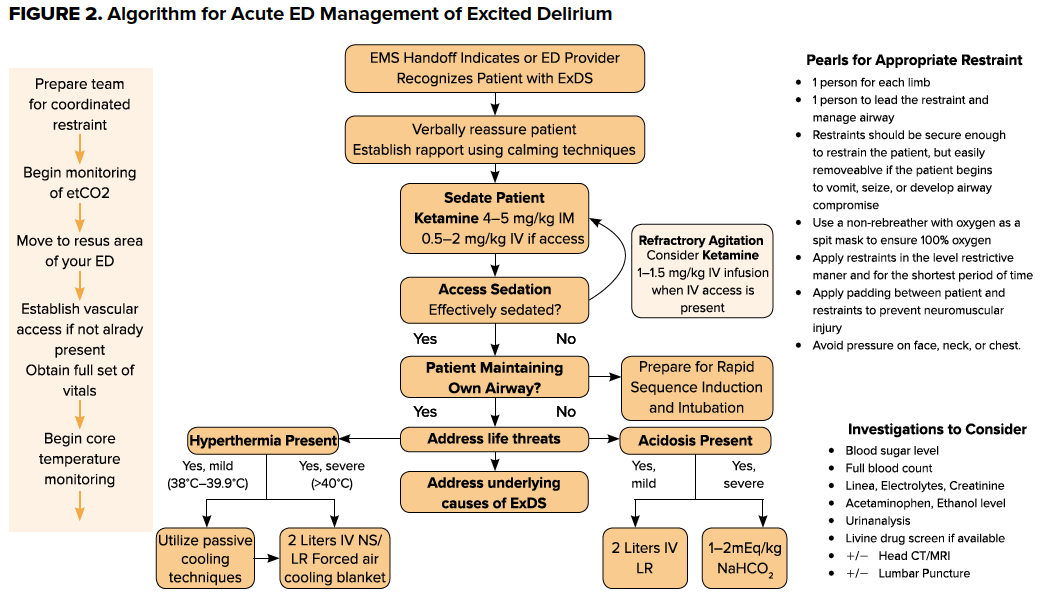
La gestion de l’hyperthermie est un principe important de la gestion de l’ExDS, et doit être initiée immédiatement après le contrôle de l’agitation. La gestion de la température dans l’ExDS est similaire à celle dans le cadre de l’hyperthermie environnementale, et peut inclure le retrait des vêtements, le refroidissement externe passif, les systèmes de couverture de refroidissement à air forcé, et les fluides IV froids.
Éviter l’acidose
L’évitement de toute acidose est important, et peut être secondaire à une variété d’étiologies, y compris l’hypoperfusion, la rhabdomyolyse, et la dépression respiratoire. Dans le cadre du bilan initial, des gaz du sang veineux ou artériel doivent être obtenus pour évaluer les déséquilibres acido-basiques sous-jacents. La prise en charge doit être ciblée sur la pathologie sous-jacente et peut inclure une réanimation liquidienne intraveineuse ou une assistance respiratoire. Dans le cas d’un patient ExDS pris en charge par sédation, y compris la kétamine, la surveillance du CO2 end-tidal (etCO2) est nécessaire pour surveiller la fréquence, la profondeur et l’adéquation de la respiration.
Investigation de l’étiologie sous-jacente
Après que le patient ait été stabilisé et sédaté, le bilan doit être guidé par l’examen physique et l’histoire. Un examen physique complet est essentiel – les patients souffrant de SDE peuvent avoir des blessures sous-jacentes importantes, et les efforts de contention peuvent exacerber tout traumatisme préexistant. Les examens initiaux doivent inclure une glycémie, une NFS, une BMP et un dépistage toxicologique de tout coingestant. Envisager des CPK si l’on soupçonne une rhabdomyolyse, des hémocultures et/ou une PL si l’on craint une septicémie et/ou une méningite septique. L’imagerie peut être poursuivie afin d’examiner tout traumatisme sous-jacent potentiel.
Conclusion du cas
Après transfert sur la civière de l’urgence, le patient a été placé dans des contentions souples à 4 points avec un nonrebreather et de l’oxygène à 100% avec l’aide de la sécurité de l’hôpital ; 5 mg/kg de kétamine IM ont été administrés, avec une réduction significative de l’agitation. Le patient a été placé sous etCO2 et amené dans la salle de réanimation pour une surveillance étroite. On a constaté qu’il était tachycardique avec un pouls de 150, hypertendu à 150/94, hyperthermique à 39,6° C. L’examen endotrachéal a révélé 38mmHg de CO2 et 20 respirations/minute. Les examens de laboratoire n’ont révélé aucune anomalie. Des packs froids ont été placés au niveau des aisselles et de l’aine, et 2 L de ringers lactés refroidis ont été administrés par voie IV avec une amélioration de la température.
Sur la base de l’examen physique et de l’histoire, la préoccupation était pour un délire excité secondaire à un agent sympathomimétique inconnu avec des qualités hallucinogènes, et le patient a été admis à l’étape de l’USI avec des soins de soutien.
Le délire agité du patient s’est résolu le deuxième jour d’hospitalisation, et il a été transféré en psychiatrie hospitalière pour une observation continue. Il est sorti le jour 4 avec une orientation vers les services psychiatriques et un soutien pour la consommation de drogues.
1. Mash D. Délire excité et mort subite : Un trouble syndromal à l’extrémité du continuum neuropsychiatrique. Front Physiol. 2016;7:435.
2. Gonin P, Beysard N, Yersin B, Carron PN. Le délire d’excitation : une revue systématique. Acad Emerg Med. 2018;25(5):552-565.
3. Vilke GM, DeBard ML, Chan TC, et al. Excited Delirium Syndrome (ExDS) : définition basée sur une revue de la littérature. J Emerg Med. 2012;43(5):897-905.
4. Wetli CV, Fishbain DA. Psychose et mort subite induites par la cocaïne chez les consommateurs récréatifs de cocaïne. J Forensic Sci. 1985;30(3):873-880.
5. Atis SE, Yilmaz G, Bozan O, Cekmen B. Une drogue terrifiante menace les rues : Flakka – Un rapport de cas. J Mol Imag Dynamic. 2018;8(1):142.
6. Prosser JM, Nelson LS. La toxicologie des sels de bain : une revue des cathinones synthétiques. J Med Toxicol. 2012;8(1):33-42.
7. Gottlieb M, Long B, Koyfman A. Approche du patient agité du service des urgences. J Emerg Med. 2018;54(4):447-457.
8. Otahbachi M, Cevik C, Bagdure S, Nugent K. Délire excité, contentions et mort inattendue : une revue de la pathogénie. Am J Forensic Med Pathol. 2010;31(2):107-112.
9. Mash DC. Délire excité et mort subite : Un trouble syndromal à l’extrémité du continuum neuropsychiatrique. Front Physiol. 2016;7:435.
10. Plush T, Shakespeare W, Jacobs D, Ladi L, Sethi S, Gasperino J. Cocaine-induced agitated delirium : a case report and review. J Intensive Care Med. 2015;30(1):49-57.
11. DeBard ML, Adler J, Bozeman W, Chan T, et al : ACEP Excited Delirium Task Force. Rapport du livre blanc sur le syndrome du délire excité. 2009.
12. Mort S. BET 1 : syndrome du délire excité et mort subite. Emerg Med J. 2013;30(11):958-960.
13. Vilke GM, Bozeman WP, Dawes DM, Demers G, Wilson MP. Syndrome du délire excité (ExDS) : Options de traitement et considérations. J Forensic Leg Med. 2012;19(3):117-121.
14. Ville de la Nouvelle-Orléans. Effort de protocole de la région 1. État de la Louisiane. 2013.
15. Tassey T. Out of Ativan ?! La crise de pénurie de médicaments aux États-Unis EM Resident. 2016;43(1):28-29.
16. Mankowitz SL, Regenberg P, Kaldan J, Cole JB. La kétamine pour la sédation rapide des patients agités dans le cadre des services préhospitaliers et d’urgence : A Systematic Review and Proportional Meta-Analysis. J Emerg Med. 2018;55(5):670-681.
