Le terme stéréochimique diastéréotopique fait référence à la relation entre deux groupes dans une molécule qui, s’ils étaient remplacés, généreraient des composés qui sont des diastéréoisomères. Les groupes diastéréotopiques sont souvent, mais pas toujours, des groupes identiques attachés au même atome dans une molécule contenant au moins un centre chiral.
Par exemple, les deux atomes d’hydrogène de la fraction CH2 dans le (S)-2-bromobutane sont diastéréotopiques. Le remplacement d’un atome d’hydrogène (coloré en bleu) par un atome de brome produira le (2S,3R)-2,3-dibromobutane. Le remplacement de l’autre atome d’hydrogène (coloré en rouge) par un atome de brome produira le diastéréoisomère (2S,3S)-2,3-dibromobutane.
 |
 |
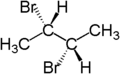 |
| (S)-2-bromobutane | (2S,3R)-2,3-dibromobutane | (2S,3S)-2,3-dibromobutane |
Dans les molécules chirales contenant des groupes diastéréotopiques, comme dans le 2-bromobutane, il n’y a aucune exigence de pureté énantiomérique ou optique ; quelle que soit sa proportion, chaque énantiomère générera des ensembles énantiomères de diastéréoisomères lors de la substitution des groupes diastéréotopiques (bien que, comme dans le cas de la substitution par le brome dans le 2-bromobutane, les isomères méso n’ont, à proprement parler, aucun énantiomère).
Les groupes diastéréotopiques ne sont pas des images miroir les uns des autres autour d’un plan quelconque. Ils sont toujours différents, dans n’importe quel environnement, mais peuvent ne pas être distingués. Par exemple, les deux paires d’hydrogènes CH2 dans le chlorhydrate de phénylalaninate d’éthyle (PhCH2CH(NH3+)COOCH2CH3 Cl-) sont diastéréotopiques et donnent toutes deux des paires de signaux 1H-RMN distincts dans le DMSO-d6 à 300 MHz, mais dans le 2-nitrobutanoate d’éthyle similaire (CH3CH2CH(NO2)COOCH2CH3), seul le groupe CH2 à côté du centre chiral donne des signaux distincts de ses deux hydrogènes avec le même instrument dans le CDCl3. Ces signaux sont souvent complexes en raison de petites différences de déplacement chimique, d’un chevauchement et d’un couplage fort supplémentaire entre les hydrogènes géminés. D’autre part, les deux groupes CH3 de l’ipsénol, qui sont à trois liaisons du centre chiral, donnent des doublets 1H séparés à 300 MHz et des signaux 13C-RMN séparés dans le CDCl3, mais les hydrogènes diastéréotopiques dans le chlorhydrate d’alaninate d’éthyle (CH3CH(NH3+)COOCH2CH3 Cl-), également à trois liaisons du centre chiral, présentent des signaux 1H-RMN à peine distinguables dans le DMSO-d6.

Des groupes diastéréotopiques apparaissent également dans les molécules achirales. Par exemple, une paire quelconque d’hydrogènes CH2 dans le 3-pentanol (figure 1) est diastéréotopique, car les deux carbones CH2 sont énantiotopiques. La substitution de l’un quelconque des quatre hydrogènes CH2 crée deux centres chiraux à la fois, et les deux produits possibles de la substitution de l’hydrogène à l’un quelconque des carbones CH2 seront des diastéréoisomères. Ce type de relation est souvent plus facile à détecter dans les molécules cycliques. Par exemple, toute paire d’hydrogènes CH2 dans le cyclopentanol (figure 2) est de manière similaire diastéréotopique, et ceci est facilement discernable car l’un des hydrogènes de la paire sera cis au groupe OH (du même côté de la face du cycle) tandis que l’autre sera trans à celui-ci (du côté opposé).
Le terme diastéréotopique s’applique également à des groupes identiques attachés à la même extrémité d’un fragment d’alcène qui, s’ils étaient remplacés, généreraient des isomères géométriques (entrant également dans la catégorie des diastéréoisomères). Ainsi, les hydrogènes CH2 du propène sont diastéréotopiques, l’un étant cis par rapport au groupe CH3, et l’autre étant trans par rapport à lui, et le remplacement de l’un ou l’autre par CH3 générerait du cis- ou du trans–2-butène.

La diastéréotopicité n’est pas limitée aux molécules organiques, ni aux groupes attachés au carbone, ni aux molécules avec des centres tétraédriques chiraux (hybridés sp3) : par exemple, la paire d’hydrogènes dans tout groupe CH2 ou NH2 dans l’ion tris(éthylènediamine)chrome(III) (Cr(en)33+), où le centre métallique est chiral, sont diastéréotopiques (figure 2).
Les termes énantiotopique et diastéréotopique peuvent également être appliqués aux faces des groupes planaires (notamment les groupes carbonyles et les moitiés d’alcènes). Voir la règle de priorité de Cahn-Ingold-Prelog.
