クロロベンゼン 化学的性質、用途、生産
用途
フェノール、アニリン、DDT製造;塗料用溶剤;カラー印刷;ドライクリーニング業。
概要
クロロベンゼンは、ベンゼン環上の水素原子が1個塩素で置換された単環の芳香族化合物である。 液相で触媒を用いてベンゼンを塩素化することにより製造されます。 クロロベンゼンは、常温では無色でアーモンドに似た甘い香りのする可燃性の液体で、比較的高い蒸気圧、中程度のオクタノール-水分配係数(log 2.8)、中程度から低い水溶性(497.9 mg/L @ 25℃)を有しています。 クロロベンゼンは非極性溶媒には高い溶解度を示しますが、水にはほとんど溶解しません。 テクニカルグレードのクロロベンゼンは通常99%の純度で、< 0.05% のベンゼン、< 0.1% のジクロロベンゼンが汚染物質として含まれている。 一般的な溶剤であり、他の化学物質の製造に広く使用される中間体である。 Rhodococcus phenolicusは、クロロベンゼンを唯一の炭素源として分解することができる細菌種である。
用途
- クロロベンゼンは主にo-およびp-ニトロクロロベンゼン、2,4-ジニトロクロロベンゼンの合成原料として用いられる。ニトロクロロベンゼンの生産以外の重要な定量的化学変換はジフェニルオキシド、ジフェニルジクロロシランが生産されることである。
- クロロベンゼンは主にトリフェニルホスフィン(有機合成用触媒)、フェニルシラン、チオフェノール(農薬・医薬中間体)などの化学品の合成原料として使用される。 また、メチレンジフェニルジイソシアネートなどの有機合成反応用溶剤、ウレタン原料、農業用アジュバント、塗料・インキ、電子機器用洗浄溶剤などの合成原料としても使用されます。
- フェノール、アニリン、DDTの製造、塗料用溶剤、熱媒体
- クロロベンゼンはMDIやTDIなどのイソシアネート製造のプロセス溶剤、各種農薬製剤の溶剤として使用されています。 さらに染料産業における縮合反応の溶媒としても使用されます。
- クロロベンゼンは化学合成に使用される基本物質で、使用量の95%は閉鎖系で中間製品や最終製品に変換されます。
- 3種の無定形染料と顔料の生産においてプロセス溶剤として使用されます。 顔料や染料はすべてチオインジゴイドカラーです。
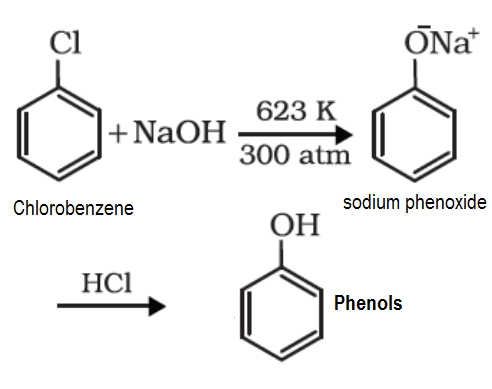
- クロロベンゼンはベンゼン環のモノ置換によって形成されるハロアレーンの一例です。 クロロベンゼンを623K、320atmで水酸化ナトリウムと融合させるとフェノキシドナトリウムが生成する。 3611>
毒性
クロロベンゼンの人に対する毒性は、疲労、吐き気、嗜眠、頭痛、上気道および眼の刺激である。 クロロベンゼンの皮膚への接触は刺激を引き起こした。 3611>クロロベンゼンの経口LD50値は、マウスで1,445 mg/kg、ラットで1,427~3,400 mg/kg、ウサギで2,250~2,830 mg/kgであった。 6時間吸入ばく露後のLC50は、マウスで1,889 ppm、ラットで2,968 ppmであった。
化学的性質
無色液体 触媒(FeCl3またはAICI3)の存在下、ベンゼンを塩素化すると、第一生成物としてクロロベンゼンが得られる。 第二のCIで置換するとオルト、パラ、メタジクロロベンゼンが得られ、最終的にはすべての水素が置換されてヘキサクロロベンゼン(C6C16)が得られる。 紫外線の存在下でベンゼンを塩素化すると、シクロヘキサンの誘導体である六塩化ベンゼン(C6H6C~)が生成する。
化学的性質
クロロベンゼンは、モノクロロベンゼンとも呼ばれ、単環の芳香族化合物である。 無色の液体で、アーモンドのような芳香族臭があり、溶剤として使用するために製造され、他の化学物質(殺虫剤)の製造や、特定の他の化学物質、ゴム、染料、グリース溶剤の製造に使用されています。 オルトおよびパラニトロクロロベンゼンやアニリンを製造するための原料として、塗料の溶剤として、また熱媒体として使用されています。 過去には、クロロベンゼンはフェノールやDDTの製造の中間体として使用されていました。 クロロベンゼンは、産業界や自治体の排出物から環境中に侵入します。 また、廃棄物焼却炉での不完全燃焼によるクロロベンゼンの生成と排出も考えられます。
クロロベンゼンは水に中程度に溶け、1,000ミリグラムまでは1リットルの水と混ざります。 クロロベンゼンは水にやや溶けにくく、半減期は2~20日です。 クロロベンゼンは、土壌中(数ヶ月)、空気中(3.5日)、水中(1日未満)で難分解性である。
この化合物は加熱して分解すると、塩化水素ガス、COおよびCO2の有毒なガスを発生する。 一般的な同義語は、モノクロロベンゼン、塩化ベンゼン、クロロベンゾルである。 強酸化剤、ジメチルスルホキシドとは相容れない。
クロロベンゼン(別名:モノクロロベンゼン、MCB)は、引火性の液体である。 また、接着剤、塗料、塗料除去剤、つや出し剤、染料、薬剤の製造にも使用されています。 過去には、フェノールや関連化学物質、農薬(DDTなど)、アニリンを作るためにMCBを使用していた。
クロロベンゼンは、空気に触れると蒸発することがある。 水と混ぜるとわずかに溶ける。 クロロベンゼンの健康や環境への影響は、クロロベンゼンがどの程度存在するか、暴露の長さや頻度に依存します。 また、暴露時の人の健康状態や環境の状態にも依存する。
物理的性質
無色透明の可燃性液体で、甘いアーモンドのような、薬品のような、あるいは防虫剤のようなにおいがする。 Leonardosら(1969)は、210ppbvの臭気閾値濃度を報告している。 40℃において、臭気が検出された最低濃度は190μg/Lであった。 25 ℃で、味が検出される最低濃度は 190 μg/L であった (Young et al., 1996)。 60 ℃の水中での平均的な最小検出臭閾値濃度は 0.08 mg/L であった (Alexander et al., 1982)。 Cometto-Mu?izand Cain (1994) は、平均鼻腔刺激性閾値濃度を 10,553 ppmv と報告している。
用途
塗料用溶剤、熱媒体、フェノールやアニリンの製造に使用される。
用途
クロロベンゼンはハロゲン化ベンゼンであり、農業汚染の化学的毒性QSAR研究に使用されています。
用途
モノクロロベンゼンは溶剤として商業的に使用され、フェノールやニトロクロロベンゼンの製造に使用される。
定義
ChEBI。 モノクロロベンゼン類の中で最も単純なもので、1個の水素が塩素で置換されたベンゼンである。
定義
塩素とベンゼンの触媒反応による無色の液体で、水酸化ナトリウムと極限状態(300℃、200気圧)で反応させるとフェノールに変換される。 また、他の有機化合物の製造にも使用される。
合成参考文献
Journal of the American Chemical Society, 74, p.6297, 1952 DOI: 10.1021/ja01144a523
Tetrahedron Letters, 23, p.371, 1982 DOI: 10.1016/S0040-4039(00)86833-1
概要
無色~澄明の黄色っぽい液体でアーモンド様の甘いにおいがする。 引火点84°F。 水にほとんど溶けず、水よりやや濃い(9.2 lb / gal)。 蒸気は空気より重い。 農薬、染料、その他の化学物質の製造に使用される。
空気 & 水反応
極めて可燃性が高い。 水に不溶。
反応性プロファイル
粉末状のナトリウムまたは三塩化リン+ナトリウムと時々爆発的な反応を起こす。 ジメチルスルホキシドとは激しく反応することがある。 酸化剤と激しく反応する。 プラスチック、ゴム、塗膜の一部を侵す。 過塩素酸銀と衝撃に弱い溶媒和塩を形成する。 .
有害性
発がん性の可能性がある。 吸入および皮膚接触を避ける。 火災の危険性は中程度。 爆発限界は1.8-9.6%。
健康被害
皮膚、目、粘膜を刺激する。 皮膚に繰り返し接触すると、脱脂作用により皮膚炎を起こすことがある。 蒸気やミストの慢性的な吸入により、肺、肝臓、腎臓に障害を与える可能性がある。 急性蒸気暴露は、咳から一過性の麻酔および中枢神経系抑制までの症状を引き起こす可能性がある。
クロロベンゼンの急性(短期)影響については、限られた情報しか得られていない。 クロロベンゼンの急性吸入暴露は、ナルコーシス、落ち着きのなさ、震え、筋肉の痙攣を引き起こした。 クロロベンゼンのヒトへの慢性(長期)暴露は、中枢神経系(CNS)に影響を及ぼす。 ヒトの神経毒性の徴候には、しびれ、チアノーゼ、知覚過敏(感覚の増大)、筋肉の痙攣が含まれる。 クロロベンゼンのヒトにおける発がん性の影響については、情報がありません。 EPA はクロロベンゼンをグループ D に分類しており、ヒトに対する発がん性については分類できないとしている。
火災の危険性
引火性液体、引火点(密閉式カップ)29℃、蒸気圧8.8 torr at 20℃、自己発火温度638℃(1180°F)
クロロベンゼン蒸気は空気と1.3~7.1%(空気中)の範囲で爆発混合物を形成する。 ジメチルスルホキシドは、クロロベンゼンと接触すると激しく分解する(NFPA 1997)。 銀や水銀などの過塩素酸塩の多くは、衝撃に弱い溶媒和過塩素酸塩を形成し、衝撃で爆発する可能性がある。
安全性プロファイル
発がん性が疑われている。 摂取および腹腔内経路では中程度の毒性。 実験的催奇形性及び生殖への影響。 突然変異のデータあり。 強い麻薬性で、わずかに刺激性がある。 ジクロロベンゾールは強い麻薬性である。 低濃度での反復暴露の影響はほとんど知られていないが、腎臓および肝臓に障害を起こす可能性がある。 報告されている産業上の疾病は、おそらくニトロベンゾールが原因である可能性があります。 熱または炎にさらされた場合、危険な火災の危険性がある。 熱または炎にさらされた場合、中程度の爆発の危険がある。 粉末状のナトリウムまたは三塩化リン+ソジウムと爆発する可能性のある反応。 AgClO4と激しく反応する。 酸化剤と激しく反応する。 クロリン化炭化水素、芳香族も参照。 消火には、泡、CO2、ドライケミカル、水を使用し、火災をブランケット化する。 クロロベンゼンは、アニリン、フェノールおよびクロロニトロベンゼンの製造、染料および殺虫剤の製造における中間体、溶剤、乳化剤として使用されます。
発がん性
クロロベンゼンは、さまざまな細菌および酵母のアッセイにおいて変異原性を示さなかった。 既存のデータでは、クロロベンゼンのヒトへの暴露において遺伝毒性は懸念される領域ではない可能性が示唆された。
環境動態
生物学的。 活性汚泥中では、5日後にクロロベンゼンの31.5%が二酸化炭 素に無機化した (Freitag et al., 1985)。 土壌細菌とシュードモナス属細菌の混合培養では、クロロベンゼンはクロロフェノールに変換された(Ballschiter and Scholz, 1980)。 土壌から分離した純粋な微生物培養液はクロロベンゼンを2-および4-クロロフェノールに水酸化した (Smith andRosazza, 1974)。 クロロベンゼンは、酵母エキスと沈殿した生活排水の接種物とともに、25 ℃の暗所で静置培養された。 5 mg/Lの濃度で、1週間および2週間後の生分解収率はそれぞれ89および100%であった。 10 mg/Lの濃度では、有意な
出荷
UN1134 クロロベンゼン、ハザードクラス.A.C.、
出荷
UN1134 クロロベンゼン、ハザードクラス: 3;Labels: 3-引火性液体。
精製方法
主な不純物は、クロロベンゼンの合成に使用した*ベンゼンにもともと含まれていた塩素化不純物と、未塩素化炭化水素であると考えられる。 精製方法は、濃H2SO4で数回洗浄後、NaHCO3またはNa2CO3水溶液、水で洗浄し、CaCl2、K2CO3またはCaSO4で乾燥し、P2O5で精留する方法が一般的である。 また、リンデ4Aモレキュラーシーブで乾燥することもできる。 低コンダクタンス材料を得るために、活性アルミナを通過させ、その上に保管する方法が用いられています。
不適合 強酸化剤、ジメチルスルホキシド、ナトリウムパウダー、過塩素酸銀と激しく反応し、火災や爆発の危険を引き起こす。 一部のプラスチック、ゴム、コーティングを侵す。 加熱すると分解し、ホスゲン、塩化水素ガスを発生する。
廃棄上の注意
焼却する場合は、他の可燃性燃料と混合して焼却することが望ましい。
