Klorbensen Kemiska egenskaper, användning, produktion
Användning
Tillverkning av fenol, anilin, DDT; lösningsmedel för färg, färgtryck, kemtvättar.
Beskrivning
Klorbensen är en monocyklisk aromatisk förening där en väteatom på bensenringen är substituerad med ett klor. Den framställs genom klorering av bensen i flytande fas med en katalysator. Klorbensen är en färglös, brandfarlig vätska med en söt mandelliknande lukt vid rumstemperatur med ett relativt högt ångtryck, måttlig oktanol-vattenfördelningskoefficient (log 2,8) och måttlig till låg vattenlöslighet (497,9 mg/l vid 25 °C). Klorbensen har en hög löslighet i opolära lösningsmedel, men är nästan olöslig i vatten. Klorbensen av teknisk kvalitet är vanligtvis 99 % ren med < 0,05 % bensen och < 0,1 % diklorbenzener som föroreningar. Det är ett vanligt lösningsmedel och en ofta använd mellanprodukt vid tillverkning av andra kemikalier. Rhodococcus phenolicus är en bakterieart som kan bryta ned klorbensen som enda kolkälla.
Användningar
- Klorbensen används främst som råvara för syntesen av o- och p-nitrochlorbenzen och 2,4-dinitrochlorbenzen.Viktiga kvantitativa kemiska omvandlingar utöver framställningen av nitrochlorbenzener är framställningen av difenyloxid och difenyldiklorosilan.
- Klorbensen används huvudsakligen som råmaterial för syntes av kemikalier, inklusive trifenylfosfin (katalysator för organisk syntes), fenylsilan och tiofenol (bekämpningsmedel och farmaceutisk mellanprodukt). Det används också som råvara för syntes av lösningsmedel för organiska syntesreaktioner, inklusive metylendifenyldiisocyanat, uretanråvara, adjuvans för jordbruket, färg och bläck samt rengöringslösningsmedel för elektronik.
- framställning av fenol, anilin, DDT; lösningsmedel för färger; värmeöverföringsmedium.
- Khlorbensen används som processlösningsmedel vid framställning av isocyanater som MDI och TDI och som lösningsmedel i olika växtskyddsformuleringar. Det används vidare som lösningsmedel i kondensationsreaktioner inom färgämnesindustrin.
- Klorbensen är ett grundämne som används i kemiska synteser där 95 % av den använda mängden omvandlas i slutna system till mellan- och slutprodukter.
- Det används som processlösningsmedel vid framställning av tre indigoida färgämnen och pigment. Alla pigment och färgämnen är thioindigoida färger.
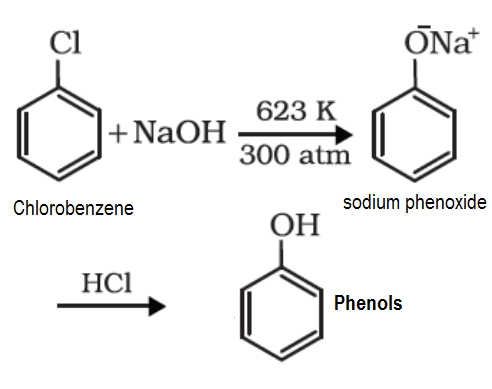
- Khlorbensen är ett exempel på haloarener som bildas genom monosubstitution av bensenringen. När klorbensen fusioneras med natriumhydroxid vid 623 K och 320 atm bildas natriumfenoxid. Slutligen ger natriumfenoxid vid försurning fenoler.
Toxicitet
De toxiska effekterna av klorbensen på människor var utmattning, illamående, letargi, huvudvärk och irritation av de övre luftvägarna och ögonen. Kontakt av klorbensen med huden framkallade irritation. Inga rapporter om sensibilisering av klorbensen erhölls i denna undersökning.
De orala LD50-värdena för klorbensen var 1 445 mg/kg hos möss, 1 427-3 400 mg/kg hos råttor och 2 250-2 830 mg/kg hos kaniner. LC50-värdena efter 6 timmars exponering genom inandning var 1 889 ppm hos möss och 2 968 ppm hos råttor.
Kemiska egenskaper
Färglös vätska, Klorering av bensen i närvaro av en katalysator (FeCl3 eller AICI3) ger klorbensen som första produkt. Substitution med ett andra CI ger ortho-, para- eller metadiklorbensen. Eventuellt kan alla väten substitueras för att ge hexaklorbensen, C6C16. I närvaro av ultraviolett ljus ger klorering av bensen bensenhexaklorid, C6H6C~, ett derivat av cyklohexan.
Kemiska egenskaper
Klorbensen, även kallat monoklorbensen, är en monocyklisk aromatisk förening. Det är en färglös vätska med en aromatisk mandelliknande lukt och tillverkas för användning som lösningsmedel, används vid tillverkning av andra kemikalier (bekämpningsmedel) och vid tillverkning av vissa andra kemikalier, gummi, färgämnen och fettlösningsmedel. Den används som råmaterial för att framställa orto- och paranitrochlorbenzener och anilin, som lösningsmedel för färger och som värmeöverföringsmedium. Tidigare användes klorbensen som mellanprodukt vid framställning av fenol och DDT. Klorbensen kommer in i miljön från industriella och kommunala utsläpp. En annan potentiell källa är bildning och utsläpp av klorbensen som en produkt av ofullständig förbränning i avfallsförbränningsanläggningar.
Klorbensen är måttligt löslig i vatten; upp till 1 000 milligram blandas med en liter vatten. Klorbensen är svagt persistent i vatten, med en halveringstid på mellan 2 och 20 dagar. Klorbensen är persistent i jord (flera månader), luft (3,5 dagar) och vatten (mindre än 1 dag).
Vid upphettning till nedbrytning avger denna förening giftiga ångor av vätekloridgas, CO och CO2. Vanliga synonymer är monoklorbensen, bensenklorid och klorbenzol. Den är oförenlig med starka oxidationsmedel och dimetylsulfoxid.
Klorbensen (även bäst känd som monoklorbensen eller MCB) är en brandfarlig vätska. Företag använder också MCB för att tillverka lim, färger, färgborttagningsmedel, polermedel, färgämnen och läkemedel. Tidigare har företag använt MCB för att tillverka fenol och relaterade kemikalier, bekämpningsmedel (som DDT) och anilin.
Klorbensen kan avdunsta när den utsätts för luft. Den löser sig något när den blandas med vatten. Effekter av klorbensen på människors hälsa och miljön beror på hur mycket klorbensen som finns och hur länge och hur ofta man exponeras. Effekterna beror också på personens hälsa eller miljöns tillstånd när exponeringen sker.
Fysiska egenskaper
Klar, färglös, brandfarlig vätska med en söt mandel-, medicin- eller malkuleliknande lukt. En lukttröskelkoncentration på 210 ppbv rapporterades av Leonardos et al. (1969). Vid 40 °C var den lägsta koncentration vid vilken en lukt upptäcktes 190 μg/L. Vid 25 °C var den lägsta koncentration vid vilken en smak upptäcktes 190 μg/L (Young et al., 1996). Den genomsnittliga lägsta koncentrationen vid 60 °C för den minst påvisbara lukttröskeln i vatten var 0,08 mg/L (Alexander et al., 1982). Cometto-Mu?iz och Cain (1994) rapporterade en genomsnittlig tröskelkoncentration för nasal doft av 10 553 ppmv.
Användningar
Klorbensen används som lösningsmedel för färger, som värmeöverföringsmedium och vid tillverkning av fenol och anilin.
Användningar
Klorbensen är en halogenerad bensen som används i QSAR-forskning om kemisk toxicitet för föroreningar i jordbruket.
Användningar
Monoklorbensen används kommersiellt som lösningsmedel och för att framställa fenol och nitrochlorbenzener.
Definition
ChEBI: Den enklaste medlemmen av klassen monoklorbensenar, dvs. bensen där ett enda väte har ersatts av ett klor.
Definition
Färglös vätska som framställs genom katalytisk reaktion av klor med bensen och som kan omvandlas till fenol genom reaktion med natriumhydroxid under extrema förhållanden (300 °C och 200 atmosfärers tryck). Den används också vid tillverkning av andra organiska föreningar.
Syntes Referens(er)
Journal of the American Chemical Society, 74, s. 6297, 1952 DOI: 10.1021/ja01144a523
Tetrahedron Letters, 23, s. 371, 1982 DOI: 10.1016/S0040-4039(00)86833-1
Allmän beskrivning
En färglös till klar, gulaktig vätska med en söt mandellik lukt. Flampunkt 84°F. Praktiskt taget olöslig i vatten och något tätare än vatten (9,2 lb / gal). Ångor är tyngre än luft. Används för att framställa bekämpningsmedel, färgämnen och andra kemikalier.
Luft &Vatten Reaktioner
Lättantändligt. Olösligt i vatten.
Reaktivitetsprofil
Klorbensen genomgår en ibland explosiv reaktion med pulveriserad natrium eller fosfortriklorid + natrium. Kan reagera våldsamt med dimetylsulfoxid. Reagerar kraftigt med oxiderande ämnen. Angriper vissa former av plast, gummi och beläggningar. Bildar ett stötkänsligt solvatiserat salt med silverperklorat. .
Farligt
Möjligen cancerframkallande. Undvik inandning och hudkontakt. Måttlig brandrisk. Explosionsgränser 1,8-9,6 %.
Hälsofara
Irriterande för hud, ögon och slemhinnor. Upprepad exponering av huden kan orsaka dermatit på grund av avfettningsverkan. Kronisk inandning av ångor eller dimma kan leda till skador på lungor, lever och njurar. Akut exponering för ångor kan orsaka symtom som sträcker sig från hosta till övergående bedövning och depression i centrala nervsystemet.
Det finns begränsad information om de akuta (kortsiktiga) effekterna av klorbensen. Akut inhalationsexponering av djur för klorbensen gav narkos, rastlöshet, skakningar och muskelspasmer. Kronisk (långvarig) exponering av människor för klorbensen påverkar det centrala nervsystemet (CNS). Tecken på neurotoxicitet hos människor inkluderar domningar, cyanos, hyperestesi (ökad känsel) och muskelspasmer. Det finns ingen information om klorbensens cancerframkallande effekter på människor. EPA har klassificerat klorbensen som en grupp D, som inte kan klassificeras som cancerframkallande för människor.
Brandfarlighet
Brandfarlig vätska; flampunkt (sluten kopp)29°C (84°F); ångtryck 8,8 torr vid20°C (68°F); självantändningstemperatur 638°C (1180°F).
Klorbensenångor bildar explosiva blandningar med luft inom intervallet 1,3-7,1 volymprocent i luft. Dimetylsulfoxid sönderfaller våldsamt i kontakt med klorbensen (NFPA 1997). Många metallperklorater, t.ex. silver- och kvicksilverperklorater, kan bilda stötkänsliga solvatiserade perklorater som kan explodera vid en stöt.
Säkerhetsprofil
Misstänkt cancerframkallande. Måttligt giftigt genom förtäring och intraperitoneal väg. Experimentella teratogena och reproduktiva effekter. Uppgifter om mutationer har rapporterats. Starkt narkotiskt ämne med lätt irriterande egenskaper. Diklorbenzoler är starkt narkotiska. Man vet lite om effekterna av upprepad exponering vid lägre koncentrationer, men det kan orsaka skador på njurar och lever. De arbetssjukdomar som rapporterats kan möjligen bero på nitrobenzol. Farlig brandrisk vid exponering för värme eller flammor. Måttlig explosionsrisk vid exponering för värme eller flammor. Potentiellt explosiv reaktion med pulveriserad natrium eller fosfortriklorid + natrium. Våldsam reaktion med AgClO4. Reagerar kraftigt med oxidationsmedel. Se även KALORERADE HYDROKARBONER, AROMATISKA. För att bekämpa branden, använd skum, CO2, torrkemikalier, vatten för att täcka branden. Associerad med EPA Superfund sites
Potentiell exponering
Klorbensen används vid tillverkning av anilin, fenol och klornitrobenzen, som mellanprodukt vid tillverkning av färgämnen och bekämpningsmedel, som lösningsmedel och emulgeringsmedel.
Carcinogenicitet
Klorbensen var inte mutagent i olika bakterie- och jästanalyser. Befintliga uppgifter tyder på att genotoxicitet kanske inte är ett problemområde när det gäller exponering för klorbensen hos människor.
Miljöförlopp
Biologiskt. I aktiverat slam mineraliserades 31,5 % av den applicerade klorbensenen till koldioxid efter 5 dagar (Freitag et al., 1985). En blandkultur av jordbakterier eller en Pseudomonas sp. omvandlade klorbensen till klorfenol (Ballschiter och Scholz, 1980). Rena mikrobiella kulturer isolerade från jord hydroxylerade klorbenzen till 2- och 4-klorfenol (Smith och Rosazza, 1974). Klorbensen inkuberades statiskt i mörker vid 25 °C med jästextrakt och inokulum av sedimenterat hushållsavloppsvatten. Vid en koncentration på 5 mg/L var den biologiska nedbrytningen i slutet av 1 och 2 veckor 89 respektive 100 %. Vid en koncentration på 10 mg/L var signifikant
Skeppning
UN1134 Klorbensen, faroklass: 3;Etiketter: 3 – Brandfarlig vätska.
Reningsmetoder
De viktigaste föroreningarna är sannolikt klorerade föroreningar som ursprungligen fanns i *bensen som användes vid syntesen av klorbensen, och även oklorerade kolväten. En vanlig reningsmetod är att tvätta den flera gånger med conc H2SO4, sedan med vattenhaltigt NaHCO3 eller Na2CO3 och vatten, följt av torkning med CaCl2, K2CO3 eller CaSO4, sedan med P2O5 och destillering. Den kan också torkas med Linde 4A-molekylsikt. Passage genom och lagring över aktiverad aluminiumoxid har använts för att erhålla material med låg konduktivitet.
Inkompatibiliteter
Reagerar våldsamt med starka oxidationsmedel;dimetylsulfoxid; natriumpulver; silverperklorat;orsakar brand- och explosionsrisk. Angriper vissa plaster,gummi och beläggningar. Nedbryts vid upphettning och ger upphov till fosgen- och vätekloridångor.
Avfallshantering
Förbränning, helst efter blandning med ett annat brännbart bränsle; försiktighet måste iakttas för att säkerställa fullständig förbränning för att förhindra bildning av fosgen; en syraskrubber är nödvändig för att avlägsna de halosyror som bildas.
