


Com a terapia anti-VEGF pacientes com degeneração macular relacionada com a idade neovascular, tipicamente têm melhorias significativas na acuidade visual e na qualidade de vida. Embora os resultados a curto prazo sejam nada menos que espetaculares, persistem várias questões importantes relativas ao tratamento destes pacientes a longo prazo. Elas incluem:
- Qual é o melhor agente?
- Quantas vezes se deve tratar?
- A dosagem a longo prazo destes agentes causa perda de visão e danos?
- Existem novas plataformas no horizonte para a administração destes agentes a longo prazo?
- Este artigo responde a estas questões com base em resultados de ensaios clínicos cruciais.
Todos os agentes anti-VEGF são iguais? Com que frequência devemos tratar?
Em 2006, os estudos de referência ANCHOR e MARINA demonstraram a eficácia e segurança do ranibizumabe mensal (Lucentis, Roche/Genentech) com dosagem mensal. Os pacientes ganharam 10,7 e 6,6 letras, respectivamente, aos dois anos.1-2 Posteriormente, os estudos paralelos VIEW1 e VIEW2 mostraram melhora média na visão aos dois anos com aflibercept (Eylea, Regeneron Pharmaceuticals) q8 semanas após três doses iniciais de carga mensal.3
Os estudos subseqüentes nos permitiram avaliar a eficácia desses medicamentos empregando intervalos de dosagem menos freqüentes, incluindo regimes trimestrais, pro re nata (PRN) e treat-and-extend. O estudo PIER examinou a dosagem trimestral com ranibizumabe após três doses mensais de carga e, embora superior à observação, os pacientes PIER perderam 2,3 letras da linha de base a um ano.4
Uma das primeiras exceções foi o PrONTO, um estudo de Fase I/II que avaliou 40 pacientes em dois anos com monitorização mensal e retratamento PRN baseado em parâmetros de acuidade visual, exame clínico e tomografia de coerência óptica.5 Os resultados da acuidade visual aproximaram-se dos de ANCHOR e MARINA com quase metade do número de injeções, mas o estudo careceu de um braço de controle de tratamento mensal. Estes resultados não foram duplicados nos ensaios PRN subsequentes.
O ensaio HARBOR comparou a dosagem mensal e PRN do ranibizumabe. O grupo mensal de 0,5-mg ganhou 9,1 letras a 24 meses vs. 7,9 letras para o grupo PRN. Enquanto esta diferença não foi estatisticamente significativa, o número mediano de injeções (mas não o número de visitas) foi reduzido de 21,4 para 13,3,6
CATT e IVAN foram estudos similares que compararam a dosagem mensal e PRN de ranibizumabe e bevacizumabe fora do rótulo (Avastin, Roche/Genentech). Em dois anos, verificou-se que a dosagem de PRN era não-inferior ao tratamento mensal em ambos os estudos (exceto para PRN bevacizumab no CATT), embora houvesse uma tendência para melhor visão nos grupos mensais.7,8
TREX comparou o ranibizumab mensal com um regime de tratamento e extensão (T&E).9 Mais uma vez, a diferença de acuidade visual não foi estatisticamente significativa (10,5 no grupo mensal e 8,7 no grupo T&E), mas tendeu para uma melhor visão no grupo mensal. O número médio de injeções foi de 25,5 vs. 18,6 ao longo de dois anos. Além disso, nenhum paciente do grupo mensal perdeu mais de 2 letras, enquanto cinco pacientes do grupo T&E perderam pelo menos 3 linhas de visão.
Embora estes estudos tenham mostrado resultados estatisticamente semelhantes com a dosagem mensal a curto prazo, os resultados absolutos dos dados têm sido quase unanimemente superiores com a dosagem mensal de agentes anti-VEGF.
O que acontece após dois anos?
Os dados após dois anos destes estudos clínicos não são tão fáceis de interpretar e aplicar como os dados do estudo clínico, principalmente porque estes estudos de extensão avaliaram principalmente a segurança dos medicamentos a longo prazo. Portanto, o acompanhamento e os cronogramas de tratamento não foram tão rigorosos.

HORIZON foi o estudo de extensão para pacientes nos ensaios MARINA, ANCHOR e FOCUS. Estes pacientes não seguiram um protocolo; eles receberam tratamento a critério dos investigadores durante as visitas de avaliação a cada três a seis meses. Aos quatro anos, os pacientes de HORIZON perderam essencialmente os ganhos iniciais de VA e regressaram à visão de base (-0,1 letras).10 Uma análise mais detalhada dos dados encontrou uma associação entre melhor visão e mais injeções.
O estudo CATT de cinco anos avaliou pacientes monitorados e tratados a critério dos investigadores após os dois primeiros anos do estudo. Em média, os pacientes perderam 3 letras em comparação com a visão de base. Os pacientes foram vistos uma média de oito vezes por ano e receberam uma média de cinco tratamentos por ano.11 Algumas discussões surgiram sobre se a perda de visão era devida a subtratamento ou ao desenvolvimento de atrofia macular, mas o estudo não foi capaz de provocar essa diferença.12
O estudo de extensão VIEW 1 monitorou pacientes com mais rigor. Os participantes receberam a dosagem de intervalo fixo > dose de 8 semanas, mas eles poderiam receber tratamentos mais frequentes se atendessem aos critérios pré-estabelecidos. Nesta extensão, os pacientes retiveram uma visão muito melhor, com uma visão média de ganho de 7,1 letras a partir da linha de base (comparado com um ganho de 10,4 letras no ponto final primário de um ano).13
O que acontece a longo prazo e a frequência de dosagem é importante?

Os melhores dados a longo prazo que temos são de estudos observacionais. O Estudo SEVEN-UP foi uma extensão dos ensaios de ranibizumab. Embora não houvesse um cronograma de visitas ou protocolo de injeção pré-estabelecido, os dados fornecem algumas informações. Aos sete anos, os pacientes perderam em média 8,6 cartas da linha de base. Os pacientes que não receberam injeções nos três anos seguintes perderam 8,7 letras da linha de base; aqueles que receberam de uma a cinco injeções perderam 10,8 letras; aqueles que receberam de seis a 10 injeções perderam 6,9 letras; e aqueles que receberam mais de 11 injeções ganharam 3,9 letras da linha de base.14
O Grupo de Estudo Fight Retinal Blindness Study da Austrália observou pacientes tratados com anti-VEGF por sete anos. Estes pacientes perderam uma média de 2,6 letras da linha de base, tendo recebido uma média de cinco injeções por ano após o ano dois, quando tinham ganho 4 letras da linha de base.15
Finalmente, o estudo FIDO foi um estudo observacional de um único centro, usando dose fixa de 4 semanas para os dois primeiros anos e >q8 semanas depois disso. Estes pacientes ganharam 12,1 letras da linha de base (de um pico de 16,1 letras em dois anos) com uma média de 10,5 injeções por ano.16
A mensagem central destes estudos observacionais de longo prazo é que claramente, em média, mais injeções traduzidas em melhor visão.

Temos agora dados de 10 anos
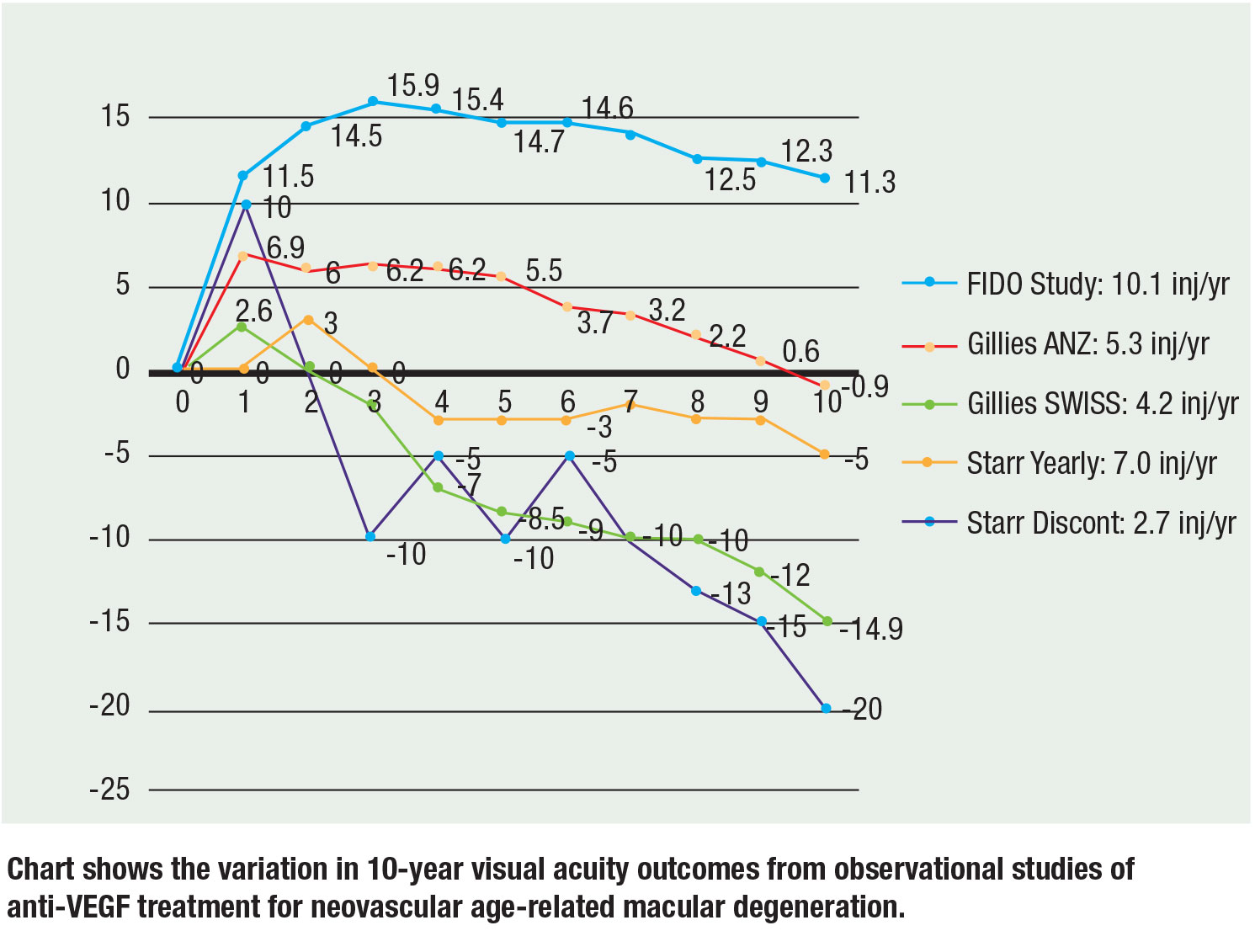
Recentemente, três grandes estudos observacionais relataram dados de 10 anos e os resultados permanecem consistentes: Mais injecções traduzem-se numa melhor acuidade visual. Mark Gillies, MD, e colegas reportaram dados observacionais da Austrália-Nova Zelândia e Suíça. Nos pacientes da ANZ, a visão média diminuiu 0,9 letras desde a linha de base aos 10 anos, com uma mediana de 5,3 injecções/ano num regime T&E em comparação com os pacientes suíços, cuja visão diminuiu em média 14,9 letras com uma mediana de 4,2 injecções por ano em PRN. A conclusão deles foi que o tratamento contínuo e mais injeções alcançaram melhor visão.17
Matthew Starr, MD, e colegas avaliaram uma coorte que incluiu pacientes que tiveram pelo menos duas injeções. Em média, os pacientes receberam de cinco a sete injeções por ano. Olhos que receberam pelo menos uma injeção por ano perderam aproximadamente 7 letras da linha de base, enquanto olhos que não receberam pelo menos uma injeção anual perderam 15 letras da linha de base.18
A nossa coorte FIDO de 10 anos alcançou um aumento médio na visão de 11,3 letras de um pico de 15,9 com uma média de 10,1 injeções por ano durante o período de estudo.19
É importante notar que existem riscos inerentes com comparações entre os julgamentos, dadas as diferentes acuidades visuais iniciais e populações de pacientes, mas as inclinações e tendências se prendem à correlação de mais injeções com melhor visão. A figura (página 29) resume os dados de 10 anos dos três ensaios.
O tratamento frequente resulta na progressão para a atrofia geográfica?
A preocupação da progressão da atrofia geográfica com o tratamento anti-VEGF tem sido uma preocupação e uma razão frequentemente invocada para não se tratar frequentemente. Algumas evidências sugerem que o risco de perda da visão por subtratamento supera de longe esta preocupação potencial. O ensaio SEVEN-UP mostrou maior incidência de AG em olhos semelhantes do que em olhos tratados com o anti-VEGF.14
Outras vezes, os dados de 10 anos da FIDO demonstraram uma incidência ligeiramente menor de AG com perda de visão aos 10 anos nos olhos tratados em comparação com os olhos não tratados (15 vs. 19 por cento).19 É provável que a progressão da GA verdadeira seja independente de
tratamento anti-VEGF, e o que se observa é o ressecamento do complexo neovascular que se parece com GA mas com um impacto menos desgastante na visão.
Bottom Line
Tratamento contínuo e regular com agentes anti-VEGF proporciona resultados excepcionais no tratamento da DMRI úmida. Os dados a longo prazo demonstram que o risco de perda de visão é maior devido ao subtratamento do que devido ao tratamento contínuo em intervalos regulares, como atualmente aplicado em regimes de dosagem de intervalo fixo ou conservadores de tratamento e extensão. Plataformas de entrega a longo prazo, como o sistema de entrega ao domicílio e a terapia genética, parecem promissoras na diminuição das barreiras da não conformidade, da carga de visitas frequentes e dos desafios das exigências de dosagem individual variável. RS
1. Brown DM, Kaiser PK, Michels M, et al. Ranibizumab versus verteporfin para degeneração macular relacionada à idade neovascular. N Engl J Med. 2006;355:1432-1444.
2. Rosenfeld PJ, Brown DM, Heier JS, et al. MARINA Study Group, Ranibizumab for neovascular age related macular degeneration. N Engl J Med. 2006;355:1419-1431.
3. Schmidt-Erfurth U, Kaiser PK, Korobelnik JF, et al. Intravitreal aflibercept injection for neovascular age-related macular degeneration: noventa e seis semanas de resultados dos estudos VIEW. Oftalmologia. 2014;121:193-201.
5. Lalwani GA, Rosenfeld PJ, Fung AE, et al. Um regime de dose variável com ranibizumabe intravitreal para degeneração macular relacionada à idade neovascular: ano 2 do Estudo PrONTO. Am J Ophthalmol. 2009;148:43-58.
6. Ho AC, Busbee BG, Regillo CD, et al, para o Grupo de Estudo HARBOR. Vinte e quatro meses de eficácia e segurança de 0,5 ou 2,0 mg de ranibizumabe em pacientes com degeneração macular subfoveal relacionada à idade neovascular. Oftalmologia. 2014;121:2181-2192.
7. Martin DF, Maguire MG, Fine SL, et al, para o Grupo de Pesquisa Comparação de Ensaios de Degeneração Macular Relacionados à Idade (CATT). Ranibizumab e bevacizumab para o tratamento da degeneração macular neovascular relacionada à idade: resultados de dois anos. Oftalmologia. 2012;119:1388-1398.
8. Chakravarthy U, Harding SP, Rogers CA, et al. Tratamentos alternativos para inibir o VEGF na neovascularização coróide relacionada à idade: resultados de 2 anos do ensaio de controle aleatório IVAN. Lanceta. 2013;382:1258-1267.
9. Wykoff CC, Ou WC, Brown DM, et al. Randomized trial of treat-and-extend versus monthly dosing for neovascular-related age related macular degeneration: 2-year results of the TREX-AMD study. Retina Ophthalmol. 2017;1:314-321.
10. Singer MA, Awh CC, Sadda S, et al. HORIZON: Um ensaio de extensão de ranibizumab com rótulo aberto para a neovascularização coróide secundária à degeneração macular relacionada à idade. Oftalmologia. 2012;119:1175-1183.
11. Maguire MG, Martin DF, Ying GS, et al. Resultados de cinco anos com tratamento anti-vascular endotelial do fator de crescimento da degeneração macular relacionada à idade: A comparação dos ensaios de tratamento da degeneração macular relacionada com a idade. Oftalmologia. 2016;123:1751-1761.
12. Grunwald JE, Pistilli M, Ying GS, et al. Crescimento da atrofia geográfica na comparação de ensaios de tratamentos de degeneração macular relacionada com a idade. Oftalmologia. 2015;122:809-816.
13. Kaiser PK, Singer M, Tolentino M, et al. Long-term safety and visual outcome of intravitreal aflibercept in neovascular age related macular degeneration. Retina Ophthalmol. 2017;1:304-313.
14. Rofagha S, Bhisitkul RB, Boyer DS, Sadda SR, Zhang K, para o Grupo de Estudo SEVEN-UP. et al. Resultados de sete anos em pacientes tratados com ranibizumab em ANCHOR, MARINA e HORIZON: Um estudo de coorte multicêntrico (SEVEN-UP). Oftalmologia. 2013;120:2292-2299.
15. Gillies MC, Campanha A, Barthelmes D, et al, para o Grupo de Estudo da Retina de Luta contra a Cegueira. Resultados a longo prazo do tratamento da degeneração macular relacionada à idade neovascular: Dados de um estudo observacional. Oftalmologia. 2015;122:1837-1845.
16. Peden MC, Suñer IJ, Hammer ME, Grizzard WS. Desfechos a longo prazo em olhos que recebem dosagem de agentes de fator de crescimento endotelial anti-vascular fixos para degeneração macular relacionada à idade úmida. Oftalmologia. 2015;122:803-808.
17. Gillies M, Arnold J, Bhandari S, et al. Resultados de dez anos de degeneração macular neovascular relacionada à idade de duas regiões. Am J Ophthalmol. 2020;210:116-124.
18. Starr MR, Kung FF, Bui YT, et al. Dez anos de seguimento de pacientes com degeneração macular exsudativa relacionada à idade tratados com injeções intravitreais do fator de crescimento endotelial anti-vascular. Retina. Publicado online em 13 de novembro de 2019.
19. Suñer IJ, Peden MC, Hammer ME, Grizzard WS. Resultados de dez anos em olhos recebendo dosagem de agentes de fator de crescimento endotelial anti-vascular fixos para degeneração macular relacionada à idade úmida. Trabalho apresentado na Retina Society 2019; 12 de setembro de 2019; London, U.K.
20. Campochiaro PA, Marcus DM, Awh CC, et al. The port delivery system with ranibizumab for neovascular age related macular degeneration: results from the randomized phase 2 LADDER clinical trial. Oftalmologia. 2019;126:1141-1154.
21. Ho AC; o Grupo de Estudo Janssen/ORBIT. Programas de entrega de precisão para terapia celular e genética. Trabalho apresentado em: Vail Vitrectomy Meeting; 10 de Fevereiro de 2019; Vail, CO.
22. ADVM-022 terapia gênica para AMD úmida (OPTIC). Patrocinador: Adverum Biotechnologies. ClinicalTrials.gov Identifier: NCT03748784. Disponível em: https://clinicaltrials.gov/ct2/show/NCT03748784. Acesso em: 18 de abril de 2020.
23. RegenxBio relata os resultados financeiros e operacionais do primeiro trimestre de 2019 e uma atualização adicional do ensaio interino da fase I/IIa para o RGX-314 para o tratamento de AMD úmida. Rockville, MD; 7 de maio de 2019. https://www.prnewswire.com/news-releases/regenxbio-reports-first-quarter-2019-financial-and-operating-results-and-additional-positive-interim-phase-iiia-trial-update-for-rgx-314-for-the-treatment-of-wet-amd-300845423.html Acessado em 9 de julho de 2020.
