O termo estereoquímico diastereotópico refere-se à relação entre dois grupos numa molécula que, se substituída, geraria compostos que são diastereómeros. Grupos diastereotópicos são frequentemente, mas nem sempre, grupos idênticos ligados ao mesmo átomo numa molécula contendo pelo menos um centro quiral.
Por exemplo, os dois átomos de hidrogénio da fracção CH2 em (S)-2-bromobutano são diastereotópicos. A substituição de um átomo de hidrogênio (azul colorido) por um átomo de bromo irá produzir (2S,3R)-2,3-dibromobutano. A substituição do outro átomo de hidrogênio (vermelho) por um átomo de bromo produzirá o diastereômero (2S,3S)-2,3-dibromobutano.
 |
 |
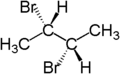 |
| (S)-2-bromobutano | (2S,3R)-2,3-dibromobutane | (2S,3S)-2,3-dibromobutano |
Em moléculas quirais contendo grupos diastereotopicos, como no 2-bromobutano, não há necessidade de pureza enantiomérica ou óptica; não importa sua proporção, cada enantiômero gerará conjuntos enantioméricos de diastereômeros na substituição de grupos diastereotópicos (embora, como no caso da substituição por bromo no 2-bromobutano, os meso isômeros não possuem, a rigor, nenhum enantiômero).
Grupos diastereotópicos não são imagens de espelho uns dos outros sobre qualquer plano. Eles são sempre diferentes, em qualquer ambiente, mas podem não ser distinguíveis. Por exemplo, ambos os pares de hidrogênios CH2 em cloridrato de etil fenilalaninato (PhCH2CH(NH3+)COOCH2CH3 Cl-) são diastereotópicos e ambos dão pares de sinais distintos de 1H-NMR em DMSO-d6 a 300 MHz, mas no grupo similar de etil 2-nitrobutanoato (CH3CH2CH(NO2)COOCH2CH3), somente o grupo CH2 próximo ao centro quiral dá sinais distintos de seus dois hidrogênios com o mesmo instrumento em CDCl3. Tais sinais são frequentemente complexos devido a pequenas diferenças no deslocamento químico, sobreposição e um forte acoplamento adicional entre os hidrogênios geminais. Por outro lado, os dois grupos CH3 de ipsenol, que estão a três ligações do centro quiral, dão duplos 1H separados a 300 MHz e sinais 13C-NMR separados no CDCl3, mas os hidrogénios diasterotópicos em cloridrato de alaninato de etilo (CH3CH(NH3+)COOCH2CH3 Cl-), também a três ligações do centro quiral, mostram sinais 1H-NMR pouco distinguíveis em DMSO-d6.

Grupos distereotópicos também surgem em moléculas achirais. Por exemplo, qualquer par de hidrogênios CH2 em 3-pentanol (Figura 1) são diastereotópicos, já que os dois carbonos CH2 são enantiotópicos. A substituição de qualquer um dos quatro hidrogênios CH2 cria dois centros quirais ao mesmo tempo, e os dois possíveis produtos de substituição de hidrogênio em qualquer um dos carbonos CH2 serão diastereômeros. Este tipo de relação é muitas vezes mais fácil de detectar em moléculas cíclicas. Por exemplo, qualquer par de hidrogênio CH2 no ciclopentanol (Figura 2) é similarmente diastereotópico, e isso é facilmente discernido como um dos hidrogênios do par será cis para o grupo OH (no mesmo lado da face do anel) enquanto o outro será trans para ele (no lado oposto).
O termo diastereotópico é também aplicado a grupos idênticos ligados à mesma extremidade de um grupo alcalino que, se substituído, geraria isómeros geométricos (também pertencentes à categoria de diastereómeros). Assim, os hidrogênios CH2 do propeno são diastereotópicos, sendo um cis para o grupo CH3, e o outro trans para ele, e a substituição de um ou outro por CH3 geraria cis ou trans-2-buteno.

A diastereotopicidade não está limitada a moléculas orgânicas, nem a grupos ligados ao carbono, nem a moléculas com centros quirais tetraédricos (sp3-hibridizados): por exemplo, o par de hidrogênios em qualquer grupo CH2 ou NH2 no íon tris(etilenodiamina)cromo(III) (Cr(en)33+), onde o centro metálico é quiral, são diastereotópicos (Figura 2).
Os termos enantiotópico e diastereotópico também podem ser aplicados às faces de grupos planares (especialmente grupos carbonílicos e alcenos). Ver regra de prioridade de Cahn-Ingold-Prelog.
