La sindrome da delirio eccitato è una presentazione comune ma poco caratterizzata in ED con un’ampia diagnosi differenziale. I pazienti sono spesso identificati inizialmente dalle forze dell’ordine, ma i tentativi di controllare gli individui che sperimentano l’ExDS tramite costrizioni fisiche, chimiche o elettriche sono associati a un tasso estremamente elevato di morbilità e mortalità.
Caso
Un uomo di 25 anni si presenta all’ED portato da EMS per stato mentale alterato (AMS). Prima dell’arrivo, i paramedici forniscono un rapporto radio che afferma che il paziente è stato trovato agitato, comportandosi in modo aggressivo, e poi è salito sul cofano dell’ambulanza. È stato notato che era estremamente forte e difficile da trattenere. I paramedici hanno somministrato 5 mg di midazolam per via intramuscolare e sono stati in grado di trattenerlo fisicamente, ma all’arrivo rimane estremamente agitato, urlando e sbattendosi contro le barre laterali della barella. Non risponde a nessuna domanda e il suo discorso non ha senso. All’esame, il paziente è marcatamente tremolante, caldo al tatto, con scatti mioclonici e bruxismo. Si notano estese abrasioni superficiali sull’addome, sul torace e sulle estremità. È troppo agitato per ottenere i segni vitali iniziali. Quali sono i tuoi prossimi passi?
Background
La sindrome da delirio eccitato (ExDS) è una presentazione comune ma scarsamente caratterizzata del DE con un’ampia diagnosi differenziale. Descritta in letteratura da più di 100 anni,1 si ipotizza che coinvolga un eccesso catecolaminergico con catecolamine endogene legate allo stress, farmaci catecolaminergici esogeni,2 e/o una sovrastimolazione dei recettori della dopamina e del glutammato NMDA nel contesto di una malattia psichiatrica o medica organica. Le cause possono essere raggruppate a grandi linee in eziologie metaboliche/endocrine, neurologiche, infettive, tossicologiche e psichiatriche (Tabella 1).
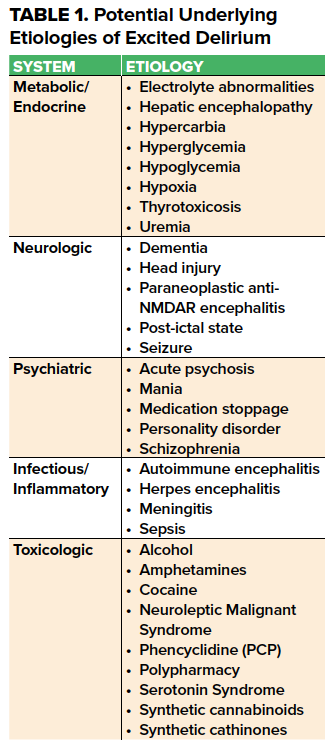
La più comune tra queste è la presenza concomitante di intossicazione acuta da farmaci, in particolare simpaticomimetici, e storia di malattia mentale con caratteristiche psicotiche. L’incidenza dell’ExDS varia ampiamente, con un aumento dell’incidenza negli anni ‘803 legato all’aumento dell’uso di cocaina,4 anfetamine e fenciclidina. Recentemente, sono stati implicati i catinoni sintetici e i cannabinoidi.5,6
I pazienti sono spesso identificati inizialmente dalle forze dell’ordine. Gli interventi delle forze dell’ordine per controllare gli individui affetti da ExDS tramite costrizioni fisiche, chimiche o elettriche sono associati a un tasso estremamente elevato di morbilità e mortalità; l’ExDS è implicato in più del 3% degli interventi della polizia che comportano l’uso della forza, è associato a più del 10% dei decessi in custodia della polizia e tra il 38% e l’86% della mortalità legata all’ExDS si è verificata in custodia della polizia, in particolare associata a metodi di coercizione della polizia e/o asfissia posizionale.2
Di per sé, l’ExDS comporta un rischio di mortalità estremamente elevato, con circa 2/3 dei pazienti con ExDS che muoiono nel contesto pre-ospedaliero7 in assenza di qualsiasi trauma maggiore, costrizione fisica o intervento della polizia. La mortalità è più fortemente associata alla depressione respiratoria, all’ipertermia grave, all’acidemia o a una combinazione di queste.8 Di queste, l’ipertermia profonda ha la più forte associazione con la mortalità:9 le temperature estreme possono alterare la permeabilità della barriera emato-encefalica, contribuire al malfunzionamento o alla degradazione delle proteine e potenziare la neurotossicità indotta dal glutammato.10
Diagnosi differenziale
Ad oggi, non esiste una definizione universalmente riconosciuta di ExDS. La descrizione iniziale si è sviluppata dall’identificazione post mortem basata sull’anamnesi ed era un termine comprensivo usato in molte impostazioni mediche e legali. In un libro bianco del 2009, l’American College of Emergency Physicians ha descritto l’ExDS come un sottoinsieme dell’AMS e ha raccomandato che nonostante la vaghezza dell’entità clinica, le caratteristiche salienti della storia dovrebbero essere combinate con la diagnosi differenziale per le cause comuni di AMS per descrivere la presentazione. L’ExDS è stata descritta come “una sindrome dall’eziologia incerta caratterizzata da delirio, agitazione e disfunzione autonomica iperadrenergica”, con “sintomi caratteristici di comportamento bizzarro e aggressivo, urla, paranoia, panico, violenza verso gli altri, forza fisica inaspettata e ipertermia”.1 I pazienti con ExDS presentano tipicamente una qualsiasi combinazione di agitazione, elevata tolleranza al dolore, tachipnea e diaforesi; questi pazienti hanno una propensione a sviluppare una grave acidemia con progressione verso l’arresto cardiaco improvviso.11 Le caratteristiche comuni della sindrome e l’ampia sovrapposizione con altre condizioni richiedono l’indagine di altre eziologie sottostanti, come indicato nella Tabella 1.
Gestione
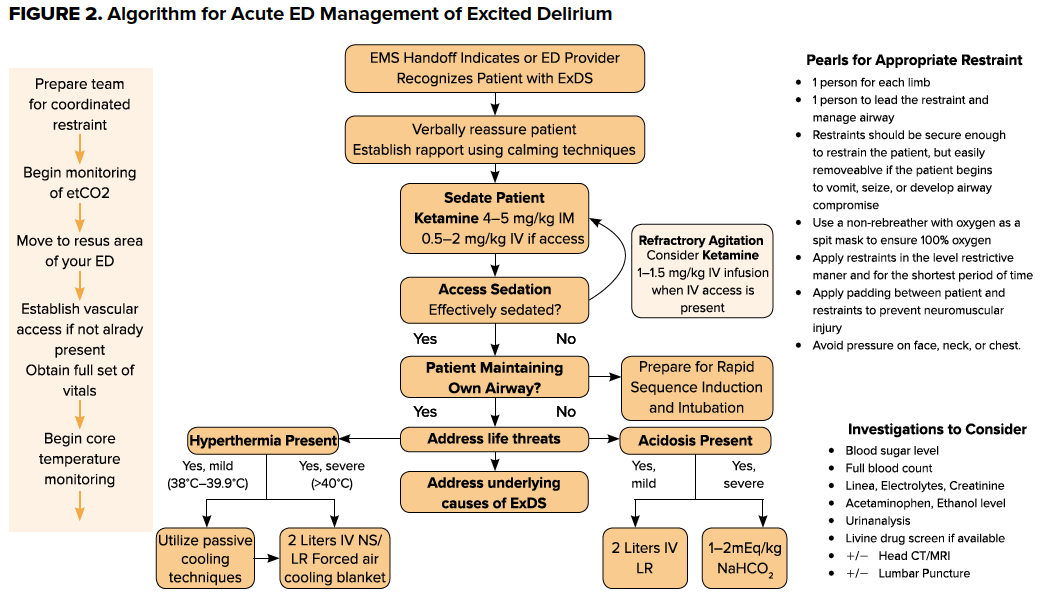
La gestione è adattata alla presentazione del paziente e dovrebbe essere incentrata su 4 pilastri della cura basata sull’evidenza: controllo dell’agitazione, correzione dell’ipertermia, evitare l’acidosi e indagine sull’eziologia sottostante (Tabella 1).
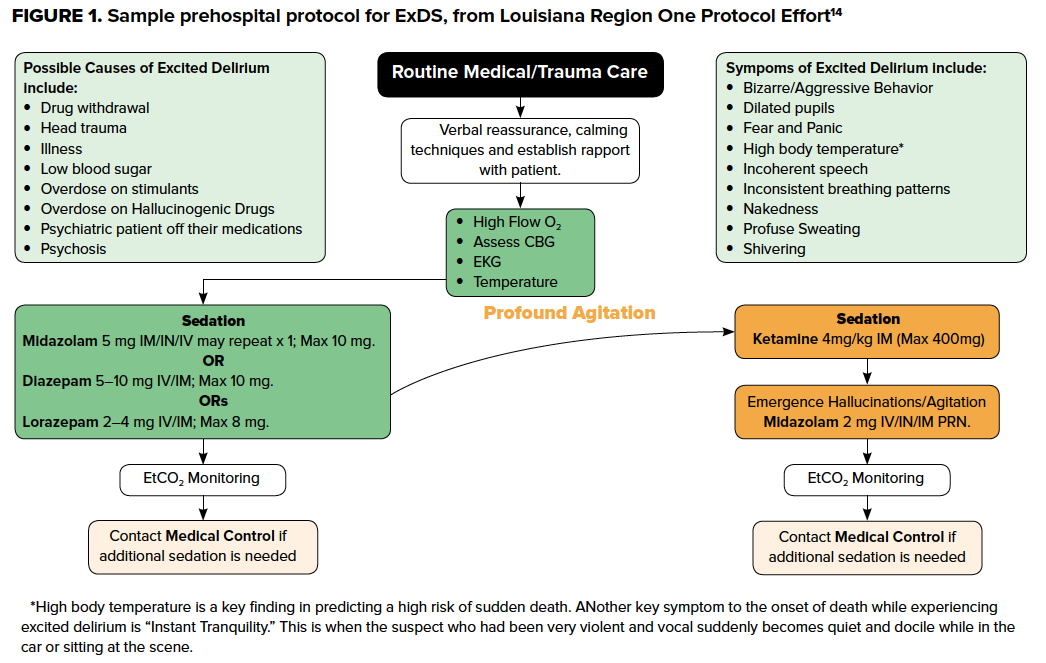
Perché l’asfissia posizionale, la depressione respiratoria, l’ipertermia grave, l’acidosi e/o le aritmie fatali indotte dalla catecolamina12 possono precipitare il collasso cardiovascolare, queste devono essere prevenute e gestite in modo aggressivo. Questi pilastri sono validi sia nell’ambiente pre-ospedaliero che nell’ED, poiché un rapido riconoscimento e un trattamento deliberato e appropriato da parte degli operatori pre-ospedalieri possono ridurre i danni e prevenire esiti negativi. Molte agenzie EMS hanno protocolli specifici per affrontare l’ExDS, spesso enfatizzando il primato del posizionamento sicuro e la rapida sedazione con benzodiazepine e/o ketamina. Se non esplicitamente definito nel protocollo, i fornitori pre-ospedalieri dovrebbero dare la priorità a questi approcci nella pratica, riconoscendo che i pazienti ExDS sono, o hanno il potenziale di diventare malati critici molto rapidamente. L’identificazione precoce da parte del personale EMS può attenuare il rischio di morte improvvisa, allertare il personale dell’ED ricevente e assistere gli esaminatori medici nel comprendere meglio la presentazione e identificare la probabilità che il paziente stesse sperimentando l’ExDS.13
Controllo dell’agitazione
Le raccomandazioni di consenso per la gestione farmacologica dell’AMS è di trattare prima l’eziologia sottostante e poi affrontare i sintomi comportamentali. Tuttavia, l’ExDS è caratterizzato da uno stato di agitazione pericolosa che quasi universalmente richiede la sedazione.2 L’agitazione grave può precludere l’accesso alla flebo o le analisi nelle prime fasi dell’incontro con il paziente. Come tale, gli obiettivi iniziali nel paziente indifferenziato con ExDS dovrebbero essere quelli di fornire rapidamente ed efficacemente la sedazione mentre si trattiene il paziente in una posizione sicura. A seguito di molti decessi in ospedale di pazienti sottoposti a contenzione, la Joint Commission e molte politiche ospedaliere elaborano requisiti specifici per una contenzione fisica sicura. Questi includono una frequente rivalutazione faccia a faccia con l’operatore della necessità della contenzione per ridurre al minimo il tempo di contenzione meccanica. I principi importanti quando si immobilizza un paziente includono l’evitare la pressione su viso, collo e petto, che porterebbe all’asfissia, all’acidosi respiratoria o metabolica e alla morte. Allo stesso modo, l’ExDS può essere secondario all’ipossia, ed è preferibile posizionare un non-rebreather con ossigeno al 100%, che funge anche da maschera di sputo. Inoltre, è spesso necessario utilizzare 4 o 5 punti di immobilizzazione, ponendo il paziente in posizione supina con la testa del letto sollevata a 30° mentre si immobilizza un braccio del paziente sopra la testa e l’altro sotto la vita.
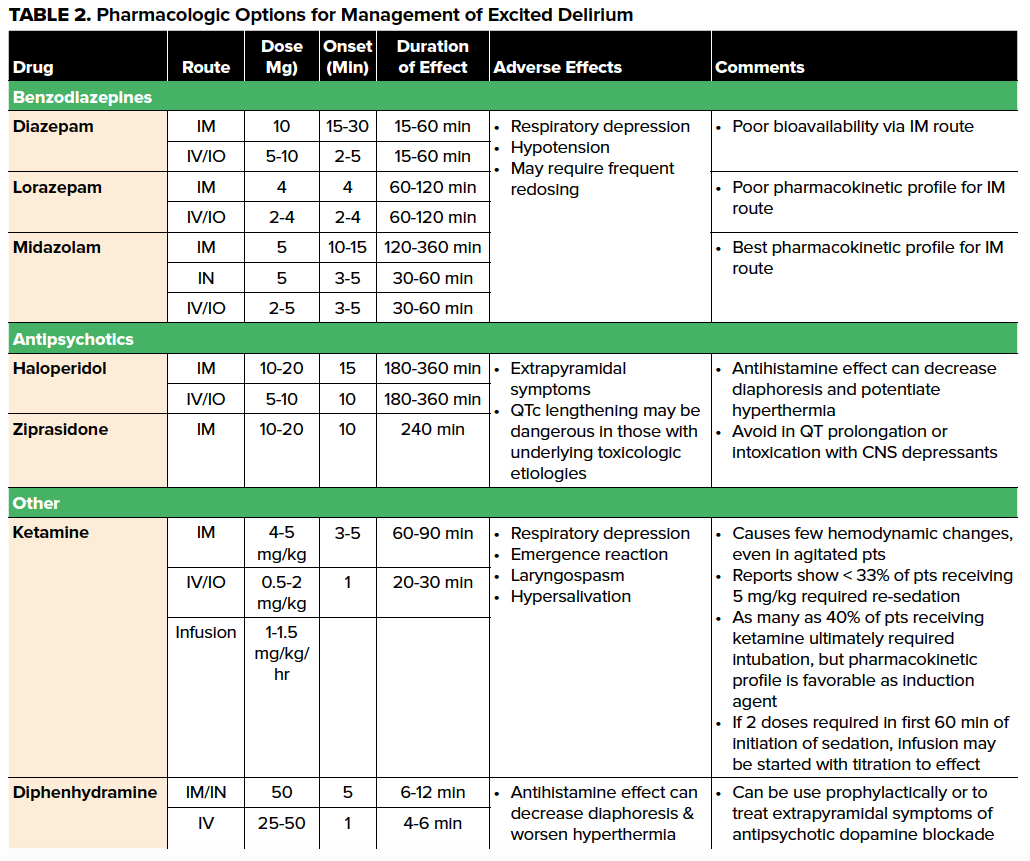
Mentre i pilastri tradizionali per la gestione farmacologica dell’agitazione includono benzodiazepine (in particolare lorazepam e midazolam), antistaminici come la difenidramina e antipsicotici, ci sono molti svantaggi di questi farmaci nel paziente ExDS (Tabella 2). Poiché la progressione verso il collasso cardiovascolare è maggiormente associata a ipertermia, depressione respiratoria e acidemia, le scelte farmacologiche nella sedazione dei pazienti con ExDS dovrebbero integrare gli sforzi per contrastare queste alterazioni della fisiologia, non peggiorarle. Negli ultimi anni, le carenze nazionali di diazepam e lorazepam per via endovenosa15 , insieme a una preponderanza di prove e alla preferenza degli operatori, hanno incoraggiato l’uso della ketamina per la gestione della sedazione degli ExDS, con intervalli di dosaggio tipici forniti nella Tabella 2. La relativa latitudine nel calcolo e nel percorso del dosaggio, la rapida insorgenza dell’azione e la facilità di progressione dalla sedazione all’induzione e all’intubazione in sequenza ritardata o rapida rendono la ketamina una buona scelta primaria nei pazienti con ExDS con o senza accesso IV.16 Un altro vantaggio della ketamina è il fatto che preserva i riflessi delle vie aeree del paziente, consentendogli di continuare a respirare spontaneamente. Sebbene la maggior parte dei pazienti sedati con ketamina non necessiti di una gestione aggressiva delle vie aeree, l’attenzione alle vie aeree del paziente, così come il monitoraggio della sedazione procedurale, devono essere utilizzati in tutti i pazienti con ExDS trattati con ketamina.
Correzione dell’ipertermia
La gestione dell’ipertermia è un principio importante della gestione dell’ExDS e dovrebbe essere iniziata immediatamente dopo il controllo dell’agitazione. La gestione della temperatura nell’ExDS è simile a quella dell’ipertermia ambientale e può includere la rimozione degli indumenti, il raffreddamento esterno passivo, sistemi di coperte di raffreddamento ad aria forzata e fluidi freddi per via endovenosa.
Evitare l’acidosi
Evitare qualsiasi acidosi è importante e può essere secondaria a una varietà di eziologie, tra cui ipoperfusione, rabdomiolisi e depressione respiratoria. Come parte del workup iniziale, i gas sanguigni venosi o arteriosi dovrebbero essere ottenuti per valutare gli squilibri acido/base sottostanti. La gestione deve essere mirata alla patologia sottostante e può includere la rianimazione con liquidi per via endovenosa o il supporto respiratorio. Nel caso di un paziente ExDS gestito con la sedazione, compresa la ketamina, è necessario il monitoraggio della CO2 end-tidal (etCO2) per monitorare la frequenza, la profondità e l’adeguatezza della respirazione.
Indagine sull’eziologia sottostante
Dopo che il paziente è stato stabilizzato e sedato, il workup deve essere guidato dall’esame fisico e dall’anamnesi. Un esame fisico completo è fondamentale: i pazienti con ExDS possono avere lesioni sottostanti significative, e gli sforzi per immobilizzare il paziente possono esacerbare qualsiasi trauma preesistente. Le indagini iniziali dovrebbero includere la glicemia, l’emocromo, il BMP e gli screening tossicologici per qualsiasi co-ingestante. Considerare la CPK se si sospetta una rabdomiolisi, le emocolture e/o la puntura lombare se si teme una sepsi e/o una meningite settica. L’imaging può essere perseguito per indagare qualsiasi potenziale trauma sottostante.
Conclusione del caso
Dopo il trasferimento sulla barella dell’ED, il paziente è stato messo in restrizioni morbide a 4 punti con un non respiratore e ossigeno al 100% con l’assistenza della sicurezza dell’ospedale; sono stati somministrati 5 mg/kg di ketamina IM, con significativa riduzione dell’agitazione. Il paziente è stato messo sotto etCO2 e portato nella sala di rianimazione per un attento monitoraggio. È stato trovato tachicardico con un polso di 150, iperteso a 150/94, ipertermico a 39,6° C. L’end-tidal mostrava 38mmHg di CO2 e 20 respirazioni/minuto. Gli esami non hanno rivelato anomalie. Impacchi freddi sono stati posizionati all’ascella e all’inguine, e 2 L di ringer raffreddati sono stati somministrati IV con miglioramento della temperatura.
In base all’esame fisico e all’anamnesi, la preoccupazione era per un delirio eccitato secondario a un agente simpaticomimetico sconosciuto con qualità allucinogene, e il paziente è stato ammesso allo stepdown dell’ICU con cure di supporto.
Il delirio agitato del paziente si è risolto il giorno 2 dell’ospedale, ed è stato trasferito in psichiatria per l’osservazione continua. È stato dimesso il giorno 4 con rinvio ai servizi psichiatrici e supporto per l’uso di farmaci.
1. Mash D. Delirio eccitato e morte improvvisa: Un disturbo sindromico all’estremità estrema del continuum neuropsichiatrico. Front Physiol. 2016;7:435.
2. Gonin P, Beysard N, Yersin B, Carron PN. Delirio eccitato: una revisione sistematica. Acad Emerg Med. 2018;25(5):552-565.
3. Vilke GM, DeBard ML, Chan TC, et al. Excited Delirium Syndrome (ExDS): definizione basata su una revisione della letteratura. J Emerg Med. 2012;43(5):897-905.
4. Wetli CV, Fishbain DA. Psicosi indotta da cocaina e morte improvvisa nei consumatori ricreativi di cocaina. J Forensic Sci. 1985;30(3):873-880.
5. Atis SE, Yilmaz G, Bozan O, Cekmen B. Una droga terrificante minaccia le strade: Flakka – Un rapporto di caso. J Mol Imag Dynamic. 2018;8(1):142.
6. Prosser JM, Nelson LS. La tossicologia dei sali da bagno: una revisione dei catinoni sintetici. J Med Toxicol. 2012;8(1):33-42.
7. Gottlieb M, Long B, Koyfman A. Approccio al paziente agitato del dipartimento di emergenza. J Emerg Med. 2018;54(4):447-457.
8. Otahbachi M, Cevik C, Bagdure S, Nugent K. Excited delirium, restraints, and unexpected death: a review of pathogenesis. Am J Forensic Med Pathol. 2010;31(2):107-112.
9. Mash DC. Delirio eccitato e morte improvvisa: A Syndromal Disorder at the Extreme End of the Neuropsychiatric Continuum. Front Physiol. 2016;7:435.
10. Plush T, Shakespeare W, Jacobs D, Ladi L, Sethi S, Gasperino J. Delirio agitato indotto da cocaina: un case report e revisione. J Intensive Care Med. 2015;30(1):49-57.
11. DeBard ML, Adler J, Bozeman W, Chan T, et al: ACEP Excited Delirium Task Force. White Paper Report on Excited Delirium Syndrome. 2009.
12. Morte S. BET 1: Sindrome da delirio eccitato e morte improvvisa. Emerg Med J. 2013;30(11):958-960.
13. Vilke GM, Bozeman WP, Dawes DM, Demers G, Wilson MP. Sindrome da delirio eccitato (ExDS): Opzioni di trattamento e considerazioni. J Forensic Leg Med. 2012;19(3):117-121.
14. Città di New Orleans. Region One Protocol Effort. Stato della Louisiana. 2013.
15. Tassey T. Fuori Ativan? La crisi della carenza di farmaci negli Stati Uniti EM Resident. 2016;43(1):28-29.
16. Mankowitz SL, Regenberg P, Kaldan J, Cole JB. Ketamina per la sedazione rapida di pazienti agitati nelle impostazioni pre-ospedaliere e del dipartimento di emergenza: A Systematic Review and Proportional Meta-Analysis. J Emerg Med. 2018;55(5):670-681.
