


Con la terapia anti-VEGF i pazienti con degenerazione maculare senile neovascolare hanno tipicamente miglioramenti significativi nell’acuità visiva e nella qualità della vita. Mentre i risultati a breve termine sono a dir poco spettacolari, persistono diverse domande importanti sulla gestione a lungo termine di questi pazienti. Essi includono:
- Qual è il miglior agente?
- Quanto spesso si dovrebbe trattare?
- Il dosaggio a lungo termine di questi agenti provoca perdita della vista e danni?
- Sono all’orizzonte nuove piattaforme per la somministrazione a lungo termine di questi agenti?
- Questo articolo risponde a queste domande sulla base dei risultati degli studi clinici pivotal.
Gli agenti anti-VEGF sono tutti uguali? Quanto spesso dovremmo trattare?
Nel 2006, gli studi di riferimento ANCHOR e MARINA hanno dimostrato l’efficacia e la sicurezza di ranibizumab (Lucentis, Roche/Genentech) con dosaggio mensile. I pazienti hanno guadagnato 10,7 e 6,6 lettere, rispettivamente, a due anni.1-2 Successivamente, gli studi paralleli VIEW1 e VIEW2 hanno mostrato un miglioramento medio della vista a due anni con aflibercept (Eylea, Regeneron Pharmaceuticals) q8 settimane dopo tre dosi di carico mensili iniziali.3
Gli studi successivi ci hanno permesso di valutare l’efficacia di questi farmaci utilizzando intervalli di dosaggio meno frequenti, tra cui trimestrale, pro re nata (PRN) e treat-and-extend. Lo studio PIER ha esaminato il dosaggio trimestrale con ranibizumab dopo tre dosi di carico mensili e, sebbene superiore all’osservazione, i pazienti PIER hanno perso 2,3 lettere dal basale a un anno.4
Una delle prime eccezioni è stata PrONTO, uno studio di fase I/II che ha valutato 40 pazienti per due anni con monitoraggio mensile e ritrattamento PRN basato su acuità visiva, esame clinico e parametri di tomografia a coerenza ottica.5 I risultati di acuità visiva si sono avvicinati a quelli di ANCHOR e MARINA con quasi la metà del numero di iniezioni, ma lo studio non aveva un braccio di controllo con trattamento mensile. Questi risultati non sono stati duplicati nei successivi studi PRN.
Lo studio HARBOR ha confrontato il dosaggio mensile e PRN di ranibizumab. Il gruppo mensile da 0,5 mg ha guadagnato 9,1 lettere a 24 mesi contro 7,9 lettere per il gruppo PRN. Mentre questa differenza non era statisticamente significativa, il numero mediano di iniezioni (ma non il numero di visite) è stato ridotto da 21,4 a 13,3.6
CATT e IVAN erano studi simili che confrontavano il dosaggio mensile e PRN di ranibizumab e bevacizumab off-label (Avastin, Roche/Genentech). A due anni, il dosaggio PRN è risultato non inferiore al trattamento mensile in entrambi gli studi (tranne che per il bevacizumab PRN nel CATT), anche se c’era una tendenza verso una visione migliore nei gruppi mensili.7,8
TREX ha confrontato ranibizumab mensile con un regime treat-and-extend (T&E).9 Ancora una volta, la differenza di acuità visiva non era statisticamente significativa (10,5 nel gruppo mensile e 8,7 nel gruppo T&E), ma la tendenza era verso una visione migliore nel gruppo mensile. Il numero medio di iniezioni è stato di 25,5 contro 18,6 in due anni. Inoltre, nessun paziente della coorte mensile ha perso più di 2 lettere, mentre cinque pazienti T&E hanno perso almeno 3 linee di visione.
Mentre questi studi hanno mostrato risultati statisticamente simili con il dosaggio mensile a breve termine, i risultati dei dati assoluti sono stati quasi unanimemente superiori con il dosaggio mensile degli agenti anti-VEGF.
Cosa succede dopo due anni?
I dati oltre i due anni di questi studi clinici non sono così facili da interpretare e applicare come i dati degli studi clinici, soprattutto perché questi studi di estensione hanno valutato principalmente la sicurezza del farmaco a lungo termine. Quindi, il follow-up e i programmi di trattamento non erano così rigorosi.

HORIZON era lo studio di estensione per i pazienti degli studi MARINA, ANCHOR e FOCUS. Questi pazienti non hanno seguito un protocollo; hanno ricevuto il trattamento a discrezione degli investigatori durante le visite di valutazione ogni tre o sei mesi. A quattro anni, i pazienti HORIZON hanno essenzialmente perso i guadagni iniziali di VA e sono regrediti alla visione di base (-0,1 lettere).10 Ulteriori analisi dei dati hanno trovato un’associazione tra una migliore visione e più iniezioni.
Lo studio quinquennale CATT ha valutato i pazienti monitorati e trattati a discrezione degli investigatori dopo i primi due anni dello studio. In media, i pazienti hanno perso 3 lettere rispetto alla visione iniziale. I pazienti sono stati visitati in media otto volte all’anno e hanno ricevuto una media di cinque trattamenti all’anno.11 Si è discusso se la perdita della vista fosse dovuta al sottotrattamento o allo sviluppo dell’atrofia maculare, ma lo studio non era alimentato per individuare questa differenza.12
Lo studio di estensione VIEW 1 ha monitorato i pazienti in modo più rigoroso. I partecipanti hanno ricevuto un dosaggio fisso-intervallo >q8-settimana, ma potrebbero ricevere trattamenti più frequenti se soddisfano i criteri prespecificati. In questa estensione, i pazienti hanno mantenuto una visione molto migliore, con un guadagno medio di 7,1 lettere dal basale (rispetto a un guadagno di 10,4 lettere all’endpoint primario di un anno).13
Cosa succede a lungo termine e la frequenza di dosaggio è importante?

I migliori dati a lungo termine che abbiamo sono da studi osservazionali. Lo studio SEVEN-UP era un’estensione degli studi sul ranibizumab. Anche se non c’era un programma di visite prespecificato o un protocollo di iniezione, i dati forniscono alcune informazioni. A sette anni, i pazienti hanno perso in media 8,6 lettere dal basale. I pazienti che non hanno ricevuto iniezioni nei tre anni successivi hanno perso 8,7 lettere dal basale; quelli che hanno ricevuto da una a cinque iniezioni hanno perso 10,8 lettere; quelli che hanno avuto da sei a 10 iniezioni hanno perso 6,9 lettere; e quelli che hanno ricevuto più di 11 iniezioni hanno guadagnato 3,9 lettere dal basale.14
Il Fight Retinal Blindness Study Group dall’Australia ha osservato pazienti trattati con anti-VEGF per sette anni. Questi pazienti hanno perso una media di 2,6 lettere dal basale, avendo ricevuto una media di cinque iniezioni all’anno dopo il secondo anno, quando avevano guadagnato 4 lettere dal basale.15
Infine, lo studio FIDO era uno studio osservazionale monocentrico che utilizzava un dosaggio fisso di q4 settimane per i primi due anni e >q8 settimane dopo. Questi pazienti hanno guadagnato 12,1 lettere dal basale (da un picco di 16,1 lettere a due anni) con una media di 10,5 iniezioni all’anno.16
Il messaggio centrale di questi studi osservazionali a lungo termine è che chiaramente, in media, più iniezioni si traducono in una visione migliore.

Ora abbiamo dati a 10 anni
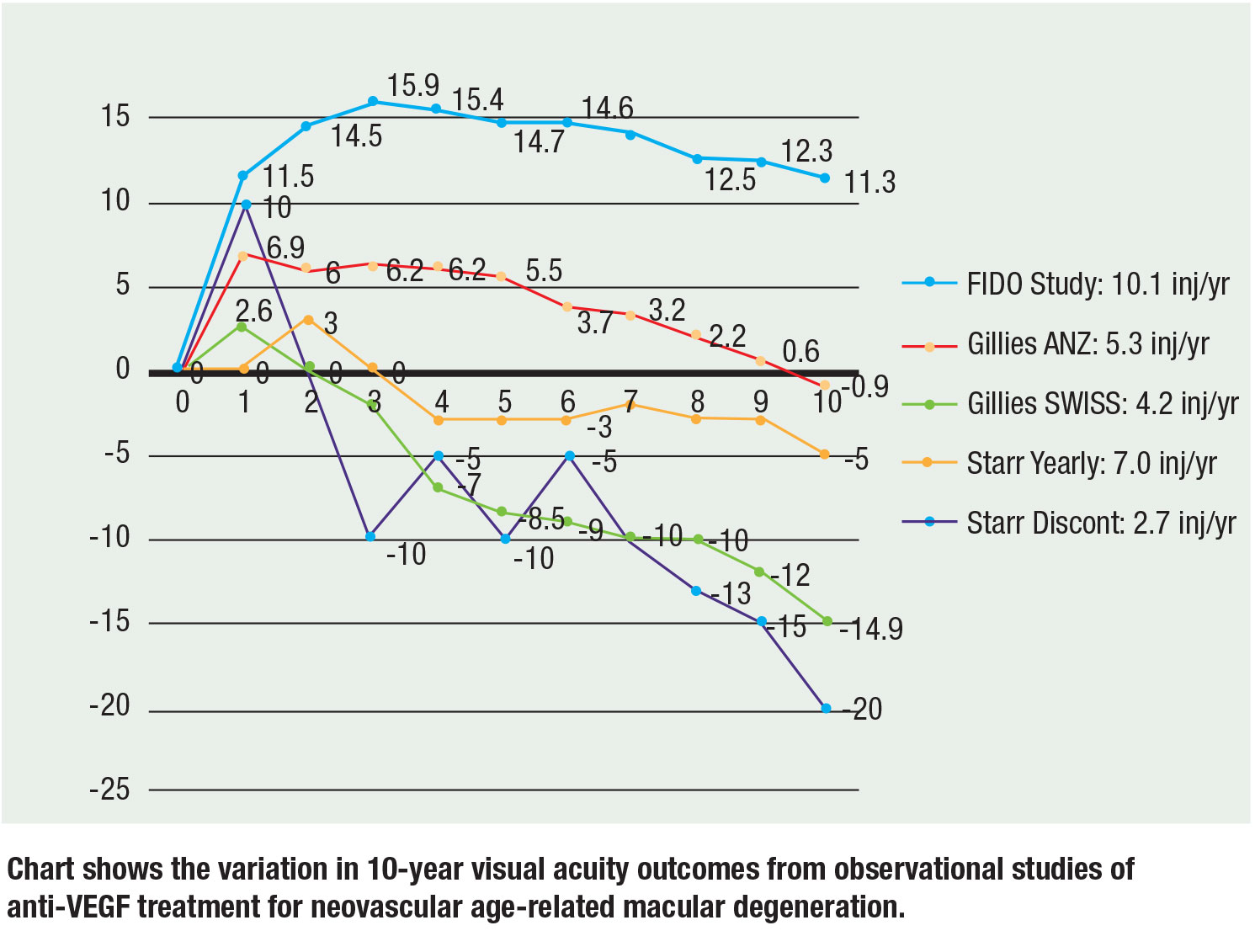
Di recente, tre grandi studi osservazionali hanno riportato dati a 10 anni e i risultati rimangono coerenti: Più iniezioni si traducono in una migliore acuità visiva. Mark Gillies, MD, e colleghi hanno riportato dati osservazionali dall’Australia-Nuova Zelanda e dalla Svizzera. Nei pazienti dell’ANZ, la visione media è diminuita di 0,9 lettere dal basale a 10 anni con una mediana di 5,3 iniezioni/anno su un regime T&E rispetto ai pazienti svizzeri, la cui visione è diminuita di una media di 14,9 lettere con una mediana di 4,2 iniezioni all’anno su PRN. La loro conclusione è stata che il trattamento continuo e più iniezioni hanno ottenuto una visione migliore.17
Matthew Starr, MD, e colleghi hanno valutato una coorte che includeva pazienti che avevano almeno due iniezioni. In media, i pazienti hanno ricevuto da cinque a sette iniezioni all’anno. Gli occhi che hanno ricevuto almeno un’iniezione all’anno hanno perso circa 7 lettere dal basale, mentre gli occhi che non hanno ricevuto almeno un’iniezione all’anno hanno perso 15 lettere dal basale.18
La nostra coorte FIDO di 10 anni ha ottenuto un aumento medio della vista di 11,3 lettere da un picco di 15,9 con una media di 10,1 iniezioni all’anno nel periodo dello studio.19
È importante notare che ci sono rischi intrinseci con i confronti incrociati degli studi, data la diversa acuità visiva iniziale e le popolazioni di pazienti, ma le pendenze e le tendenze confermano la correlazione tra più iniezioni e una migliore visione. La figura (pagina 29) riassume i dati a 10 anni dai tre studi.
Il trattamento frequente porta alla progressione verso l’atrofia geografica?
La preoccupazione della progressione dell’atrofia geografica con il trattamento anti-VEGF è stata una preoccupazione e un motivo frequentemente invocato per non trattare frequentemente. Alcune prove suggeriscono che il rischio di perdita della vista da sottotrattamento supera di gran lunga questa potenziale preoccupazione. Lo studio SEVEN-UP ha mostrato una maggiore incidenza di GA in occhi simili a quelli trattati con anti-VEGF.14
Inoltre, i dati a 10 anni del FIDO hanno dimostrato un’incidenza leggermente inferiore di GA con perdita della vista a 10 anni negli occhi trattati rispetto ai colleghi non trattati (15 contro 19 per cento).19 È probabile che la progressione della vera GA sia indipendente dal
trattamento anti-VEGF, e ciò che si osserva è l’essiccazione del complesso neovascolare che assomiglia alla GA ma con un impatto meno deleterio sulla vista.
Bottom Line
Il trattamento continuo e regolare con agenti anti-VEGF fornisce risultati eccezionali nella gestione della AMD umida. I dati a lungo termine dimostrano che il rischio di perdita della vista è maggiore in caso di sottotrattamento che in caso di trattamento continuo a intervalli regolari, come attualmente applicato nel dosaggio a intervalli fissi o nei regimi conservativi treat-and-extend. Le piattaforme di consegna a lungo termine come il sistema di consegna portuale e la terapia genica sembrano promettenti nel diminuire le barriere della non conformità, l’onere delle visite frequenti e le sfide dei requisiti di dosaggio individuali variabili. RS
1. Brown DM, Kaiser PK, Michels M, et al. Ranibizumab contro verteporfina per la degenerazione maculare senile neovascolare. N Engl J Med. 2006;355:1432-1444.
2. Rosenfeld PJ, Brown DM, Heier JS, et al. MARINA Study Group, Ranibizumab for neovascular age-related macular degeneration. N Engl J Med. 2006;355:1419-1431.
3. Schmidt-Erfurth U, Kaiser PK, Korobelnik JF, et al. Intravitreal aflibercept injection for neovascular age-related macular degeneration: ninety-six-week results of the VIEW studies. Oftalmologia. 2014;121:193-201.
4. Regillo CD, Brown DM, Abraham P, et al. Randomized, double-masked, sham-controlled trial of ranibizumab for neovascular age-related macular degeneration: PIER Studio anno 1. Am J Ophthalmol. 2008;145:239-248.
5. Lalwani GA, Rosenfeld PJ, Fung AE, et al. A variable-dosing regimen with intravitreal ranibizumab for neovascular age-related macular degeneration: year 2 of the PrONTO Study. Am J Ophthalmol. 2009;148:43-58.
6. Ho AC, Busbee BG, Regillo CD, et al, per il gruppo di studio HARBOR. Efficacia e sicurezza a ventiquattro mesi di ranibizumab 0,5 o 2,0 mg in pazienti con degenerazione maculare neovascolare subfoveale legata all’età. Oftalmologia. 2014;121:2181-2192.
7. Martin DF, Maguire MG, Fine SL, et al, per il Comparison of Age-related Macular Degeneration Treatments Trials (CATT) Research Group. Ranibizumab e bevacizumab per il trattamento della degenerazione maculare senile neovascolare: risultati a due anni. Oftalmologia. 2012;119:1388-1398.
8. Chakravarthy U, Harding SP, Rogers CA, et al. Alternative treatments to inhibit VEGF in age-related choroidal neovascularization: 2-year findings of the IVAN randomized control trial. Lancet. 2013;382:1258-1267.
9. Wykoff CC, Ou WC, Brown DM, et al. Studio randomizzato di treat-and-extend versus dosaggio mensile per la degenerazione maculare senile neovascolare: risultati a 2 anni dello studio TREX-AMD. Ophthalmol Retina. 2017;1:314-321.
10. Singer MA, Awh CC, Sadda S, et al. HORIZON: uno studio di estensione in aperto di ranibizumab per la neovascolarizzazione coroideale secondaria alla degenerazione maculare legata all’età. Oftalmologia. 2012;119:1175-1183.
11. Maguire MG, Martin DF, Ying GS, et al. Risultati a cinque anni con il trattamento del fattore di crescita endoteliale anti-vascolare della degenerazione maculare senile neovascolare: Il confronto delle prove di trattamento della degenerazione maculare legata all’età. Oftalmologia. 2016;123:1751-1761.
12. Grunwald JE, Pistilli M, Ying GS, et al. Crescita dell’atrofia geografica nel confronto delle prove di trattamento della degenerazione maculare legata all’età. Oftalmologia. 2015;122:809-816.
13. Kaiser PK, Singer M, Tolentino M, et al. Sicurezza a lungo termine e risultato visivo di aflibercept intravitreale nella degenerazione maculare senile neovascolare. Ophthalmol Retina. 2017;1:304-313.
14. Rofagha S, Bhisitkul RB, Boyer DS, Sadda SR, Zhang K, per il gruppo di studio SEVEN-UP. et al. Seven-year outcomes in ranibizumab-treated patients in ANCHOR, MARINA, and HORIZON: A multicenter cohort study (SEVEN-UP). Oftalmologia. 2013;120:2292-2299.
15. Gillies MC, Campain A, Barthelmes D, et al, per il Fight Retinal Blindness Study Group. Esiti a lungo termine del trattamento della degenerazione maculare senile neovascolare: Dati da uno studio osservazionale. Ophthalmology. 2015;122:1837-1845.
16. Peden MC, Suñer IJ, Hammer ME, Grizzard WS. Esiti a lungo termine negli occhi che ricevono un dosaggio fisso-intervallo di agenti anti-vascular endothelial growth factor per la degenerazione maculare umida legata all’età. Ophthalmology. 2015;122:803-808.
17. Gillies M, Arnold J, Bhandari S, et al. Esiti decennali della degenerazione maculare neovascolare legata all’età da due regioni. Am J Ophthalmol. 2020;210:116-124.
18. Starr MR, Kung FF, Bui YT, et al. Follow-up di dieci anni di pazienti con degenerazione maculare essudativa legata all’età trattati con iniezioni intravitreali anti-vascular endothelial growth factor. Retina. Pubblicato online il 13 novembre 2019.
19. Suñer IJ, Peden MC, Hammer ME, Grizzard WS. Esiti decennali in occhi che ricevono un dosaggio fisso-intervallo di agenti di fattore di crescita endoteliale anti-vascolare per la degenerazione maculare umida legata all’età. Carta presentata alla Retina Society 2019; 12 settembre 2019; Londra, U.K.
20. Campochiaro PA, Marcus DM, Awh CC, et al. Il sistema di consegna del porto con ranibizumab per la degenerazione maculare senile neovascolare: risultati dello studio clinico randomizzato di fase 2 LADDER. Ophthalmology. 2019;126:1141-1154.
21. Ho AC; il gruppo di studio Janssen/ORBIT. Programmi di consegna di precisione per la terapia cellulare e genica. Documento presentato a: Vail Vitrectomy Meeting; 10 febbraio 2019; Vail, CO.
22. Terapia genica ADVM-022 per AMD umida (OPTIC). Sponsor: Adverum Biotechnologies. Identificatore ClinicalTrials.gov: NCT03748784. Disponibile presso: https://clinicaltrials.gov/ct2/show/NCT03748784. Accessed April 18, 2020.
23. RegenxBio riporta i risultati finanziari e operativi del primo trimestre 2019 e un ulteriore aggiornamento positivo della sperimentazione intermedia di fase I/IIa per RGX-314 per il trattamento di AMD umida . Rockville, MD; 7 maggio 2019. https://www.prnewswire.com/news-releases/regenxbio-reports-first-quarter-2019-financial-and-operating-results-and-additional-positive-interim-phase-iiia-trial-update-for-rgx-314-for-the-treatment-of-wet-amd-300845423.html Accesso al 9 luglio 2020.
