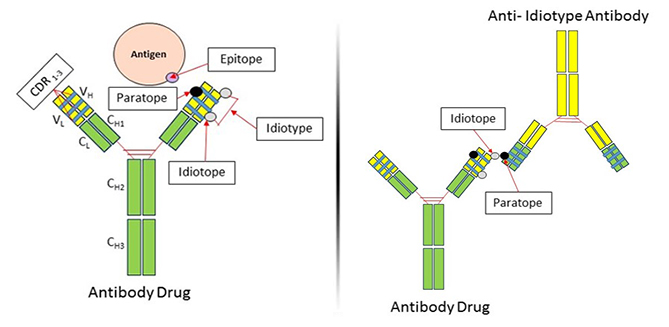
Wie in Abbildung 1 dargestellt, bindet ein anti-idiotypischer (Anti-ID) Antikörper an den Idiotyp eines anderen Antikörpers, in der Regel ein Antikörper-Medikament. Ein Idiotyp kann definiert werden als die spezifische Kombination von Idiotopen, die in den komplementbestimmenden Regionen (CDRs) eines Antikörpers vorhanden sind. Ein einzelnes Idiotop ist eine spezifische Region innerhalb der Fv-Region eines Antikörpers, die an das Paratop (antigene Epitop-Bindungsstelle) eines anderen Antikörpers bindet. Daher kann ein Idiotop fast als Synonym für eine antigene Determinante eines Antikörpers angesehen werden.
|
A: Antikörper-Wirkstoff, der auf ein antigenes Epitop abzielt |
B: Anti-Idiotyp-Antikörper, der auf einen Antikörper-Wirkstoff abzielt |
|---|---|
 |
|
Abbildung 1. Struktur des Anti-Idiotyp-Antikörpers. (A) Das Paratop eines Antikörperwirkstoffs bindet an das Epitop eines Zielantigens innerhalb der CDR-Region des Antikörperwirkstoffs. (B) Das Paratop eines Anti-ID bindet an das Idiotop seines Ziel-Antikörperwirkstoffs. Das Idiotop befindet sich in der CDR-Region des Antikörpermedikaments und kann neben der Antigenbindungsstelle des Antikörpermedikaments liegen, mit dieser identisch sein oder weit davon entfernt sein.
Typen von Anti-Idiotyp-Antikörpern
Es gibt drei Hauptklassifizierungen von Anti-ID-Antikörpern auf Nachweisbasis, wie in Abbildung 2 dargestellt. Der erste ist ein Antigen-blockierender Anti-ID-Antikörper, der so genannt wird, weil sich das Paratop und das Idiotop des zielgerichteten Antikörpers überschneiden. Aus diesem Grund konkurrieren das Zielantigen des Antikörpermedikaments und der Anti-ID-Antikörper miteinander. Daher kann diese Form von Anti-ID-Antikörpern nur den freien Antikörperwirkstoff nachweisen. Die zweite Klassifizierung von Anti-ID-Antikörpern wird als nicht blockierend bezeichnet, weil sich das Paratop und das Idiotop des Antikörpermedikaments nicht überschneiden. Daher können der Anti-ID-Antikörper und das Antigen gleichzeitig an den Antikörperwirkstoff binden, ohne sich gegenseitig in ihrer Bindungsfähigkeit zu beeinträchtigen. Aus diesem Grund werden nicht blockierende Anti-ID-Antikörper zum Nachweis aller Formen des verfügbaren Antikörperwirkstoffs (frei oder antigengebunden) verwendet. Die dritte Klassifizierung von Anti-ID-Antikörpern ist ein komplexer spezifischer Anti-ID. Dies liegt daran, dass der Anti-ID-Antikörper nur dann an den Antikörperwirkstoff binden kann, wenn dieser bereits an sein Antigen gebunden ist. Daher ist diese Art von Anti-ID-Antikörper nur in der Lage, gebundenen Antikörperwirkstoff nachzuweisen.
|
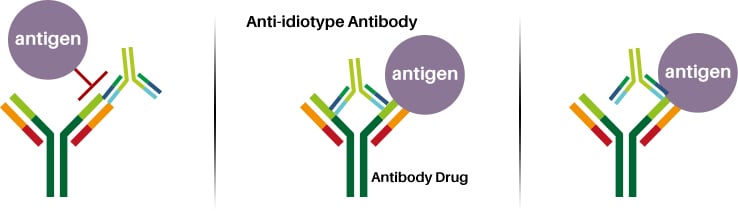
A: Antigen-blockierender Anti-ID-Antikörper |
B: Nicht-blockierender Anti-ID-Antikörper |
C: Komplexer spezifischer Anti-ID-Antikörper |
|---|---|---|
 |
||
|
Paratope-Spezifisch |
Nicht Paratop-spezifisch |
Wirkstoff-Zielkomplex-spezifisch |
Abbildung 2. Arten von Anti-Idiotyp-Antikörpern. (A) Antigenblockierende Anti-IDs binden direkt an die Antigenbindungsstelle eines Antikörperwirkstoffs und konkurrieren so direkt mit dem Zielantigen. (B) Der Idiotyp, an den nicht blockierende Anti-IDs binden, überschneidet sich überhaupt nicht mit dem Paratop des Antikörperwirkstoffs, so dass der Antikörperwirkstoff sein Zielantigen und einen Anti-ID gleichzeitig binden kann. (c) Komplexe spezifische Anti-IDs binden nur dann an das Idiotop eines Antikörperwirkstoffs, wenn dieser bereits an sein entsprechendes Antigen gebunden ist.
Verwendung von Anti-Idiotyp-Antikörpern
Pharmakokinetische Assays
Da die meisten Anti-ID-Antikörper gegen einen spezifischen Antikörperwirkstoff erzeugt werden, werden sie in der präklinischen Praxis häufig für pharmakokinetische (PK) Analysen verwendet. PK ist die Untersuchung des Arzneimittelstoffwechsels im Körper. Insbesondere wollen Kliniker die Geschwindigkeit der Arzneimittelabsorption, -verteilung, -bioverfügbarkeit und -ausscheidung in verschiedenen Patientenkohorten bestimmen. Um dies zu erreichen, müssen die Forscher in der Lage sein, Antikörper-Medikamente zu verfolgen, die zu verschiedenen Zeitpunkten nach der Verabreichung an ihr bestimmtes Ziel gebunden oder ungebunden sind. Durch den Einsatz von Anti-IDs, in erster Linie mAbs, können verschiedene Formen von Antikörpertherapeutika im Serum, Blut, Urin oder anderen Körperflüssigkeiten von Patienten leicht verfolgt und quantifiziert werden. Beispiele für pharmakokinetische Assays (ELISA-Format) mit Anti-IDs sind in Abbildung 3 dargestellt.
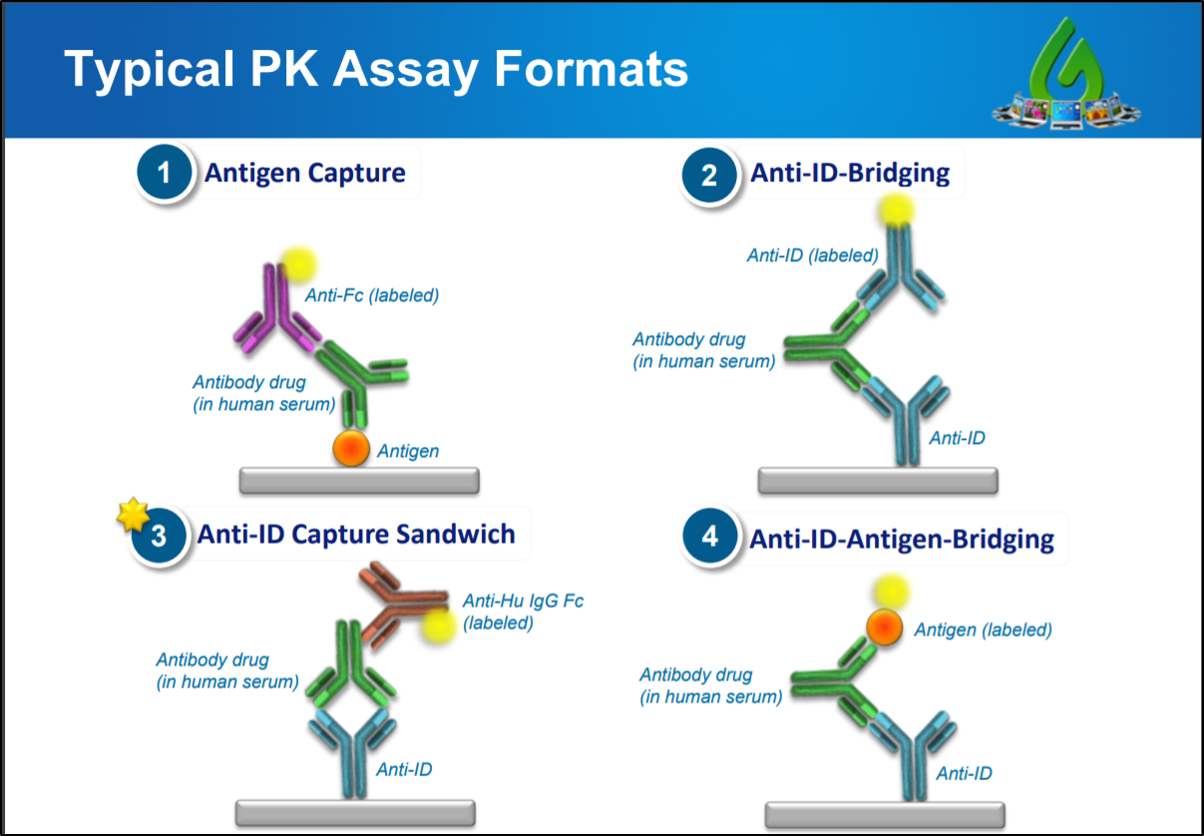
Abbildung 3. Arten von ELISA-basierten PK-Assays. Es gibt 4 gängige Methoden zur Durchführung eines ELISA-basierten PK-Assays. (1) Beim Antigen-Capture-Assay wird eine antigenbeschichtete Platte verwendet, die freie Antikörper binden soll. Ein markierter Anti-ID wird dann über die Antikörperdroge gewaschen, gebunden und visualisiert. Ein ähnliches Visualisierungsprotokoll wird für die anderen drei Arten von PK-Assays verwendet. (2) Bei einem Anti-ID-Bridging-Assay wird eine mit Anti-ID beschichtete Platte mit einem freien Antikörperwirkstoff und anschließend mit einem markierten Anti-ID überspült. (3) Bei einem Anti-ID-Capture-Sandwich-Assay wird eine mit Anti-ID beschichtete Platte mit einem markierten Anti-ID-IgG der konstanten Region gewaschen. (4) Bei einem Anti-ID-Antigen-Bridging-Assay wird eine Anti-ID-beschichtete Platte mit einem an ein markiertes Antigen gebundenen Antikörperwirkstoff gewaschen.
Immunogenitätstests
Polyklonale Anti-IDs werden in der Regel für Immunogenitätstests als Referenzkontrollen verwendet. Unter Immunogenität versteht man die Fähigkeit eines Therapeutikums, wie z.B. eines Antikörpermedikaments, eine humorale und/oder zellvermittelte Immunantwort zu induzieren, die zur Entwicklung von Anti-Drug-Antikörpern (ADAs) führt. ADAs führen dazu, dass alle Wirkungen des Antikörpermedikaments zunichte gemacht werden, so dass der therapeutische Aspekt des Medikaments im Wesentlichen vollständig gehemmt wird. Daher ist es für Forscher äußerst wichtig, die Immunogenität eines neuen Antikörpermedikaments während der präklinischen Analyse zu analysieren. Ein ADA ist einem Anti-IDs sehr ähnlich, da beide an denselben Antikörper-Wirkstoff binden. Daher kann ein Pool von polyklonalen Anti-IDs als Positivkontrolle verwendet werden, wenn das Vorhandensein von ADAs in Patientenproben analysiert wird. Ein Beispiel für einen ELISA-basierten Immunogenitätstest unter Verwendung eines Anti-IDs als Positivkontrolle ist in Abbildung 4 dargestellt.
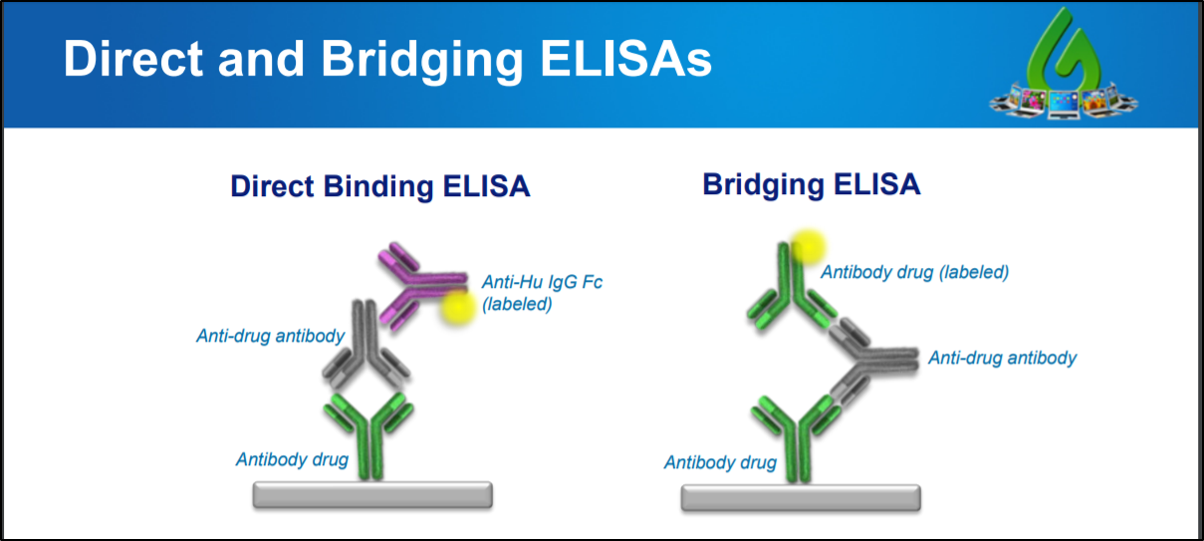
Abbildung 4. Arten von Immunogenitätstests. (A) Wenn ein Antikörper-Medikament die Entwicklung von ADAs induziert, können die ADAs durch einen direkten Bindungs-ELISA sichtbar gemacht werden. Bei diesem Assay wird eine mit einem Antikörperwirkstoff beschichtete Platte mit Serum gewaschen. Anschließend wird die Platte mit einem markierten IgG gewaschen, das sich nur an die konstante Region der ADAs bindet. Daher fluoresziert der ELISA nur, wenn ADAs im Probenserum vorhanden sind. (B) Bei einem Bridging-ELISA-Assay wird eine mit einem Antikörperwirkstoff beschichtete Platte mit ADA-haltigem Serum in Kontakt gebracht, das sich an eine ScFv-Region eines Antikörperwirkstoffs bindet. Die verbleibende ADA-ScFv-Region bindet an eine markierte Version desselben Antikörperwirkstoffs. Beide Assays müssen mit einer positiven Kontrolle, wie Anti-IDs, analysiert werden.
GenScripts Anti-Idiotyp-Antikörper-Generierungspakete
GenScript bietet jetzt verschiedene Anti-ID-Generierungspakete, die spezifisch für die Downstream-Anwendung, Wirtsspezies und Klonalität Ihrer Wahl sind. GenScripts Anti-ID-Generierungspakete umfassen….
Rodent mAb: Immunisieren Sie Mäuse oder Ratten mit Ihrem Antikörper-Medikament, um starke Anti-ID-Antikörper zu entwickeln, die in nur 3 Monaten für den perfekten Preis generiert werden! Zum Lieferumfang gehören stabile Hybridom-Zelllinien, gereinigte mAb und ein umfassender COA-Bericht, der den Blockierungstyp und die Spezifitätstests analysiert.
Kaninchen-MAb: Anti-ID-Antikörper, die mit der GenScripts MonoRabTM-Plattform erzeugt wurden, binden mit der höchsten Spezifität und Sensitivität auf dem Markt. Nach der hausinternen Analyse des Überstands des elterlichen Klons durchlaufen die positiven Klone die Sequenzierung der V-Region, was eine optimale rekombinante Expression des von Ihnen ausgewählten mAb ermöglicht. Dieses Paket enthält auch garantierte Lieferung eines zweiten Biotin-konjugierten Anti-ID-mAb-Paares, um einfache Generierung der Sandwich-ELISA-basierten PK-Analyse zu ermöglichen.
Kaninchen-pAb: GenScripts Kaninchen-pAbs bieten eine bequeme Durchlaufzeit und Preisspanne für Kunden, die an der Verwendung von polyklonalen Anti-IDs für Immunogenitätsanalyse interessiert sind. Mit unserem Express-Antikörper-Generierungsprotokoll und umfangreichem Reinigungs- und Screening-Prozess sind GenScripts Kaninchen-Anti-ID pAbs eine zuverlässige Option für Ihr nächstes Projekt.
Klicken Sie hier, um über fertige Anti-Idiotyp-Antikörper-Produkte gegen Blockbuster-Medikamente zu erfahren.
Anti-idiotype-Antikörper-Services
100% Erfolgsrate mit über 200 Projekten
Hohe Spezifität und Sensitivität
Downstream-Immunoassay-Entwicklungsservice

GenScripts Antikörper-Bild-Wettbewerb
Haben Sie einen mAb mit GenScripts Antikörper-Services generiert?
Haben Sie Mikroskopie mit diesem mAb durchgeführt?
Möchten Sie teilnehmen, um ein MacBook Pro zu gewinnen?
